1、选择题 下列说法正确的是( )
A.实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
B.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
C.Cl-存在时,铝表面的氧化膜易被破坏,因此含盐腌制食品不宜直接存放在铝制容器中
D.将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性
参考答案:A.海水中只有化合态的碘,实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤,然后需将碘离子氧化为碘单质,在提取的过程中用的氧化剂可以是H2O2,然后再萃取,故A错误;
B.乙醇在浓硫酸加热170℃发生消去反应生成乙烯气体,反应的化学方程式为CH3CH2OH浓硫酸
本题解析:
本题难度:一般
2、选择题 实验室中要使AlCl3溶液中的Al3+离子全部沉淀出来,适宜用的试剂是
A.NaOH溶液
B.Ba(OH)2溶液
C.盐酸
D.氨水
参考答案:D
本题解析:A、B项:都是强碱溶液,碱少量Al3+会剩余一部分留在溶液中,过量Al3+会转化为AlO2-在溶液中,所以在使用的多少的问题上无法确定,故错。C项:盐酸不与Al3+反应,故错。D项:加入氨水使Al3+转化为Al(OH)3沉淀,即使氨水过量沉淀也不溶解,故对。故选D。
点评:本题看的是铝离子(Al3+)与碱溶液的反应,学生要注意的是,在往含有氯离子(Al3+)的溶液中滴加强碱,现象为先有沉淀,后沉淀消失;若滴加弱碱氨水,则生成沉淀但不溶解。
本题难度:一般
3、填空题 生产着色铝片的工艺流程如下:
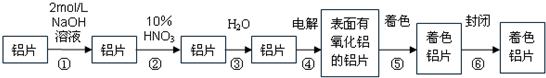
请回答下列问题:
(1)第①步中NaOH溶液的作用是______.
(2)第②步HNO3的作用是对铝片进行抛光,写出其反应的离子方程式______.
(3)在第④步电解是以铝为阴极,铝片为阳极,在硫酸介质中控制电压电流,使阳极放出O2与Al反应使铝表面形成一层致密的氧化膜.写出有关的电极反应式:阴极:______,阳极:______.
(4)氧化膜质量的检验:取出铝片干燥,在氧化膜未经处理的铝片上分别滴一滴氧化膜质量检查液(3gK2CrO4+75mL水+25mL浓盐酸),判断氧化膜质量的依据是______.
A.铝片表面有无光滑?B.比较颜色变化
C.比较质量大小?D.比较反应速率大小
(5)将已着色的铝干燥后在水蒸气中进行封闭处理约20~30min,封闭的目的是使着色的氧化膜更加致密,有关反应化学方程式是______.
参考答案:(1)因铝表面的油污,用热碱液除可以金属表面油污,故答案为:洗去铝表面的油污;
(2)因铝与硝酸反应:Al+4HNO3=Al(NO3)3+NO↑+2H2O,离子方程式为:Al+4H++NO3-=Al3++NO↑+2H2O,故答案为:Al+4H++NO3-=Al3++NO↑+2H2O;
(3)阴极是溶液中的阳离子H+得到电子:6H++6e-=H2↑;阳极是水中的氢氧根离子放电产生氧气,放出O2与Al反应使铝表面形成一层致密的氧化膜:2Al+3H2O-6e-=Al2O3+6H+,故答案为:6H++6e-=H2↑;2Al+3H2O-6e-=Al2O3+6H+;
(4)因K2CrO4是黄色的,其中的Cr(+6价)有氧化性能和Al反应应该是被还原成+3价(绿色),颜色发生了变化,故选:B.
(5)因Al和H2O(g)生成了氧化铝,所以化学方程式为:2Al+3H2O(g)?△?.? Al2O3+3H2(g),故答案为:2Al+3H2O(g)?△?.? Al2O3+3H2(g).
本题解析:
本题难度:一般
4、选择题 某研究性学习小组为了探究镁粉与溴水反应的机理,做了如下四组实验:①将镁粉投入冷水中,未见任何现象;②将镁粉放入溴水中,观察到只是开始时产生极少量的气泡,但溴水的颜色逐渐褪去;③将镁粉放入液溴中,未观察到任何明显现象;④向含足量镁粉的液溴中滴加几滴水,观察到溴的红棕色很快褪去.则下列关于镁与溴水的反应机理的论述中正确的是( )
A.镁粉只直接与溴水中的溴反应
B.镁粉只与溴水中的酸反应
C.产生极少量的气泡是由于镁粉与水反应得到
D.镁粉在水的催化下与溴发生反应
参考答案:D
本题解析:
本题难度:一般
5、填空题 向20 mL某物质的量浓度的AlCl3溶液中滴入2 mol/L NaOH溶液时,得到的Al(OH)3沉淀质量与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题
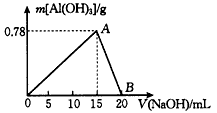
(1)图中A点表示的意义是____________________。
(2)图中B点表示的意义是____________________。
(3)上述两步反应用总的离子方程式可表示为___________________。
(4)若溶液中有Al(OH)3沉淀0.39 g,则此时用去NaOH溶液的体积为____________________。
参考答案:(1)生成Al(OH)3沉淀的最大值
(2)Al(OH)3沉淀完全溶解于NaOH溶液成为NaAlO2溶液
(3)Al3++4OH-=AlO2-+2H2O
(4)7.5 mL或17.5 mL
本题解析:
本题难度:一般