1������� ��֪�����Ȼ�ѧ����ʽ����H2��g�� +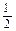 O2��g����H2O��l�� ��H="-285" kJ��mol-1
O2��g����H2O��l�� ��H="-285" kJ��mol-1
��H2��g�� +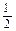 O2��g����H2O��g�� ��H="-241.8" kJ��mol-1?��C��s�� +
O2��g����H2O��g�� ��H="-241.8" kJ��mol-1?��C��s�� +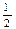 O2��g����CO��g�� ��H="-110.5" kJ��mol-1
O2��g����CO��g�� ��H="-110.5" kJ��mol-1
�� C��s�� +O2��g����CO2��g�� ��H="-393.5" kJ��mol-1?�ش��������⣺
��1��H2��ȼ����Ϊ?��C��ȼ����Ϊ?��
��2��ȼ��1gH2����Һ̬ˮ���ų�������Ϊ?��
��3��д��COȼ�յ��Ȼ�ѧ����ʽ?��
�ο��𰸣���1��285? 393��5
��2��142��5
��3��CO��g��+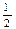 O2��g����CO2��g��? ��H="-283" kJ��mol-1
O2��g����CO2��g��? ��H="-283" kJ��mol-1
�����������
�����Ѷȣ���
2��ѡ���� ����˵����ȷ���ǣ�?��
A��pH=2��pH=l��������c��H+��֮��Ϊ10��1
B��һԪ����һԪ��ǡ����ȫ��Ӧ�����Һ��һ������c��H+��=c��OH-��
C��KAl��SO4��2��Һ������Ũ�ȵĴ�С˳��Ϊc��SO2-4��>c��K+��>c��Al3+��>c��H+��>c��OH-��
D�������£���pH��Ϊ12�İ�ˮ��NaOH��Һ�ֱ��ˮϡ��100����NaOH��Һ��pH�ϴ�
�ο��𰸣�C
���������A:pH=2��pH=l��������c��H+��֮��Ϊ1��10���ų�
B������кͺ���Һ��һ�������ԣ�c��H+����c��OH-����һ����ȣ�����ȷ
C�����������Ӳ���ˮ�⣬��Һ�����ԣ���ȷ
D������������ڵ���ƽ�⣬��ϡ�����п��Դٽ�����룬��ϡ����ͬ������ˮ��pH�ϴ���ȷ
��ΪC
�����Ѷȣ���
3��ѡ���� �ڲ�ͬ�¶��£�ˮ��Һ��c(H��)��c(OH��)����ͼ��ʾ��ϵ������˵����ȷ���ǣ�?��

A��a���Ӧ����Һ��c���Ӧ����ҺpHֵ��С��
pH��c����pH��a��
B��d���Ӧ����Һ�д������ڣ�K+��Ba2����NO3����I��
C��25��ʱ��Ka(HF)��3.6��10��4,Ka��CH3COOH����1.75��10��5,?
0.1mol/L��NaF��Һ��0.1mol/L ��CH3COOK��Һ��ȣ�
c(Na��)��c(F��)��c(K��)��c(CH3COO��)
D����b���Ӧ����Һ��ֻ��NaHA������Һ������Ũ�ȴ�С��
c(HA��)��c(H2A)��c(H��)��c(A2��)
�ο��𰸣�B
���������A����ͼ��֪��a���Ӧ����25��ʱ��ˮ������Ũ�ȣ�c(H��)=1��10��7mol/L,pH=7,c���Ӧ����T��ʱ��ˮ������Ũ�ȣ�c(H��)=1��10��6mol/L,pH=6,����pH��c��<pH��a��,����B��T��ʱ��ˮ�����ӻ�������1��10��12����d���Ӧ����Һ��c(H��)=1��10��7mol/L<c(OH��)=1��10��5mol/L,������Һ�ʼ��ԣ�����������K+��Ba2����NO3����I��������Ӧ�����Դ������棬��ȷ��C������������ĵ��볣����֪HF�����Աȴ��������ǿ�����Ե�Ũ�ȵ�NaF��Һ��ˮ��̶ȱ�CH3COOK��Һˮ��̶�����c(F��)> c(CH3COO��),c(Na��)= c(K��)����c(Na��)��c(F��)<c(K��)��c(CH3COO��)������D��ͬ����֪b���Ӧ����Һ�����ԣ�˵��NaHA��Һ��HA-�ĵ���̶ȴ�����ˮ��̶ȣ�������Ũ�ȵĴ�С��ϵ��c(HA��)��c(H��)��c(A2��) ��c(H2A)������ѡB��
�����Ѷȣ�һ��
4��ѡ���� ������ʱ�������ΪV1��Ũ��Ϊc1��pH=a�Ĵ�����Һ�м������ΪV2��Ũ��Ϊc2��pH=b������������Һ����ַ�Ӧ�����й��ڷ�Ӧ����Һ������һ����ȷ����
A����pH=7����V1=V2����c1>c2
B����pH<7����c(CH3COO-)>c(Na+)>c (H+)>c (OH-)
C����cl=c2����V1=V2����a+b=14
D����pH>7����V1=V2����cl<c2
�ο��𰸣�A
���������A�������Ϊ������ҵ�Ũ�ȣ���ǡ���кͣ����Դ�������Һ�ʼ��ԣ�����ֻ�е�c1>c2��������pH=7����A��ȷ
B����pH<7��ֻ˵��c (H+)>c (OH-)������c(CH3COO-)��c(Na+)����Դ�С��ȷ����
C��������ΪһԪǿ�ᣬ��cl=c2ʱ��a+b=14������ʵ����Ϊ���ᣬ����a+b>14
D����cl=c2ʱ���������ͬ���кͺ�Ϊ��������Һ��pHҲ���Դ���7
�����Ѷȣ�һ��
5��ѡ���� һЩ������ȼ�������±������б�����ȷ���ǣ�������
| ���� | ȼ����/kJ?mol-1 | ���� | ȼ����/kJ?mol-1
����
891.0
������
2878.0
����
1560.8
�춡��
2869.6
����
2221.5
������
3531.3
|
A���������ȼ����С��3531.3?kJ?mol-1
B���ȶ��ԣ������飾�춡��
C������ȼ�յ��Ȼ�ѧ����ʽΪ2C2H6��g��+7O2��g���T4CO2��g��+6H2O��g����H=-1560.8?kJ?mol-1
D����ͬ���ʵ���������CnH2n+2��nԽ��ȼ�շų�������Խ��
�ο��𰸣�A���������2-�����黥Ϊͬ���칹�壬�ɱ����������顢�춡���ȼ���ȱȽϿ�֪����Ϊͬ���칹��Ļ����֧�����ȼ����С�����������ȼ���ȴ���2-�����飬
���������ȼ���ȴ�Լ��3540KJ/mol���ң��Ҵ���3531.3KJ/mol����A����
B���ɱ����е����ݿ�֪���춡���ȼ���ȱ��������ȼ����С�����춡��������ͣ������ȶ���Ϊ�����飼�춡�飬��B����
C����������ȼ���ȵĺ��壺��ȫȼ��1mol�������ɶ�����̼��Һ̬ˮʱ��ų�1560.8KJ�������������Ȼ�ѧ����ʽΪ2C2H6��g��+7O2��g��=4CO2��g��+6H2O��l������H=-3121.6kJ/mol����C����
D����ͬ���ʵ�����������̼�����ʵ�������Խ��ȼ�շ���Խ�࣬��nԽ��ȼ�շų�������Խ�࣬��D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��