1、填空题 (15分)铁、铝、铜等金属及其化合物在日常生活中应用广泛,请根据下列实验回答问题:
(1)单质铁属于______晶体,将FeCl3溶液加热蒸干,灼烧所得的物质是______ (填化学式):
(2)请写出铝与氢氧化钠溶液反应的化学方程式______________________________
(3)金属Cu单独与氨水或单独与双氧水都不反应,但可与二者的混合溶液反应生成深蓝色溶液,在该深蓝色的浓溶液中加入乙醇所产生的现象是______,画出呈深蓝色的离子的结构式______.
写出Cu与氨水、双氧水反应的离子方程式:____________________________________.
(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,写出其化学方程式____________.
参考答案:(1)金属晶体(1分),Fe2O3(2分)
(2)2Al+2NaOH+2H2O=2NaAlO2+3H2↑(3分)
(3)析出深蓝色晶体(1分)?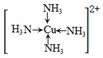 (2分)
(2分)
Cu+4NH3・H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-(3分)
(4)FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O(3分)
本题解析:(1)单质铁属于金属晶体,FeCl3溶液存在Fe3+ + 3H2O  Fe(OH)3 + 3H+,加热蒸干促进水解生成氢氧化铁沉淀、灼烧氢氧化铁分解得Fe2O3;(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(3)金属Cu与双氧水发生氧化还原反应,生成的铜离子随即与一水合氨中的氮形成配位键,这种离子化合在乙醇中溶解度小而析出深蓝色晶体,其结构为
Fe(OH)3 + 3H+,加热蒸干促进水解生成氢氧化铁沉淀、灼烧氢氧化铁分解得Fe2O3;(2)铝与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑;(3)金属Cu与双氧水发生氧化还原反应,生成的铜离子随即与一水合氨中的氮形成配位键,这种离子化合在乙醇中溶解度小而析出深蓝色晶体,其结构为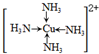 ,离子方程式是Cu+4NH3?H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-;(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,同时碳酸氢根离子电离出的氢离子与碳酸氢根离子结合成二氧化碳和水,化学方程式为FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O。
,离子方程式是Cu+4NH3?H2O+H2O2=[Cu(NH3)4]2++4H2O+2OH-;(4)在硫酸亚铁溶液中加入过量的碳酸氢铵,有FeCO3沉淀生成,同时碳酸氢根离子电离出的氢离子与碳酸氢根离子结合成二氧化碳和水,化学方程式为FeSO4+2NH4HCO3=FeCO3↓+CO2↑+(NH4)2SO4+H2O。
本题难度:一般
2、填空题 (三选一)【物质结构与性质】
已知X、Y和Z三种元素的原子序数之和等于48。X的一种1:1型氢化物分子中既有σ键又有π 键。Z是金属元素,Z的单质和化合物有广泛的用途。已知Z的核电荷数小于28,且次外层有2 个未成对电子。工业上利用ZO2和碳酸钡在熔融状态下制取化合物M(M可看做一种含氧酸盐)。M有显著的“压电性能”,应用于超声波的发生装置。经X射线分析,M晶体的最小重复单位为正方体(如图),边长为4.03×10-10m,顶点位置为Z4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占。
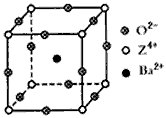
(1)Y在周期表中位于________;Z4+的核外电子排布式为_______________
(2)X的该种氢化物分子构型为____________,X在该氢化物中以____方式杂化。X和Y形成的化合物的熔点应该____(填“高于”或“低于”)X氢化物的熔点。
(3)①制备M的化学反应方程式是____________________;
②在M晶体中,若将Z4+置于立方体的体心,Ba2+置于立方体的顶点,则O2-处于立方体的____;
③在M晶体中,Z4+的氧配位数为________;
④已知O2-半径为1.40×10-10m,则Z4+半径为_________m。
参考答案:(1)第四周期第ⅡA族;1s22s22p63s23p6
(2)直线形;sp;高于
(3)①TiO2+BaCO3=BaTiO3+CO2↑;②面心;③6;④6.15×10-13
本题解析:
本题难度:一般
3、选择题 氰气(CN)2的结构如下,性质与氯气相似,下列关于氰气的说法正确的是
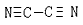
[? ]
A.一定条件下可发生加成反应
B.分子中含有两个σ键和4个π键
C.分子中 键的键长大于C-C键的键长
键的键长大于C-C键的键长
D.固态时属于原子晶体
参考答案:A
本题解析:
本题难度:一般
4、选择题 下图立方体中心的“●”表示金刚石晶体中的一个碳原子,立方体顶点的“●”表示与之紧邻的碳原子,其中正确的是
[? ]
A.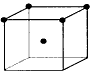
B.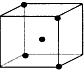
C.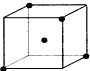
D.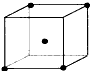
参考答案:C
本题解析:
本题难度:简单
5、填空题 (6分). 金晶体是面心立方体,立方体的每个面上5个金原子紧密堆砌(如图3,其余各面省略),金原子半径为A cm,求:
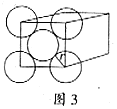
(1)金晶体中最小的一个立方体含有___________个金原子。
(2)金的密度为___________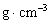 。(用带A计算式表示)
。(用带A计算式表示)
(3)金原子空间占有率为___________。(Au的相对原子质量为197,
用带A计算式表示)
参考答案:(1)4?(2) ?(3)
?(3)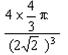
本题解析:(1)根据晶胞结构可知,金晶体中最小的一个立方体含有(8×1/8+6×1/2)=4个金原子。
(2)金原子半径为A cm,则晶胞中面对角线是4Acm,所以晶胞的边长是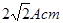 ,所以
,所以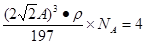 ,解得
,解得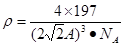 。
。
(3)晶胞的体积是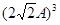 ,而金原子占有的体积是
,而金原子占有的体积是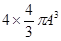 ,所以金原子空间占有率为
,所以金原子空间占有率为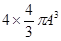 /
/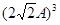 =
=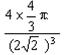 。
。
本题难度:一般