| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点整理《电解质溶液中离子浓度大小的比较》高频考点强化练习(2017年最新版)(四)
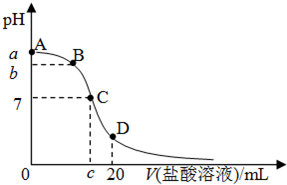 参考答案:A、在A、C间任一点,当盐酸的量很少时,溶液中以氨水的电离为主,所以溶液中离子存在的关系可能是c(NH4+)>c(OH-)>c(Cl-)>c(H+),故A错误. 本题解析: 本题难度:简单 3、选择题 物质的量浓度相同的下列溶液,pH由大到小排列正确的是 参考答案:B 本题解析: 本题难度:一般 4、选择题 常温下,一定量的醋酸与氢氧化钠溶液发生中和反应,当溶液中 参考答案:A 本题解析: 本题难度:一般 5、选择题 已知乙酸(HA)的酸性比甲酸(HB)弱且均为弱酸,在物质的量浓度均为0.1 moI/L的NaA和NaB混合溶液中,下列排列正确的是 参考答案:A 本题解析: 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《氧化钠与过.. | |