1、选择题 当金属钠着火时可以用作灭火的物质或器材的是(?)
A.水
B.砂
C.煤油
D.泡沫灭火器
参考答案:B
本题解析:2Na+2H2O 2NaOH+H2↑,H2易燃,故A不行;泡沫灭火器中有水,且能产生CO2,Na燃烧时生成的Na2O2与CO2、H2O都能反应,也不能灭火,故D错;C是火上浇油,只有B项符合题意。
2NaOH+H2↑,H2易燃,故A不行;泡沫灭火器中有水,且能产生CO2,Na燃烧时生成的Na2O2与CO2、H2O都能反应,也不能灭火,故D错;C是火上浇油,只有B项符合题意。
本题难度:简单
2、计算题 t ℃时,将一定质量的钠投入到24.6 g水中,恰好得到t ℃时的饱和溶液31.2 g,则投入的钠的质量为多少克?t ℃时,NaOH的溶解度为多少?
参考答案:6.9 g? 62.5 g
本题解析:2Na+2H2O="===2NaOH?" +? H2↑
2×23? 2×40? 2
m(Na)?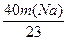 ?
?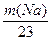
据质量守恒m(Na)+24.6 g-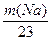 ="31.2" g
="31.2" g
m(Na)="6.9" g
m(NaOH)="12" g
设溶解度为S,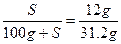
解出S="62.5" g。
本题难度:简单
3、选择题 等质量的钠进行下列实验,其中生成氢气最多的是
A.将钠投入到足量水中
B.将钠放入足量稀盐酸中
C.将钠放入足量稀硫酸中
D.将钠用铝箔包好并刺一些小孔,再放人足量的水中
参考答案:D
本题解析:钠溶于水生成氢氧化钠和氢气,则在钠的质量相等的条件下,生成的氢气相同。但选项D中生成的氢氧化钠还能和金属铝生成氢气,所以D中生成的氢气最多,答案选D。
点评:该题是中等难度的试题,试题基础性强,在注重对学生基础知识巩固和训练的同时,侧重对学生能力的培养。该题的关键是注意铝也能和氢氧化钠溶液,有利于培养学生的灵活应变能力。
本题难度:一般
4、填空题 碱金属能形成离子型氢化物。如氢化钠的化学式为NaH,其中H-具有较强的还原性。
(1)常用NaH在高温下将TiCl4还原成Ti,反应的化学方程式为_________________________。
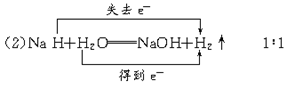
(2)NaH能与水剧烈反应生成对应的碱和氢气,反应的化学方程式为_________________ ,并在化学方程式中标明电子转移的方向和数目。该反应中氧化产物和还原产物的质量比为_____________________。
参考答案:(1)2NaH+TiCl4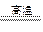 Ti+2NaCl+2HCl↑
Ti+2NaCl+2HCl↑
本题解析:(1)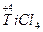

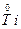 ,Ti元素价态降低,得电子,是氧化剂,NaH和TiCl4反应,谁的价态升高?显然是还原性的H-,Ti已变为单质,Na、H、Cl三元素如何结合?生成NaCl、HCl是必然结果:
,Ti元素价态降低,得电子,是氧化剂,NaH和TiCl4反应,谁的价态升高?显然是还原性的H-,Ti已变为单质,Na、H、Cl三元素如何结合?生成NaCl、HCl是必然结果:
2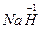 +
+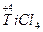 (原子的重新组合)
(原子的重新组合)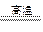 2NaCl+2
2NaCl+2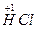 ↑+
↑+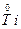 ,用化合价升降总值相等进行验证,十分合理。
,用化合价升降总值相等进行验证,十分合理。
(2)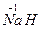 与
与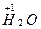 反应生成
反应生成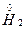 ,发生了氧化还原反应,从价态变化看,应该是+1价H原子得到了-1价H原子的电子。又由于H2O可以发生微弱的电离――水是极弱电解质,所以生成的碱应为NaOH:
,发生了氧化还原反应,从价态变化看,应该是+1价H原子得到了-1价H原子的电子。又由于H2O可以发生微弱的电离――水是极弱电解质,所以生成的碱应为NaOH:
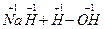 ====NaOH+H2↑
====NaOH+H2↑
(正、负相互吸引,一种化合价的正价原子或原子团跟另一种化合物中的负价原子或原子团重新结合)用化合价升降总值相等验证,也是合理的。
H2既是氧化产物,又是还原产物。
本题难度:简单
5、选择题 下列粒子中最易获得电子的是(? )
A.Li+
B.Na+
C.K+
D.Cs+
参考答案:A
本题解析:单质的还原性越弱,对应的阳离子的氧化性越强。
本题难度:简单