1��ѡ���� ���й��ڼ����Ԫ�ص���������ȷ���ǣ�?��
A���ر��Ƹ����ã��ڷ�Ӧ�и���ʧȥ���ӣ���������
B���Ʊ�ͭ���ã�����Ͷ��CuSO4��Һ���е���ͭ��������������������
C���Ƶ��۵�ϵͣ����۵����ˮ�ķе�
D���Ƶ��ܶȽ�С�����ܶȱ�ú��С
�ο��𰸣�C
����������ƺܻ��ã�������Һ�Ӵ�ʱ������ˮ�������ò�����������������ˮ����ʱ������ˮ�棬���ۻ���С��˵���ܶȱ�ˮС������ú�ʹ�
�����Ѷȣ���
2��ѡ���� ��NH4HCO3���ڸɵ��Թ��м��ȣ���ʹ�ų�����������ͨ��ʢ�������������ƺͼ�ʯ�ҵĸ���ܣ����õ��������У�?��?
A��NH3��O2
B��H2O��O2
C��CO2��O2
D��O2
�ο��𰸣�A
���������NH4HCO3���ȷֽ�ĵIJ����ǰ�����CO2��ˮ��������ͨ��ʢ�������������Ƶĸ���ܣ�CO2��ˮ���������գ�ͬʱ������������ͨ��ʢ��������ʯ�ҵĸ���ܣ��������������ܱ����գ��������յ�������ǰ�������������A��
�����Ѷȣ�һ��
3��ʵ���� ��12�֣�NaHCO3��Na2CO3��xH2O�Ļ���Ϊ�˲ⶨxֵ��ijͬѧ������ͼ��ʾ��װ�ý���ʵ��(CaCl2����ʯ�Ҿ�����)��
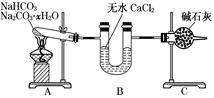
��1��Aװ�õ�������____________________________��
��2��Bװ�õ�������____________________________��
��3��Cװ�õ�������____________________________��
��4������װ��A���Թ���װ��NaHCO3��Na2CO3��xH2O�Ļ����3.7 g���þƾ��Ƽ��ȵ���Ӧ��ȫ����ʱB������1.89 g��C������0.22 g����x��ֵΪ??��
��5����װ�û����Ǻ����ƣ�����ʹ�ⶨ���ƫС��Ӧ��θĽ�________��Ϊʲô��
�ο��𰸣���1�����ȣ�ʹNaHCO3�ֽ⣬ʹNa2CO3��xH2Oʧˮ
��2�����շ�Ӧ�����ɵ�ˮ����3�����շ�Ӧ�����ɵ�CO2
��4��10
��5����Cװ�ú��ټ�һ��װ�м�ʯ�ҵ�U�ιܡ�
Ϊ�˷�ֹ�����е�CO2��H2O��Cװ���еļ�ʯ������
����������Ӹ�ʵ���Ŀ�ĺ�Ҫ����������1��Aװ�õ������Ǽ��ȣ�ʹNaHCO3�ֽ⣬ʹNa2CO3��xH2Oʧˮ����2��Bװ�õ����������շ�Ӧ�����ɵ�ˮ����3��Cװ�õ����������շ�Ӧ�����ɵ�CO2��
��4������װ��A���Թ���װ��NaHCO3��Na2CO3��xH2O�Ļ����3.7 g���þƾ��Ƽ��ȵ���Ӧ��ȫ����ʱB������1.89 g��C������0.22 g����A��B��C�������ÿ��Կ�����A���Թ���װ��NaHCO3��Na2CO3��xH2O�Ļ����������3.7 g��B������1.89 g������NaHCO3�ֽ������ˮ����Na2CO3��xH2Oʧȥ��ˮ��C������0.22 g��������̼�����Ʒֽ�����Ķ�����̼���ɶ�����ϵ��֪��2NaHCO3=Na2CO3��H2O ��CO2�� ��̼�����Ʒֽ�����Ķ�������ˮ�����ʵ�������ͬ�ġ����Լ����ϵ���£�
2NaHCO3?= ?Na2CO3?��? H2O?��? CO2��
168? 1? 18? 44
Z=0.84g? Y="0.09" g? 0.22 g
����Na2CO3��xH2O��������3.7 g-0.84g=2.86g?��
����Na2CO3��xH2O�е�ˮ��������1.89g-0.09g=1.8g
����x��ֵΪ10��
��5����װ�û����Ǻ����ƣ�����ʹ�ⶨ���ƫС��Ӧ��Cװ�ú��ټ�һ��װ�м�ʯ�ҵ�U�ιܡ�
Ϊ�˷�ֹ�����е�CO2��H2O��Cװ���еļ�ʯ�����ա�
��������Ϥ̼�����ƺ�̼���Ƶ����ʴ������ⲻ�ѽ����
̼�����ƵĻ�ѧ����
1.���ᷴӦ
��HCl��Ӧ��NaHCO?+HCl ="===" NaCl+ H?O+ CO?��
��CH?COOH��Ӧ��NaHCO?+CH?COOH====CH?COONa+H?O+CO?��
2.��Ӧ
���������Ʒ�Ӧ��NaHCO?+NaOH="===" Na2CO?+ H2O
���������Ʒ�Ӧ��Ҫ�ֹ�����������
������NaHCO?+ Ca(OH)?="===" CaCO?+ NaOH + H?O������2NaHCO?+ Ca(OH)?="===" Na2CO?+ CaCO?��+ 2H?O
3.����
���ȷֽ⣺2NaHCO?==��="=" Na?CO?+ H?O + CO?��
4.����
̼�����Ƶ��뷽��ʽ NaHCO?="Na+" + HCO3����
̼���ƵĻ�ѧ����
1 �绯
̼���ƵĽᾧˮ����ʯ��(Na2CO3��10H2O)�ڸ���Ŀ������绯��
Na2CO3��10H2O====Na2CO3+10H2O
2 ���ᷴӦ
Na2CO3+ 2HCl�������� ="===" 2NaCl +H2CO3
̼��ȶ����ֽ�ɶ�����̼��ˮ
H2CO3====H2O + CO2��
Na2CO3+ HCl�������� ="===" NaCl + NaHCO3
3 ��Ӧ
Na2CO3+ Ca(OH)2="===" 2NaOH + CaCO3����̼��ư�ɫ������������ˮ�����������ᣩ
4 ���η�Ӧ
Na2CO3+ BaCl2="===" 2NaCl + BaCO3����̼�ᱵ��ɫ������������ˮ�����������ᣩ
3Na2CO3+ Al2(SO4)3+ 3H2O ="===" 2Al(OH)3��+ 3Na2SO4+ 3CO2��
������������ɫ������������ˮ���������ᡢ�
Na2CO3+CaCl2=====2NaCl+CaCO3��
5 ��H2O��CO2��Ӧ
Na2CO3+ H2O + CO2="===" 2NaHCO3���ڼ��Ի����г���������
�����Ѷȣ�һ��
4��ѡ���� ��8gNa2O2��Na2O��Na2CO3��NaOH�Ļ����Һ��200g��������Ϊ3.65%������ǡ����ȫ��Ӧ��������Һ�����յù�������Ϊ
A��8g
B��15.5g
C��11.7g
D��������
�ο��𰸣�C
���������
��ȷ�𰸣�C
����ԭ���غ㣺Clԭ��ȫ����NaCl�У�m(NaCl)=200g��3.65%��36.5g��mol-1��58.5g��mol-1=11.7g
�����Ѷȣ�һ��
5��ѡ���� ��һ��ɫ�����ĩ������̼���ơ��������ơ��������е�һ�ֻ���֣�ij��ȤС����Ը���Ʒ����̽����
��1��ȡ������Ʒ�ܽ���ˮ���ܽ����õIJ���������?��
�ⶨ��Һ��pH���������Һ��pH=7������Ʒ��һ������?��
��2�����Ҫ�������Ʒ�Ƿ��������ƣ�ij�˵ķ������£�ȡ������1������Һ��?
?����д���Լ��������ۣ�
��3��ȡ����������Ʒ������������У�������ų�����Ҫ����ų��������ɣ����������Լ���ѡ����ʵ��Լ����һ�����ʵ������û���������ɣ���Ҫд��ʵ�鷽��������ͽ��ۡ�
���Լ���Ʒ����Һ������ʯ��ˮ������KMnO4��Һ����������Ũ��Һ������NaHCO3��Һ��
ʵ�鷽��
| ���ܵ��������Ӧ�Ľ���
|
�������������ͨ��ʢ��?��?��?__��ϴ��ƿ��
| ?
|
?
�ο��𰸣���16�֣�
��1���ձ�����������2�֣���1�֣���?������ ��1�֣���?
��2�����������ᣨ1�֣�����ַ�Ӧ�������������ټ�������BaCl2��Һ��1�֣������г�������˵����Ʒ����Na2SO4��1�֣�������������˵��˵����Ʒ��û��Na2SO4��1�֣��� ����4�֣�
ע�⣺����˵����1�֣���Ba(NO3)2���۷֡�
��3������9�֣�
ʵ�鷽��
���ܵ��������Ӧ�Ľ���
Ʒ����Һ��
������������KMnO4��Һ��������������ʯ��ˮ
��3�֣���1�֣�
��Ʒ����ɫ������KMnO4��Һ����ȫ��ɫ������ɫ��������ʯ��ˮ����ǣ���1�֣���������SO2��CO2�Ļ�����壨1�֣���
��Ʒ����ɫ������KMnO4��Һ����ȫ��ɫ������ɫ��������ʯ��ˮ������ǣ���1�֣���������SO2��1�֣���
��Ʒ�첻��ɫ������KMnO4��Һ����ɫ������ʯ��ˮ����ǣ���1�֣���������CO2��1�֣���
���������
��1���ܽ����õIJ��������У��ձ�����������̼���ƺ����������Һ�У���Ϊ������ˮ�����Һ��ʾ���ԣ�ֻ���������Dz�ˮ����Σ������ԣ��ʴ�Ϊ�������ƣ�
��2��Ҫ�������Ʒ�Ƿ��������ƣ�ֻ��������е���������Ӽ��ɣ�������������ӵ��������ӷ�Ӧ���ܺͱ����ӷ�Ӧ���ɲ���������İ�ɫ���������У�ע�ⲻ�������ᣬ������������ԣ��ܽ������������������
�ʴ�Ϊ��ȡ����������Ʒ������������У�Ȼ�����BaCl2��Һ�����г�������˵����Ʒ����Na2SO4������������˵��˵����Ʒ��û��Na2SO4��
��3��ȡ����������Ʒ������������У�������ų����������Ƕ�����̼�Ͷ��������е�����һ�֣���������Ͷ�����̼����ʹ����ʯ��ˮ����ǣ��ڼ��������̼֮ǰ�ȼ����������Ĵ��ڲ��������������������ó���ʯ��ˮ�����������̼����������ļ���ʹ��Ʒ�죬��ȥ������������ø�����أ�������̼�ļ����ó���ʯ��ˮ���ʴ�Ϊ��
ʵ�鷽��
���ܵ��������Ӧ�Ľ���
Ʒ����Һ��
������������KMnO4��Һ��������������ʯ��ˮ
��3�֣���1�֣�
��Ʒ����ɫ������KMnO4��Һ����ȫ��ɫ������ɫ��������ʯ��ˮ����ǣ���1�֣���������SO2��CO2�Ļ�����壨1�֣���
��Ʒ����ɫ������KMnO4��Һ����ȫ��ɫ������ɫ��������ʯ��ˮ������ǣ���1�֣���������SO2��1�֣���
��Ʒ�첻��ɫ������KMnO4��Һ����ɫ������ʯ��ˮ����ǣ���1�֣���������CO2��1�֣���
�����Ѷȣ���