1��ѡ���� ������ͨ�����з�ɢϵʱ���ܹ۲쵽�����ЧӦ����
A.����
B.Fe(OH)3����
C.NaCl��Һ
D.CuSO4��Һ
�ο��𰸣�B
�������������ͨ������ʱ�Ż���������ЧӦ��
A�����ᣬC��NaCl��Һ��D��CuSO4��Һ����������Һ��ֻ��B��Fe(OH)3�������ڽ��塣
��ѡB
�����Ѷȣ�һ��
2������� �±�ΪԪ�����ڱ���һ���֣������Ԫ��A��H�ڱ��е�λ�ã�
��
 ���� ����
| IA
| ?
| 0
|
1
| A
| ��A
| ��A
| ��A
| ��A
| ��A
| ��A
| ?
|
2
| ?
| ?
| ?
| B
| C
| D
| ?
| ?
|
3
| E
| ?
| F
| G
| ?
| ?
| H
| ?
|
�û�ѧ����ش��������⣺
��1��D��E��F��ԭ�Ӱ뾶�ɴ�С��˳��Ϊ_________________________��
��2��B��C��D�ĵ�һ�������ɴ�С��˳��Ϊ_________________________��
 ��3��A��D��E��H�е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ����д������һ�ֻ�����ĵ���ʽ��____________________��
��3��A��D��E��H�е�ijЩԪ�ؿ��γɼȺ����Ӽ��ֺ����Թ��ۼ��Ļ����д������һ�ֻ�����ĵ���ʽ��____________________��
 (4) E��F������������ˮ�������Ӧ�����ӷ���ʽ?
(4) E��F������������ˮ�������Ӧ�����ӷ���ʽ? ?��
?��
��5����B���γɵĻ�����CH4��CO��CH3OH�У�̼ԭ�Ӳ�ȡsp3�ӻ��ķ���������������
��CO���ӻ�Ϊ�ȵ�����ķ��Ӻ��� �ӷֱ�Ϊ?������?�����ݵȵ�����
�ӷֱ�Ϊ?������?�����ݵȵ�����
���Ʋ�CO���ӵĽṹʽ�ɱ�ʾ����������һ��CO���������������Ҽ��������ݼ���
��6������VSEPR����Ԥ��D��H���γɵ�HD4�� ���ӵĿռ乹��Ϊ______________�͡�
(7)��A��B��C��D��EԪ����ɵ�10���������У�����λ������?��?��
�ο��𰸣���1��Na��Al��O?
(2)N��O��C
 ?
?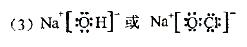
(4)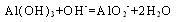
(5) CH4��CH3OH? N2? C22��?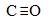 ?1? 2
?1? 2
��6������������
��7��NH4+? H3O+
�����������
�����Ѷȣ���
3��ѡ���� ����˵��������ǣ�����
A��1.5g CH3+�к��еĵ�����Ϊ0.8NA
B��CuԪ����Ԫ�����ڱ���ds��
C��s�����Բ�Σ�p�����������
D��DNA�еļ�����������ͨ�������ʵ�ֵ�
�ο��𰸣�C
���������CH3+�к��еĵ���8��1.5g CH3+��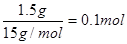 ������A��ȷ��ͭ���ڵ�IB��λ��ds����B��ȷ��P����ǷĴ��εģ�C�Ǵ���ġ������ʺ��е�Ԫ�أ������γ������D��ȷ�����Դ�ѡC
������A��ȷ��ͭ���ڵ�IB��λ��ds����B��ȷ��P����ǷĴ��εģ�C�Ǵ���ġ������ʺ��е�Ԫ�أ������γ������D��ȷ�����Դ�ѡC
�����Ѷȣ�һ��
4��ѡ���� Ԫ�����ʳ������Ա仯��ԭ���� (? )
A�����ԭ������������
B���˵����������
C��ԭ�Ӻ�������Ų��������Ա仯
D��Ԫ�صĻ��ϼ۳������Ա仯
�ο��𰸣�C
���������A��Ԫ�ص�ԭ�ӵ����ԭ���������������������Եı仯�����ܾ���Ԫ�����ʳ��������Ա仯����A����
B��ԭ����������ֵ�ϵ�������ԭ�ӵĺ˵����������ԭ�������������˵���������������ֹ����Եı仯����B����
C����ԭ�ӵĵ����Ų���֪����ԭ�������ĵ��������Ӳ��������������������������Եı仯������Ԫ�����ʵ������Ա仯����ԭ�ӵĵ��Ӳ��Ų��������Ա仯������Ԫ�����������Ա仯�ľ������أ���C��ȷ��
D��Ԫ�ص���������ϼ۵������Ա仯��ԭ�ӵĵ����Ų������Ա仯�Ľ�������ϼ�����Ԫ�ص����ʣ���D����
��ѡ��C��
����������Ҫ����Ԫ�������ɵ�ʵ�ʣ�Ԫ�����ʵ������Ա仯��Ԫ��ԭ�ӵĺ�������Ų��������Ա仯�ı�Ȼ�����
�����Ѷȣ���
5��ѡ���� 2011��3��11�����ձ������Ĵ�����У������˵�վ�����˺�й©�����ܱ�����Ŀ�����Ư���ŷ��������ʣ����к��е��ͬλ��131? 53I��131? 53I�е�������Ϊ
A��53
B��78
C��131
D��184
�ο��𰸣�B
�������������ԭ�ӵ���ɼ���ʾ�������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮������������������������131��53��78����ѡB��
�����Ѷȣ�һ��