1��ѡ���� ������ˮ��ȡ������Դ�����������о�������ȷ���ǣ�?��
A������ˮ����������ǿ���ȼ�յ����ʣ���ˣ����о���ˮ���ֽ������£�ʹ���Ϊ������Դ
B���跨��̫����ۼ����������£�ʹˮ�ֽ��������
C��Ѱ�Ҹ�Ч������ʹˮ�ֽ����������ͬʱ�ͷ�����
D��Ѱ�����⻯ѧ���ʣ����ڿ���������Դ���Էֽ�ˮ��ȡ����
�ο��𰸣�BD
�����������
�����Ѷȣ���
2��ѡ���� ��0.05molNaOH�ֱ���뵽����100mL��Һ�У���Һ�ĵ��������仯�������
A������ˮ
B��0.5mol/L����
C��0.5mol/L����
D��0.5mol/L�Ȼ��
�ο��𰸣�BD
������������������仯����,˵������Һ���ڼ���NaOHǰ������Ũ���������仯��Aѡ��������ˮ�м���NaOH������Ũ�ȷ��������仯��Cѡ���д���Ϊ�������,��Ӧǰ����Ũ�Ƚ�С,����NaOH����CH3COOH+NaOH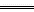 CH3COONa+H2O����ǿ�����CH3COONa,����Ũ����������A��C��ѡ��B��Dѡ����ԭ��Һ�б�������ǿ�����,����NaOH����Ȼ�����˻�ѧ��Ӧ,����Һ��Ȼ��ǿ����ʵ���Һ,�����ʵ�����ȣ�����Ũ�ȱ仯����,�ʷ������⡣
CH3COONa+H2O����ǿ�����CH3COONa,����Ũ����������A��C��ѡ��B��Dѡ����ԭ��Һ�б�������ǿ�����,����NaOH����Ȼ�����˻�ѧ��Ӧ,����Һ��Ȼ��ǿ����ʵ���Һ,�����ʵ�����ȣ�����Ũ�ȱ仯����,�ʷ������⡣
�����Ѷȣ�һ��
3��ѡ���� �����£���pH��13��NaOH��Һ��pH��2��HCl��Һ��1��9������Ȼ�ϣ�������Һ�������Ϊ������ӣ������û��Һ��pHֵ��
A��11
B��15
C��12
D��7.5
�ο��𰸣�A
���������
��ȷ�𰸣�A
C(OH�D)=(0.1mol/L��1L-0.01mol/L��9L)��10L=0.001mol/L,c(H��)=10-14 mol/L /0.001 mol/L =10-11mol/L;pH=-lg10-11=11
�����Ѷȣ�һ��
4��ѡ���� ijʵ��С��ѧ����50 mL 0.50 mol/L��������50 mL 0.55 mol/L ��NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų����������㷴Ӧ�ȣ�����˵����ȷ���ǣ�?��
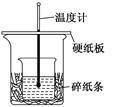
A����ͼ������ʵ�������û��������ʧ
B��������60 mL 0.50 mol/L�����50 mL 0.55 mol/L��NaOH��Һ���з�Ӧ����������˵����Ӧ�����
C��ͼ��ʵ��װ��ȱ�ٻ��β��������
D���ձ���������ֽ���������ǹ̶�С�ձ�
�ο��𰸣�C
�������������װ��ͼ��֪��С�ձ��ʹ��ձ��ı���û����ƽ��С�ձ�֮��Ҳû��������ĭ���ϣ����Բ�����û��������ʧ����Ӧ����μӷ�Ӧ�����ʵ����ʵ����й�ϵ�����Ըı������������Ӧ���Dz�ͬ�ģ������ȷ�Ĵ���C��
�����Ѷȣ�һ��
5������� ��4�֣��ִ������벻��������ҵ����������Ϊԭ�����������ֽ�һ����ij��������Ʒ����Ҫ�ɷ�Al2O3�����ڹ���ϡ���Ტ�Ƴ�500?mL��Һ��ȡ100?mL����Һ��������к� ��H+��Cl�D��Mg2����Al3����Fe3�� �������ӣ��������������ӣ�����֪�������ӵ����ʵ���Ũ��Ϊ��
c��H����?= 0.02?mol��L�D1? c��Mg2����= 0.01?mol��L�D1
c��Fe3����= 0.02?mol��L�D1?c��Cl�D��?= 0.52?mol��L�D1?
��1����Һ��Al3�� ���ʵ���Ũ��Ϊ?mol��L�D1
��2�������������Ʒ��Al2O3������Ϊ?g������ȷ��0.01 g��
�ο��𰸣���1��0.14mol��L�D1?��2��3.57g
�����������Һ�У����ӵ���������غ㣬������������ڸ������������0.52?mol��L�D1?��0.1L = ��0.02?mol��L�D1? + 0.01?mol��L�D1��2 + 0.02?mol��L�D1 ��3 + 3X����0.1L �����Al3�� ���ʵ���Ũ��X=0.14mol��L�D1?����������Ʒ����ϡ���ᣬ��Ҫ��ӦΪAl2O3 + 6HCl ="=" 2AlCl3 + 3H2O����Al2O3������Ϊm =" 102" g/mol��(0.14mol��L�D1��0.5L )/2 = 3.57g
���������⿼��ѧ���������غ�����⣬����Һ�ĵ���غ�����ʵ����غ㣬�ҵ����������غ㣬��ѧ����ʽ�ļ�����Եúܼ�
�����Ѷȣ�һ��