1��ѡ���� ��һ���¶��£��������ʵ�����CO��ˮ����ͨ�˺����ܱ������У��������·�Ӧ��CO(g)+H2O(g) 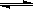 ?CO2(g)+H2(g)��һ��ʱ���Ӧ�ﵽƽ�⡣�Ը÷�Ӧ��������ȷ����
?CO2(g)+H2(g)��һ��ʱ���Ӧ�ﵽƽ�⡣�Ը÷�Ӧ��������ȷ����
A����ƽ��ʱCO�����ʵ����ﵽ��С
B���˼�CO2�� H2��Ũ���������
C��δ��ƽ��ǰ����Ӧ�������Ǵ����淴Ӧ����
D������CO������18O,���ƽ��ʱ��18Oֻ���ܴ�����CO��CO2��
�ο��𰸣�D
���������A��ȷ�����淴Ӧ�ﵽƽ�⼴Ϊ���淴Ӧ���ܴﵽ���ȣ������ת���ʣ���ƽ��ʱ��Ӧ���Ũ����С��B��ȷ�����ݻ�ѧ��Ӧ����ʽ��CO(g)��H2O(g)��1��1��ʽ��Ӧ������ʼ�������ҲΪ1��1������CO2�� H2��Ũ��������ȣ�C��ȷ��δƽ��ǰ����Ӧ����������Ӧ������У���ƽ��ǰ����Ӧ�������Ǵ����淴Ӧ���ʣ�D��������CO������18O,���ƽ��ʱ��18O���ܴ�����CO��CO2�к�H2O(g)�С�
�����Ѷȣ�һ��
2��ѡ���� ����ͼ��ʾ�������ݻ���ͬ�������٢ڢ��о��������·�Ӧ��
3A��g����B��g)  2C��g) ����H��0
2C��g) ����H��0
����˵����ȷ����

A������ʼ�¶���ͬ���ֱ������������г���3 mol A��1 mol B����ﵽƽ��ʱ��������C���ʵİٷֺ����ɴ�С��˳��Ϊ�ۣ��ڣ���
B����ά���¶Ȳ��䣬��ʼʱ����Ͷ��3 mol A��1 mol B������Ͷ��3 mol A,1 mol B��2molC����ﵽƽ��ʱ����������B��ת���ʢڣ���
C������ʼ�¶���ͬ���ֱ������������г���1 mol A��1 mol B����ﵽƽ��ʱ��������C���ʵİٷֺ���һ����ͬ
D������ʼ�¶���ͬ���ֱ������������г���3a mol A��a mol B����ﵽƽ��ʱ��������A���ʵ�ת����һ����ͬ
�ο��𰸣�A
�����������
�����Ѷȣ���
3��ѡ���� ��14�֣��Ҵ�����Ҫ�Ļ���ԭ�Ϻ�Һ��ȼ�ϣ�������һ������������CO2��H2��Ӧ�Ƶã�
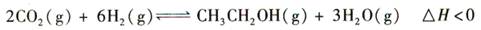
��ش�
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪ?��
��2�����¶�T1>T2ʱ����ѧƽ�ⳣ��K1?K2���>������<����=������
��3���ں��¡����ݵ��ܱ������У�����������˵��������Ӧ�Ѵﻯѧƽ��״̬����?������ĸ��ţ���
a������1molCH3CH2OH��ͬʱ����3 mol H2O
b�������и����Ũ�Ȳ���ʱ����仯
c�������л��������ܶȲ���ʱ����仯
d������������ķ�����������ʱ����仯
��4���ڹ�ҵ�����У���ʹH2��ת���ʺͻ�ѧ��Ӧ����ͬʱ��ߵĴ�ʩ��?��д��һ��������ʩ���ɣ���
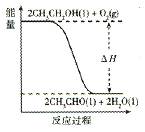
��5����ҵ�ϣ������Ҵ�Ϊԭ��������ȩ��������ͼ��ʾ��Ϣ���÷�Ӧ��?��Ӧ������ȡ������ȡ������ж�������__________________��
��6���Ҵ�������Ϊȼ�ϵ�ص�ȼ�ϡ�ij�Ҵ�ȼ�ϵ�����Ҵ�Ϊȼ�ϣ�ʹ�����Ե���ʣ��õ�ظ�����Ӧ�ĵ缫��ӦʽΪ?��
�ο��𰸣���1��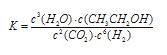
 ?��2��<?��3��b d?
?��2��<?��3��b d?
��4������CO2Ũ�ȣ�������ѹǿ��
��5������?��Ӧ������������������������
��6��CH3CH2OH �C 12 e- + 3H2O ��2CO2 + 12H+
�����������1�����ݻ�ѧƽ�ⳣ������ʽ����дԭ�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ���𰸣���2���÷�Ӧ����Ӧ�Ƿ��ȷ�Ӧ�������¶�ƽ�����淴Ӧ�ƶ���ƽ�ⳣ����С�����¶�Խ�ߣ�ƽ�ⳣ��ԽС���¶�T1��T2��K1��K2����3��a���������淴Ӧ���������Ϊƽ���־��ע�⡰˫��ͬʱ�����ϱ�����������1mol?CH3CH2OH��ͬʱ������3mol?H2O������ʾ����Ӧ���ʣ�����˵������ƽ�⣬����b�����淴Ӧ����ƽ��ʱ������ֵ����ʵ������䣬��ϵ�и���ݵ����ʵ���Ũ�Ȳ���ʱ����仯��˵������ƽ�⣬��ȷ��c����Ӧ�����������������䣬������������䣬�ܶ�ʼ�ղ��䣬��ϵ�л��������ܶȲ���ʱ����仯������˵������ƽ�⣬����d���淴Ӧ���л�������ܵ����ʵ�����С����ϵ������ķ����������٣���ϵ�����������������ʱ����仯��˵������ƽ�⣬��ȷ��ѡbd����4���ı������ӿ췴Ӧ���ʣ�ͬʱƽ��������Ӧ�ƶ�����������CO2Ũ�Ȼ�����ѹǿ����Ӧ���ʼӿ죬ƽ��������Ӧ�ƶ�������ת��������5����ͼ���֪����Ӧ�����������������������������ʸ÷�Ӧ��Ϊ���ȷ�Ӧ����6��ȼ�ϵ�ظ�����Ӧ������Ӧ���Ҵ��ڸ����ŵ磬�������������ɶ�����̼�������ӣ��缫��ӦʽΪ��CH3CH2OH-12?e-+3H2O=2CO2+12H+��
�����Ѷȣ�һ��
4��ѡ���� ��1 L�ܱ������У���1 mol A��1 mol B��Ϸ������·�Ӧ��3A(g)+B(g) 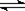 xC(g)+2D(g)������Ӧ�ﵽƽ��ʱ������0.4 mol D�������C��ƽ��Ũ��Ϊ0.4 mol/L�����������в���ȷ����
xC(g)+2D(g)������Ӧ�ﵽƽ��ʱ������0.4 mol D�������C��ƽ��Ũ��Ϊ0.4 mol/L�����������в���ȷ����
A��x��ֵΪ2
B��A��ת����Ϊ40%
C��B��ƽ��Ũ��Ϊ0.8 mol/L
D��D���������Ϊ20%
�ο��𰸣�B
�������������ʽ3A(g)? +? B(g) 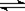 xC(g)? +? 2D(g)
xC(g)? +? 2D(g)
��ʼ���ʵ���? 1 mol? 1 mol? 0? 0
�仯���ʵ���? 0.6 mol? 0.2 mol? 0.2x mol? 0.4 mol
ƽ�����ʵ���? 0.4 mol? 0.8 mol? 0.2x mol? 0.4 mol
���Կɵ�A��ȷ��x=2��B����A��ת����Ϊ60%��C��ȷB��ƽ��Ũ��Ϊ0.8 mol/L��D��ȷD���������Ϊ20%��
�����Ѷȣ�һ��
5��ѡ���� ��Ӧ4A(g)��5B(g)==4C(g)��6D(g)����5L���ܱ������н��У�����Ӻ�C�����ʵ���������0��30mol������������ȷ����?
[? ]
A��A��ƽ����Ӧ������0��010 mol��L-1��s-1?
B�������к�D���ʵ�������Ϊ0��45 mol?
C��������A��B��C��D�����ʵ����ı�һ����4��5��4��6
D��������A�����ʵ���һ��������0��30mol
�ο��𰸣�B
���������
�����Ѷȣ���