1、填空题 (8分)已知由短周期元素组成的A、B、C、D四种常见化合物分子中所含原子数目依次为2、3、4、5,其中A、B含有18个电子,C、D含有10个电子。请回答:
(1)D中含有的化学键类型有?,已知8gD与O2完全燃烧,生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式?。
(2)室温下,若向一定量C的稀溶液中逐滴加入物质的量浓度相同的A,直至A过量,生成化合物XY4Z(X 、Y、Z表示元素符号)。讨论上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白(要求填写有关粒子化学式):
、Y、Z表示元素符号)。讨论上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH。试填写表中空白(要求填写有关粒子化学式):
?
| 离子浓度由大到小的顺序
| 溶质的化学式
| 溶液的pH
|
I
| c(XY+4)>c(Z―)>c(OH―)>c(H+)
| ?
| pH>7
|
II
| c(XY+4)=c(Z―)
| XY4Z、XY3・H2O
| ?
|
III
| ?
| XY4Z
| pH<7
|
IV
| c(Z―)>c(H+)>c(XY+4)> >c(OH―)
| ?
| pH<7
|
(3)B在空气中完全燃烧生成E,在一定条件下发生E与O2反应生成F。
①将0.05molE和0.03molO2放入容积为1L的密闭容器中,达到平衡,测得c(F)=0.04mol・L―1。计算该条件下反应的平衡常数K=?和E的平衡转化率?。
②已知上述反应是放热反应,当该反应处于平衡状态时,下列措施中有利于提高E平衡转化率的有?(填字母)。
A.升高温度? B.降低温度? C.增大压强? D.减小压强
2、选择题 一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO2 2NO+O2,达到平衡的标志是
2NO+O2,达到平衡的标志是
①相同时间内,氧气的生成速率为n mol・L-1・s-1,NO2的生成速率为2n mol・L-1・s-1
②单位时间内生成n mol O2的同时生成2n mol的NO
③混合气体的颜色不再变化 ?④混合气体的密度保持不变
⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化
A.①③⑤⑥
B.②③⑤
C.①③④
D.①②③④⑤⑥
3、选择题 在10 L密闭容器中,1 mol A和3 mol B在一定条件下反应:A(气)+xB(气) 2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是
2C(气),2min后反应达到平衡时,测得混合气体共3.4 mol,生成0.4 mol C,则下列计算结果不正确的是
[? ]
A.平衡时,物质的量比A∶B∶C=2∶11∶4
B.x值等于4
C.A的转化率20%
D.B的平均反应速率为0.04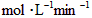
4、填空题 将2?mol?I2(g)和1?mol?H2置于某2?L密闭容器中,在一定温度下发生反应:I2(g)+H2(g) 2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示.
2HI(g) ΔH<0,并达平衡,HI的体积分数φ(HI)随时间变化如下图中曲线(Ⅱ)所示.
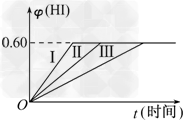
(1)达平衡时,I2(g)的物质的量浓度为________.
(2)若保持温度不变,在另一相同的2?L密闭容器中加入a?mol?I2(g)、b?mol?H2和c?mol?HI(a、b、c均大于0),发生反应,达平衡时,HI的体积分数仍为0.60,则a、b、c的关系是________.
5、选择题 在一定条件下,体积不变的密闭容器中,反应H2(g)+I2(g) 2HI(g)一定处于化学平衡状态的是?
2HI(g)一定处于化学平衡状态的是?
A.单位时间内有1mol H2消耗,同时有1mol I2生成
B.容器内的压强保持不变
C.H2(g)、I2(g)、HI(g)的浓度相等
D.单位时间内有1mol I-I键断裂同时有2mol H-I键形成