1、选择题 6.4 g铜与过量的硝酸(8 mol・L-1 60 mL)充分反应后,硝酸的还原产物有NO、NO2,反应后溶液中含H+为n mol,此时溶液中含 的物质的量为(? )
的物质的量为(? )
A.0.28 mol
B.0.31 mol
C.(n+0.2) mol
D.(n+0.4) mol
参考答案:C
本题解析:反应后溶液中的溶质为Cu(NO3)2和HNO3,所以n( )=2×n(Cu2+)+n(H+)=2×
)=2×n(Cu2+)+n(H+)=2×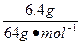 +n mol="(0.2+n)" mol。
+n mol="(0.2+n)" mol。
本题难度:简单
2、选择题

A.H2和O2
B.HCl和NH3
C.H2和Cl2
D.CO和O2
参考答案:A
本题解析:此题考查了化学反应中各反应物的计量数之间的关系及相同条件下气体的压强与气体的物质的量的关系。等物质的量的H2和O2反应,剩余0.05 mol O2,压强变为原来的1/4;HCl和NH3恰好完全反应生成固体NH4Cl,压强为0;H2与Cl2反应后物质的量不变,压强不变;CO与O2反应生成气态的CO2,压强变为原来的3/4。
本题难度:简单
3、填空题 硝酸是极其重要的化工原料,工业上将产生的NO2在密闭容器中用水多次反复循环吸收制备硝酸。
(1)工业上用水吸收NO2生产HNO3,生成的气体经多次氧化、吸收的循环操作充分转化为硝酸(假定上述过程无其他损失)。试写出上述反应的化学方程式:
______________________________________________________________。
(2)为了证明NO也可以与氧气和水共同反应生成HNO3,某学生设计了如图所示装置(有关夹持装置已略去)。
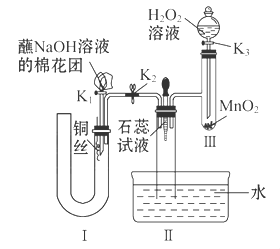
①检查装置气密性良好后,为观察到NO气体生成,打开K1,关闭K2,应从U形管的长管口注入稀硝酸至 后,迅速关闭K1,观察到U形管内的现象是____________________________________________________。
②装置Ⅲ中发生反应的化学方程式为_______________________________。
③蘸NaOH溶液的棉花团的作用是___________________________________。
④打开K2,至装置Ⅱ中长玻璃管中的气体呈无色后,打开K3,反应一段时间后,长玻璃管中并未充满液体。设计简单方法检验长玻璃管中的气体是否含NO__________________________________________________。
参考答案:(1)4NO2+O2+2H2O=4HNO3(或分成两个方程式写)
(2)①U形管右侧胶塞下沿 U形管左端液面高于右端,铜丝慢慢溶解,产生无色气体,溶液逐渐变蓝(至少答三点) ②2H2O2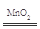 2H2O+O2↑
2H2O+O2↑
③吸收氮的氧化物防止污染环境
④再打开K3,若观察到长玻璃管中气体迅速变为红棕色,则证明余气含NO,若无颜色变化,则证明不含NO(其他合理答案也可)
本题解析:根据实验目的和所放置的试剂可以推断,Ⅰ装置的作用是制备NO,Ⅲ装置的作用是制备O2,Ⅱ装置的作用是证明NO也可以与氧气和水共同作用生成HNO3。
(1)NO2经多次氧化、用水吸收的循环操作,充分转化为硝酸的化学方程式为4NO2+O2+2H2O=4HNO3。
(2)①注入稀硝酸应至U形管右侧胶塞下沿,迅速关闭K1后,U形管左端液面高于右端,铜丝慢慢溶解,产生无色气体,溶液逐渐变蓝。
②装置Ⅲ中发生反应的化学方程式为:2H2O2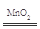 2H2O+O2↑。
2H2O+O2↑。
③蘸NaOH溶液的棉花团的作用是吸收氮的氧化物,防止污染环境。
④再打开K3,若观察到长玻璃管中气体迅速变为红棕色,则证明余气含NO,若无颜色变化,则证明不含NO。
本题难度:一般
4、实验题 (10分)碘在工农业生产和日常生活中有重要用途。
(1)右图为海带制碘的流程图。
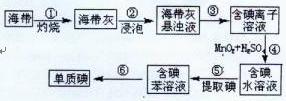
步骤③和⑤的实验操作名称分别是?、?;
步骤④中发生反应的离子方程式为?;
若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液中并振荡,观察到的现象是?。
(2)把滤纸用淀粉和碘化钾溶液浸泡,晾干后就是实验室常用的淀粉碘化钾试纸。利用淀粉碘化钾试纸可检验具有某种特性的气体。你认为淀粉碘化钾试纸用于检验具有?的气体(填序号)
A.酸性
B.碱性
C.氧化性
D.还原性