|
|
|
高考化学知识点总结《盐类水解的原理》高频试题巩固(2017年最新版)(七)
2018-03-17 06:44:13
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
1、选择题 现有常温下的四份溶液:① 0.01mol/LCH3COOH;② 0.01mol/LHCl;③ pH=12的氨水;④ pH=12的NaOH溶液。下列说法正确的是
A.①中水的电离程度最小,②③④中水的电离程度一样大
B.将②③混合,若pH=7,则消耗溶液的体积:②<③
C.将①、④混合,若有c(CH3COO¯)>c(H+),则混合液一定呈碱性
D.将①、④等体积混合,所得溶液中一定有:c(OH¯)=c(H+) + c(CH3COOH)
|
2、填空题 (14分)某温度下,水的离子积Kw=l×10-13。有酸溶液A,pH=a;碱溶液B,pH=b。为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置。
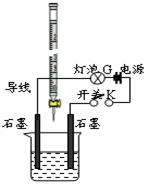
(1)实验时,烧杯中应盛 (选A或B)溶液。
(2)若A为一元强酸,B为一元强碱,且a+b=13。该同学在烧杯中先加入其中一种溶液,闭合开关K,测得烧杯中灯泡的亮度为10(假设亮度由暗到亮表示为1、2、3、…10、11、12、… 20)。断开开关K,将滴定管中的溶液逐滴加入到烧杯中。当从滴定管滴入烧杯中的溶液体积和烧杯中盛有的溶液体积相等时,停止滴加溶液并闭合开关K,此时灯泡G的亮度约为 ,原因是 。烧杯中得到的溶液pH= 。
(3)若A为强酸,B为强碱,且a+b=13。断开开关K,将滴定管中的溶液逐滴加入到烧杯中。当测得烧杯中溶液pH和“⑵”中最后得到的溶液pH相同时,停止滴加溶液。此时烧杯中的溶液中阳 离子浓度大于阴离子浓度,原因可能是 。
(4)若A的化学式为HR,B的化学式为MOH,且a+b=13,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为_ _。
此时烧杯中的混合溶液中,微粒浓度大小关系一定正确的是_ _____(填序号)。
①c(MOH)>c(M+)>C(R-)>c(H+)>c(OH-)
②c(HR)>c(M+)>c(R-)>c(OH-)>c(H+)
③c(R-)>c(M+)>c(H+)>c(OH-)
④c(M+)>c(R-)>c(OH-)>c(H+)
⑤c(M+)+ c(H+)=c(R-)+c(OH-)
⑥c(MOH)=c(H+)-c(OH-)
3、选择题 把0.2mol/L NH4Cl溶液与0.1mol/L NaOH溶液等体积混合后溶液中下列微粒的物质的量浓度的关系正确的是
A.[NH4+]=[Na+]=[OH-]>[NH3・H2O]
B.[NH4+]=[Na+]>[NH3・H2O]>[OH-]
C.[NH4+]>[Na+]>[OH-]>[NH3・H2O]
D.[NH4+]>[Na+]>[NH3・H2O]>[OH-]
4、选择题 NH4Cl稀溶液中分别加入少量下列物质或改变如下条件,能使比值c(NH4+)/c(Cl―)一定增大的是
①HCl气体 ②氨气 ③H2O ④NH4Cl固体 ⑤NaOH固体 ⑥降温
A.③④⑤
B.②④
C.②③⑥
D.②④⑥
|
5、选择题 下列物质的溶液在蒸发皿中加热蒸干并灼烧,最后得到该物质固体的是
A.氯化铝
B.硫酸镁
C.亚硫酸钠
D.碳酸氢钠