1、选择题 在下列溶液中,各组离子一定能够大量共存的是(?)
A.能使广泛pH试纸显蓝色的溶液:K+、Ba2+、Cl-、Br-
B.常温下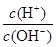 =1012的溶液:Fe2+、Mg2+、NO3-、Cl-
=1012的溶液:Fe2+、Mg2+、NO3-、Cl-
C.含有大量Al3+的溶液:Na+、Cl-、AlO2-、OH-
D.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO42-、S2-、SO32-
参考答案:A
本题解析:A项使pH试纸显蓝色是碱性溶液,离子可以大量共存;B项是pH=1的溶液,Fe2+被NO3-氧化;C项Al3+与AlO2-不能大量共存;D项是氧化性溶液,S2-、SO32-不能大量存在。
本题难度:一般
2、选择题 在下列各组离子中,能大量共存的是
[? ]
A.Ag+、NO3-、Na+、Cl-
B.K+、OH-、Cl-、Al3+
C.NO3-、Fe2+、OH-、Br-
D.K+、NH4+、Cl-、SO42-
参考答案:D
本题解析:
本题难度:一般
3、选择题 对于电解质溶液,下列说法正确的是
A.甲基橙显黄色的溶液中,不可能有: Mg2+、K+、SO42- 、NO3-
B.无色溶液中还大量含有 :Al3+、 K+、 SO32- 、ClO-
C.Fe(OH)3溶于氢碘酸发生的反应为:Fe(OH)3+3H+= Fe3++3H2O
D.在稀氨水中通入过量CO2发生的反应为:NH3・H2O+CO2= NH4++HCO3-
参考答案:D
本题解析:A.甲基橙的变色范围是PH值0~3.1~4.4~14,颜色分别为红、橙、黄,所以黄色时也可以是酸性条件,该离子组可能共存,错误;B. SO32- 与ClO-因为氧化还原反应而不能共存,、Al3+与ClO-发生双水解而不能共存,错误;C.应是2Fe(OH)3+6H+ + 2I-=2Fe2++6H2O + I2,错误;D.注意NH3・H2O是弱碱,正确。3与HI的性质。
本题难度:一般
4、选择题 下列离子或分子在无色溶液中能大量共存的一组是( )
A.Fe2+、OH-、Cl2
B.Ag+、Cl-、SO42-
C.Na+、SO42-、NO3-
D.Al3+、NO3-、NH3?H2O
参考答案:A.Fe2+、Cl2与OH-反应而不能大量共存,且Fe2+、Cl2有颜色,故A错误;
B.Ag+与Cl-反应生成AgCl沉淀而不能大量共存,故B错误;
C.溶液无色,且离子之间不发生任何反应,可大量共存,故C正确;
D.Al3+与NH3?H2O反应生成沉淀而不能大量共存,故D错误.
故选C.
本题解析:
本题难度:一般
5、填空题 某无色透明溶液,跟金属铝反应生成H2,试判断下列离子:Mg2+、Cu2+、Ba2+、H+、Ag+、SO42-、SO32-、HCO3-、、OH-、NO3-,哪些可能是构成此溶液的成分?
(1)生成Al3+时,可能存在______.
(2)当生成AlO2-时,可能存在______.
参考答案:无色透明溶液,说明原溶液中不存在Cu2+;铝具有两性,既能与酸作用产生氢气,也能与碱作用产生氢气,
(1)当与酸作用时,溶液显酸性,则SO32-、HCO3-、、OH-不存在,由于硝酸与金属反应一般没有氢气产生,
因此也不存在NO3-,
根据溶液不显电性,一定存在阴离子,即溶液中肯定有SO42-,而Ag+、Ba2+可与SO42-生成沉淀,
说明原溶液中也不存在Ag+、Ba2+,
即此时溶液中可能存在H+、SO42-、Mg2+等离子,故答案为:H+、SO42-、Mg2+;
(2)当溶液显碱性时,Mg2+、Cu2+、H+、Ag+、HCO3-不能存在,根据溶液不显电性,一定存在阳离子,
即阳离子只有Ba2+,
说明原溶液中的阴离子只能是OH-、NO3-,则原溶液中存在的离子可能是:OH-、Ba2+、NO3-,故答案为:OH-、Ba2+、NO3-.
本题解析:
本题难度:一般