1������� Ϊ��ȥ�����е�Ca2+��Mg2+��SO
�Լ���ɳ�����ʣ�ijͬѧ�����һ���Ʊ����ε�ʵ�鷽�����������£����ڳ������Լ��Թ�������
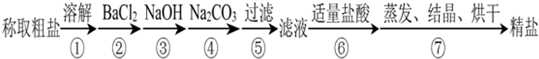
��1���ڵڢٲ��͵ڢݲ��ж���Ҫ�õ��������������÷ֱ���______��______��
��2���ж�BaCl2�ѹ����ķ�����______��
��3���ڢܲ��У���ص����ӷ���ʽ��______��
��4�������������ٹ��ˣ�����ʵ��������Ӱ�죬��ԭ����______��
2��ѡ���� �������ӷ���ʽ�У���ȷ����
A��H2SO4��Һ��Ba(OH)2��Һ��ϣ� Ba2+ + OH- + H+ + SO42��="=" BaSO4��+ H2O
B�����ۼ��뵽NaOH��Һ�У�2Al + 2OH-+ 2H2O == 2AlO2-+ 3H2��
C��ʵ������ʯ��ʯ�ƶ�����̼���壺CO32- + 2H+== CO2��+ H2O
D���ƿ�Ͷ�뵽CuSO4��Һ�У�2Na+Cu2+==2Na++Cu
3��ѡ���� �������ӷ���ʽ����ȷ����
[? ]
A��������Һ�м���Na2CO3��C6H5OH+CO32-��C6H5O-+HCO3-
B����Ba(OH)2��Һ����μ���NH4HSO4��Һ���պó�����ȫ��Ba2++OH-+H++SO42-��BaSO4��+H2O
C����Ba(OH)2��Һ�м������NaHSO3��Һ��2HSO3-+Ba2++2OH-��BaSO3��+SO32-+2H2O
D���״�-����ȼ�ϵ�أ�KOH��Һ���������Һ�������ĵ缫��Ӧʽ��CH3OH-6e-+8OH-��CO32-+6H2O
4��ѡ���� ���з�Ӧ�����ӷ���ʽ����ȷ���ǣ�������
A��ƫ��������Һ�м���������H++AlO2-+H2O�TAl��OH��3��
B������ϡ���ᷴӦ��2Fe+6H+=2Fe3++3H2��
C�����Ȼ�����Һ�м�������İ�ˮ��Al3++3NH3?H2O=Al��OH��3��+3NH4+
D��ͭƬ������������Һ�У�Cu+Ag+�TCu2++Ag
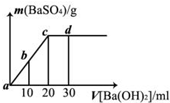
5��ѡ���� �����£���0.1mol?L-1��������Һ����μ������ʵ���Ũ����ͬ������������Һ�����ɳ����������������������Һ�������ϵ��ͼ��ʾ��a��b��c��d�ֱ��ʾʵ��ʱ��ͬ�ε���Һ�������й�˵������ȷ���ǣ�������
A����Һ�ĵ���������a��b��d��c
B����Һ��pH��a��b��c��d
C��a��Һ��b��Һ�ʼ���
D��d������������c���Ĵ�