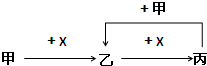
1������� ����X��Y��Z���ֳ���������Ԫ�أ�x��ԭ�ӽṹʾ��ͼ��ͼ��Y��zΪͬ���ڽ���Ԫ�أ�Y��Z������������Ӧˮ������Է�Ӧ�����κ�ˮ���ش��������⣺
��1����֪Y2?X2Ϊdz��ɫ�������ʣ����������Ӹ�����Ϊ______�����к��еĻ�ѧ��������______��
��2��������Z�ı�Ƭ�ھƾ����ϼ������ۻ����۲쵽������______�������������ԭ����______��
��3��Y��Z����������Ӧ��ˮ�����Ϸ�Ӧ�����κ�ˮ�����ӷ���ʽΪ______��
��4������3���������ﻹ�ɱ�ʾΪYZ��OH��4����YZ��OH��4�����HC1��Һ��Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�X��Y��Z���ֳ���������Ԫ�أ�����X��ԭ�ӽṹʾ��ͼ��֪a=2����XΪOԪ�أ���ϣ�1��Y2?X2Ϊdz��ɫ�������ʣ���֪YΪNaԪ�أ�Y��ZΪͬ���ڽ���Ԫ�أ����ߵ�����������Ӧˮ������Է�Ӧ�����κ�ˮ��Ϊ��������������������Ӧ����ZΪAlԪ�أ�
��1��Na2O2������������������ӹ��ɵ����ӻ�������������Ӹ�����Ϊ1��2��������������������֮���γ����Ӽ�����������������ԭ��֮���γɷǼ��Լ����ʴ�Ϊ��1��2�����Ӽ����Ǽ��Լ���
��2��������Al�ı�Ƭ�ھƾ����ϼ������ۻ������ڷ�Ӧ���������������������۵�����ߣ�������Ĥ��ס�����ڻ��ɵ�С�����£��ʴ�Ϊ���ڻ��ɵ�С�����£����������۵�����ߣ�
��3����������������������Ӧ����ƫ��������ˮ����Ӧ���ӷ���ʽΪ��Al��OH��3+OH-=AlO2-+2H2O���ʴ�Ϊ��Al��OH��3+OH-=AlO2-+2H2O��
��4��NaAl��OH��4�����HC1��Һ��Ӧ�����Ȼ������Ȼ�����ˮ����Ӧ���ӷ���ʽΪ��Al��OH��4-+4H+=Al3++4H2O���ʴ�Ϊ��Al��OH��4-+4H+=Al3++4H2O��
���������
�����Ѷȣ�һ��
2������� A��B��CΪ��ѧ�������ʣ�����һ��Ϊ������ͨ������£�AΪ���壬BΪҺ�壬CΪ���壮D��E��F��G��H��X��Y��Ϊ���������X��һ������ǿ�ᡢEΪ��ɫ���壬H�ڳ�����ΪҺ�壮����֮���ת����ϵ��ͼ��ʾ������ijЩ��Ӧ�����Ͳ��ַ�Ӧ������ȥ����
��1����Ӧ�ٵĻ�����Ӧ������______��
��2��E���׳���______��
��3��д��X�ĵ���ʽ______��
��4��Y��Һ�����ԣ���һ�㲻�������ָʾ�����飮��Y��Һ��������B��Ũ��Һ���а�ɫ�������ɣ�������D��Һ���Ϊ��ɫ��д��Y�Ľṹ��ʽ______��
��5����Ӧ�ߵĻ�ѧ����ʽΪ______���÷�Ӧ��ÿ����?3mol��A����ת�Ƶ���______?mol��
��6������D��Һ����D������Һ�Ʊ��Ľ��������������______��
�ο��𰸣���1����Ӧ�����嵥�ʺ��������ķ�Ӧ��2Fe+3Br2=2FeBr3����Ӧ����Ϊ���Ϸ�Ӧ���ʴ�Ϊ�����Ϸ�Ӧ��
��2�������ƶϣ�EΪ�������������׳ƴ������������ʴ�Ϊ��������������
��3�������ƶ�XΪHBr�����ӵĵ���ʽΪ��
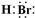
���ʴ�Ϊ��
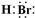
��
��4����Y��Һ�����ԣ���һ�㲻�������ָʾ�����飮��Y��Һ��������B��Br2����Ũ��Һ���а�ɫ�������ɣ�������D��FeBr3����Һ���Ϊ��ɫ֤��YΪ���ӣ��ṹ��ʽΪ��

���ʴ�Ϊ��

��
��5����Ӧ��������ˮ�����з����ķ�Ӧ������������������������Ӧ�Ļ�ѧ����ʽΪ��3Fe+4H2O��g��?����?.??Fe3O4+4H2���÷�Ӧ�з���������ԭ��Ӧ�ĵ����غ㣬��Ԫ�ػ��ϼ۴�+1�۱仯Ϊ0�ۣ�4H2O��Ӧת�Ƶ���Ϊ 8mol����Ԫ�ش�0�۱仯Ϊ+38�ۣ�ÿ���� 3mol��A��Fe������ת�Ƶ���8mol��
�ʴ�Ϊ��3Fe+4H2O��g��?����?.? Fe3O4+4H2��8��
��6��DΪFeBr3�����ȱ�����Һ�����Ʊ���������������������Һ�ͽ���ķ����ö����ЧӦ���𣬹ʴ�Ϊ�������ЧӦ��
���������
�����Ѷȣ�һ��
3������� �ɶ�����Ԫ����ɵ�����A-K������֮�������ͼ��ת����ϵ����ͼ�з�Ӧ������ʡ�ԣ���֪��A�dz���������B�dz����ǽ������ʣ�����Ϊ���壬����ɫ���ʺ�ɫ����ɫ��E��FΪ�������壬���ʱ��ȼ������ը��
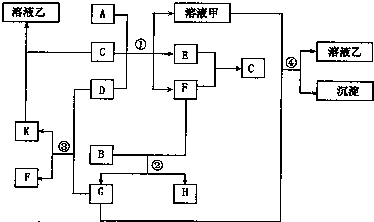
��1��д������������A��ԭ�ӽṹʾ��ͼ��______��D�ĵ���ʽ��______��K��������______��
��2��д����Ӧ�ٸ�����ǡ����ȫ��Ӧ�Ļ�ѧ����ʽ��______��
��3����Ӧ���У���B��F�����ʵ���֮��Ϊ4��3ǡ����ȫ��Ӧ�������������ʵ���֮��n��G����n��H��______��
�ο��𰸣�B�dz����ǽ������ʣ�����Ϊ���壬����ɫ���ʺ�ɫ����ɫ��E��FΪ�������壬���ʱ��ȼ������ը��ӦΪO2��H2�ķ�Ӧ����CΪH2O��A�dz�������������һ�ֹ�����ˮ�з�Ӧ����O2��H2����ù������ΪAl������DΪNa2O2������ˮ��CO2��Ӧ����GΪCO2��������K������ˮ��˵��KΪNa2CO3��FΪO2�� �����Ϣ��ɫ����B��������F����Ӧ�õ�G��CO2����˵��BΪC��̼����C��������Ӧ������CO2��CO����HΪCO������F��O2����E��Ӧ����C��ˮ����֪EΪ������
��AΪAl��BΪC��CΪH2O��DΪNa2O2��EΪH2��FΪO2��GΪCO2��HΪCO��KΪNa2CO3��
��1��AΪAl��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ3��ԭ�ӽṹʾ��ͼΪ
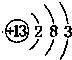
��DΪNa2O2��Ϊ���ӻ��������ʽΪ
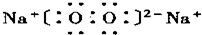
��KΪNa2CO3���׳ƴ��
�ʴ�Ϊ��
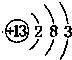
��
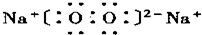
�����
��2����Ӧ��ΪAl��Na2O2��ˮ�ķ�Ӧ����ǡ����ȫ��Ӧʽ������NaAlO2��
��Ӧ�ķ���ʽΪ2Na2O2+4Al+6H2O�T4NaAlO2+6H2��+O2��
�ʴ�Ϊ��2Na2O2+4Al+6H2O�T4NaAlO2+6H2��+O2��
��3��BΪC��FΪO2�������ʵ���֮��Ϊ4��3ǡ����ȫ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ��4C+3O2?��ȼ?.?2CO2+2CO�����������ʵ���֮��n��G����n��H��=1��1��
�ʴ�Ϊ��1��1��
���������
�����Ѷȣ�һ��
4������� ��15�֣�����A��E��F����ɫ��Ӧ�ʻ�ɫ������I��1��������4��ԭ����ɲ�������10�����ӣ�B��C��D��K�ڳ����¶������嵥�ʣ�G�ڳ���������ɫҺ�壬��Ӧ�١��ݶ������ڹ�ҵ�����ķ�Ӧ�����й�����֮������Ӧת����ϵ����ͼ��ʾ�����ַ�Ӧ��������ȥ����
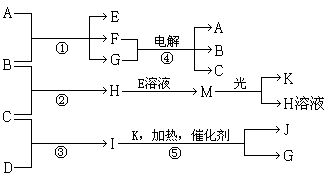
��1��д�����ʵĻ�ѧʽ��B?M?
��2��д��A���ʵĵ���ʽ?����I��?���ӣ���Ի�Ǽ��ԣ�
��3��0��1mol/LEˮ��Һ�и�����Ũ���ɴ�С��˳��Ϊ?
��4����Ӧ�ٵ����ӷ���ʽ?
��Ӧ�ݵĻ�ѧ����ʽ?
��5����Ӧ���У���ת��0��02mol���Ӻ�ֹͣ��Ӧ����Һ�������200mL�����ʱ��Һ�������ǵ���������Ӧ����PH=_________��
�ο��𰸣���1��B��Cl2? M��HClO
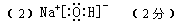 ?����? (ע�⣺�˿�1�֣�����ÿ��2��)
?����? (ע�⣺�˿�1�֣�����ÿ��2��)
��3��c��Na+����c��ClO-����c��OH-����c��H+��
��4��Cl2+2OH-=Cl-+ClO-+H2O

��5��13
�������������I��1��������4��ԭ����ɲ�������10�����ӣ�����I�ǰ�������C��������D�ǵ�����G�ڳ���������ɫҺ�壬���G��ˮ����K��������J��NO��A��E��F����ɫ��Ӧ�ʻ�ɫ������A���������ƣ�B��������E�Ǵ������ƣ�F���Ȼ��ƣ�H���Ȼ��⣬M�Ǵ����ᡣ
��1����
��2�����������Ǻ������Ӽ��ͼ��Լ������ӻ��������ʽΪ �������������Σ������Ǽ��Է��ӡ�
�������������Σ������Ǽ��Է��ӡ�
��3������������ǿ�������Σ�ˮ���Լ��ԣ���������Ũ�ȴ�С˳����c��Na+����c��ClO-����c��OH-����c��H+����
��4������
��5�����Ե缫���ʳ��ˮ�ķ���ʽΪ2NaCl��2H2O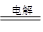 2NaOH��Cl2����H2����ת��0��02mol����ʱ��������������0.02mol����Ũ����0.1mol/L������pH��13��
2NaOH��Cl2����H2����ת��0��02mol����ʱ��������������0.02mol����Ũ����0.1mol/L������pH��13��
�����Ѷȣ�һ��
5��ѡ���� ��֪�ס��ҡ�����X��������ѧ��ѧ�г��������ʣ���ת����ϵ��ͼ��ʾ�����X�������ǣ�������
A����ΪC��XΪO2
B����ΪSO2��XΪNaOH��Һ
C����ΪFe��XΪCl2
D����ΪAlCl3��XΪNaOH��Һ