1������� ����ѧ�뼼����
��Ƴ���ͭ��ˮ�к���CN-��Cr2O72-���ӣ���Ҫ������������ŷš��ó��ⶨ�������̽��з�ˮ�������ش��������⣺
 ?
?
��1������������ˮ��������Ҫʹ�õķ�����______��
��2�����з�Ӧ��������ų����÷�Ӧ�����ӷ���ʽΪ?��
��3��������У�ÿ����0.4mol Cr2O72-ʱת�Ƶ���2.4mol���÷�Ӧ���ӷ���ʽΪ?��
��4��ȡ��������ˮ�����Թ��У�����NaOH��Һ���۲쵽����ɫ�������ɣ��ټ�Na2S��Һ����ɫ����ת���ɺ�ɫ��������ʹ�û�ѧ��������ֽ��Ͳ����������ԭ��?��
��5��Ŀǰ��������Cr2O72-��ˮ������������巨���÷������ˮ�м���FeSO4��7H2O��Cr2O72-��ԭ��Cr3+������pH��Fe��Crת�����൱��FeII[FeCr]O4���������壬�������ֱ�ʾԪ�ؼ�̬���ij���������1mol Cr2O72-�������a mol FeSO4?7H2O�����н�����ȷ����_______��
A��x ="0.5" ��a =8
B��x =0.5��a = 10
C��x =" 1.5" ��a =8
D��x =" 1.5" ��a = 10
�ο��𰸣���1��������ԭ��
��2��CN-+ClO-=CNO-+Cl-
��3��3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O
��4��Cu2++2OH-=Cu(OH)2��? Cu(OH)2(s)+S2-(aq)=CuS(s)+2OH-(aq)
����KSP(CuS)<KSP[Cu(OH)2]?
��5��D
�����������1����ͼ��֪������ˮ�е�����ʵ������ת��ʱ��������������ԭ��Ӧ������Ҫʹ�õķ���Ϊ������ԭ����
��2�����������£�CN-������NaClO����������ԭ��Ӧ��������ų���������CNO-��Cl-���ӣ����ӷ�ӦΪCN-+ClO-�TCNO-+Cl-��
��3��ÿ0.4molCr2O72-ת��2.4mol�ĵ��ӣ��軹ԭ��CrԪ�صĻ��ϼ�Ϊx����0.4mol��2��(6-x)=2.4mol�����x=+3�������ӷ�ӦΪ��
3S2O32-+4Cr2O72-+26H+�T6SO42-+8Cr3++13H2O��
��4����ͭ���������������ӷ�Ӧ����������ͭ������CuS��Cu��OH��2�����ܣ������Na2S��Һ�ܷ���������ת�����ʴ�Ϊ������ˮ���л���Cu2+���Ӽ��Cu2++2OH-�TCu(OH)2�����ټ���Na2S��Һ��CuS��Cu(OH)2�����ܣ�����Cu(OH)2��s��+S2-��aq���TCuS��s��+2OH-��aq����
��5��������������ymol��������CrԪ�������䣬���У�2-x��y=2��FeԪ�ز��䣬���У�1-x��y=a����ʧȥ�ĵ������ʵ�������Cr�õ��ĵ��ӵ����ʵ�����ȣ���x=1.5��y=4��a=10����ѡD��
�����Ѷȣ�һ��
2������� ��ѧѧ���еĻ�ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ���������������ԭ����
��ش��������⣺
 ��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��
��1����ҵ�ϲ�ȡCO��H2Ϊԭ�Ϻϳ��Ҵ����仯ѧ��Ӧ����ʽΪ��2CO��g����4H2��g��
�ο��𰸣�
���������
�����Ѷȣ�����
3��ѡ���� ����˵����ȷ����?��������
A������ƽ�ⳣ������ҺŨ�ȵ�Ӱ��
B�����볣���������Һ��c(H��)һ���ȵ��볣��С������Һ�еĴ�
C������ƽ�ⳣ�����Ա�ʾ������ʵ����ǿ��
D��H2CO3�ĵ��볣������ʽ��K��
�ο��𰸣�C
�������������ƽ�ⳣ��ֻ���¶ȵ�Ӱ�죬A����Ũ����ͬʱ���볣���������Һ��c(H��)һ���ȵ��볣��С������Һ�еĴ�B����H2CO3�ĵ��볣������ʽ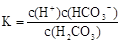 ��D�����ѡC��
��D�����ѡC��
����������ƽ�ⳣ��ֻ���¶��йأ��¶ȱ���K�䣬�¶Ȳ�����K���䡣
�����Ѷȣ���
4��ѡ���� ��֪Ksp(AgCl)=1.56��10-10��Ksp(AgBr)=7.7��10-13��Ksp(Ag2CrO4)=9.0��10-12��ij��Һ�к���C1-, Br- ��CrO42-��Ũ�Ⱦ�Ϊ0.010mo1��L-�������Һ����μ���0.010mol��L-1��AgNO3��Һʱ�����������Ӳ����������Ⱥ�˳��Ϊ
A��C1-��Br-��CrO42-
B��CrO42-��Br-��C1-
C��Br-��C1-��CrO42-
D��Br-��CrO42-��C1-