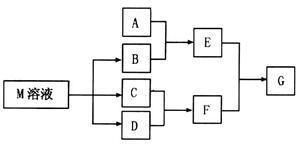
1、填空题 物质M是一种日常生活中不可缺少的调味品。已知C可在D中燃烧发出苍白色火焰。M与其他物质的转化关系如下图所示(部分产物已略去):
(1)写出用惰性电极电解M溶液的离子方程式?。
(2)若A是一种酸性氧化物,且可用于制造玻璃,则G的化学式是?。
(3)若A是一种常见金属单质,且A与B溶液能够反应,则将过量的F溶液逐滴加入E溶液,边加边振荡,所看到的实验现象是?。
(4)若A是一种盐,A溶液与B溶液混合产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则由A转化成E的离子方程式是?。
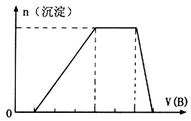
(5)若A是一种溶液,只可能含有 中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示。由此可知,该溶液中肯定含有的离子及其浓度之比为?。
中的某些离子,当向该溶液中加入B溶液时发现生成沉淀的物质的量随B溶液的体积发生变化如图所示。由此可知,该溶液中肯定含有的离子及其浓度之比为?。
参考答案:(1)2Cl?+2H2O 2OH?+H2↑+Cl2↑(2分)
2OH?+H2↑+Cl2↑(2分)
(2)H2SiO3(1分)
(3)溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失(1分)
(4)4Fe2++8OH?+O2 +2H2O = 4Fe(OH)3↓(2分)
(5)c(H+):c(Al3+):c(NH4+):c(SO42?)=1:1:2:3(2分,推断出前三种且结果正确得1分)
本题解析:C可在D中燃烧发出苍白色火焰,可知二者分别为H2、Cl2,F为HCl,物质M是一种日常生活中不可缺少的调味品,为NaCl,则B为NaOH 。
(1)用惰性电极电解NaCl溶液,生成NaOH、H2、Cl2,离子方程式为:
2Cl?+2H2O 2OH?+H2↑+Cl2↑
2OH?+H2↑+Cl2↑
(2)若A是一种酸性氧化物,且可用于制造玻璃,则A为SiO2,与NaOH反应生成的E为Na2SiO3,与HCl反应生成的G为H2SiO3。
(3)A是一种常见金属单质,能与NaOH溶液反应,则A为Al,E为Na[Al(OH)4],将过量的盐酸逐滴加入Na[Al(OH)4]溶液,边加边振荡,Na[Al(OH)4]先与HCl反应生成Al(OH)3,继续加入HCl,Al(OH)3与HCl反应生成AlCl3,所以实验现象为:溶液中逐渐有白色絮状沉淀生成,且不断增加;然后又由多到少,最后消失。
(4)A溶液与B溶液混合产生白色絮状沉淀且瞬间变为灰绿色,最后变成红褐色的E,则A中含Fe2+,生成的E为Fe(OH)3,发生的反应有:Fe2++2OH?=Fe(OH)2↓,4Fe(OH)2+O2+2H2O=4Fe(OH)3,两步反应加和可得离子方程式:4Fe2++8OH?+O2 +2H2O = 4Fe(OH)3↓
(5)根据图像,设图像中加入单位体积的NaOH溶液含NaOH为1mol,加入第一部分NaOH没有沉淀生成,发生的反应为:OH?+H+=H2O,则原溶液含H+,物质的量为1mol;继续加入3mol NaOH生成沉淀,最后加入1mol NaOH,Al(OH)3溶解,则原溶液含Al3+,物质的量为1mol;则Mg2+、Fe3+、CO32?一定不存在;中间加入2mol NaOH,沉淀不变,发生的反应为OH?与NH4+反应,则原溶液含NH4+,物质的量为2mol,阴离子只能为SO42?,根据电荷守恒可得SO42?的物质的量为3mol,所以c(H+):c(Al3+):c(NH4+):c(SO42?)=1:1:2:3
本题难度:困难
2、选择题 能正确表示下列反应的离子方程式是( )
A.将氯化亚铁溶液和稀硝酸混合:Fe2++4H++NO3-=Fe3++2H2O+NO↑
B.将磁性氧化铁溶于盐酸:Fe3O4+8H+=3Fe3++4H2O
C.碳酸钙跟醋酸反应:CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑
D.将铁粉加入稀硫酸中:2Fe+6H+=2Fe3++3H2↑
参考答案:A.将氯化亚铁溶液和稀硝酸混合,暗影的离子方程式为3Fe2++4H++NO3-=3Fe3++2H2O+NO↑,故A错误;
B.磁性氧化铁溶于盐酸反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O,故B错误;
C.碳酸钙不溶于水,醋酸为弱电解质,二者反应的离子方程式为CaCO3+2CH3COOH=Ca2++2CH3COO-+H2O+CO2↑,故C正确;
D.铁和稀硫酸反应的离子方程式为Fe+2H+=Fe2++H2↑,故D错误.
故选C.
本题解析:
本题难度:一般
3、选择题 下列离子方程式正确的是?
A.铁跟盐酸反应:2Fe +6H+ ==2Fe3++3H2↑
B.氯气与水反应:Cl2 + H2O ="=" 2H++Cl+ClO-
C.硫酸与氢氧化钡溶液反应:Ba2++OH-+H++SO42-="=" BaSO4↓+ H2O
D.金属钠与水反应:2Na +2H2O ==2Na++2OH-+H2↑
参考答案:D
本题解析:
正确答案:D
A. 铁跟盐酸反应: Fe +2H+ ==Fe2++H2↑
B.氯气与水反应:Cl2 + H2O  ?H++Cl+HClO
?H++Cl+HClO
C.硫酸与氢氧化钡溶液反应:Ba2++2OH-+2H++SO42-="=" BaSO4↓+2H2O
本题难度:一般
4、选择题 下列离子方程式书写正确的是( )
A.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+=Ca2++2H2O
B.亚硫酸氢钠水HSO3-+H2O?SO32-+H3O+
C.氧化铁溶于氢碘酸:Fe2O3+6H+=2Fe3++3H2O
D.用石墨电极电解NaCl溶液:2Cl-+2H2O
2OH-+Cl2↑+H2↑
参考答案:
A.离子方程式中应将易溶于水,易电离的强电解质拆成离子形式.该选项中澄清的石灰水和稀盐酸都属于此类.故澄清的石灰水与稀盐酸反应的离子方程式为:H++OH-=H2O.故A错误;
B.亚硫酸是二元弱酸,根据盐类水解的规律,亚硫酸氢根离子水解,水解生成亚硫酸,其水解方程式为::HSO3-+H2O?H2SO3+OH-.故B错误;
C.氧化铁与氢碘酸电离出的氢离子反应,生成+3价的铁离子,但Fe3+能将氢碘酸电离出的-1价的碘离子氧化,其正确的离子反应方程式为:Fe2O3+6H++2I-=2Fe2++3H2O+I2.故C错误;
D.用石墨作电极电解氯化钠溶液,阳极吸附的是溶液中的阴离子Cl-、OH-,Cl-比OH-更易失去电子,发生反应:2Cl--2e-=Cl2↑,生成氯气和氢氧化钠,阴极吸附溶液中H+和Na+,H+优先于Na+得到电子,发生反应:2H++2e-=H2↑,生成氢气,所以总的电极反应为:2Cl-+2H2O?电解?.?2OH-+Cl2↑+H2↑,故D正确;
故选D.
本题解析:
本题难度:一般
5、选择题 能正确表示下列化学反应的离子方程式的是
A.氢氧化钡溶液与盐酸的反应 2OH-+2H+= 2H2O
B.澄清的石灰水与稀盐酸反应 Ca(OH)2 + 2H+= Ca2+ + 2H2O
C.铜片插入硝酸银溶液中 Cu + Ag+= Cu2+ + Ag
D.碳酸钙溶于稀盐酸中 CaCO3+2H+=Ca2++H2O+CO2?
参考答案:D
本题解析:A错,离子方程式是化学计量数也应为最简整数比;B错,澄清石灰水要拆成离子形式;C错,电荷未守恒;D正确;
本题难度:简单