1、填空题 下图中A―F均为中学化学中常见的物质,它们之间有如下转化关系。其中A、D 为金属单质。(反应过程中水及其他产物已略去)

(1)C是?,J是?(填化学式)。
(2)写出C与NaOH反应生成F的化学方程式 ?
(3)A在常温下也可与NaOH溶液反应生成F,写出此反应的化学反应方程式?:
参考答案:(1) Al2O3,(2分) FeCl3(2分)
(2)Al2O3+2NaOH=2NaAlO2 + H2O?(2分)
(3)2Al+2NaOH+2H2O=2NaAlO2 +3H2 ↑(2分)
本题解析:(1)由I红褐色固体知I为氢氧化铁,D为单质,所以根据元素守恒得D为铁单质;C能与氢氧化钠溶液反应,猜想C为氧化铝,则A与B的反应是铝与氧化铁高温炼铁的反应。所以C为Al2O3,J为FeCl3
(2)C为氧化铝,与氢氧化钠溶液反应生成偏铝酸钠和水,化学方程式为Al2O3+2NaOH=2NaAlO2 + H2O?
(3)A为单质Al,与氢氧化钠溶液反应生成偏铝酸钠和氢气,化学方程式为2Al+2NaOH+2H2O=2NaAlO2 +3H2↑
本题难度:一般
2、选择题 某同学研究铝及其化合物的性质时设计了如下两个实验方案。
方案①:2.7 g Al X溶液
X溶液 Al(OH)3沉淀
Al(OH)3沉淀
方案②:2.7 g Al Y溶液
Y溶液 Al(OH)3沉淀
Al(OH)3沉淀
NaOH溶液和稀盐酸的浓度均是3 mol/L,如图是向X溶液和Y溶液中分别加入NaOH溶液和稀盐酸时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法正确的是
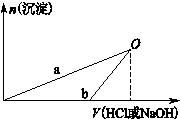
A.X溶液溶质为AlCl3,Y溶液溶质为NaAlO2
B.b曲线表示的是向X溶液中加入NaOH溶液
C.在O点时两方案中所得溶液浓度相等
D.a、b曲线表示的反应都是氧化还原反应
参考答案:C
本题解析:A项:A项:由题意知X溶液为AlCl3溶液,Y为NaOH和NaAlO2的混合溶液,前者因AlCl3水解而显酸性,后者显碱性;B、D项:a曲线表示的是向X溶液中加入NaOH溶液, b曲线表示的是向Y溶液中加入盐酸,两曲线表示的反应都是非氧化还原反应;C项:O点所得溶液的溶质只是NaCl,由于向X溶液和Y溶液中所加盐酸和氢氧化钠溶液的浓度及体积均相等,由原子守恒可知,在O点时两方案中所得NaCl的物质的量相同,浓度也相同。故选C。
点评:铝既能与酸反应又能与碱反应且反应都有氢气生成,经常用来一起考察,清楚其中反应原理是解题的关键。
本题难度:简单
3、选择题 下列物质既能跟硫酸反应,又能跟氢氧化钠溶液反应的是
A.Al
B.NaHCO3
C.Al2O3
D.Al(OH)3
参考答案:ABCD
本题解析:铝的单质、氧化物、氢氧化物均有两性;弱酸酸式盐均符合要求。
本题难度:简单
4、选择题 将由Mg和Al组成的一定质量的混合物投入500 mL 稀硫酸中,固体全部溶解并产生气体。待反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液的体积关系如右图所示。则下列说法正确的是
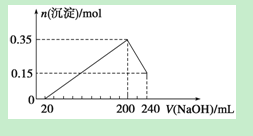
A.上述由Mg和Al组成的混合物的质量为8g
B.硫酸的物质的量浓度为1 mol・L-1
C.生成的H2在标准状况下的体积为11.2L
D.NaOH溶液的物质的量浓度为3.75 mol・L-1
参考答案:B
本题解析:A、混合质量为0.15×24+0.35×27="9" g,错误;B、氢氧化钠的物质的量浓度是0.2mol÷0.04L=5.0mol/L,则沉淀最大值是生成硫酸钠是(0.2L×5mol/L)÷2=0.5mol,所以稀硫酸的浓度是0.5mol÷0.5L=1.0mol/L,正确;C、稀硫酸反应生成的氢气是0.3mol+0.15mol=0.45mol,标准状况下的体积是10.08L,错误;D、根据反应Al(OH)3+NaOH=NaAlO2+2H2O可知,氢氧化钠的物质的量浓度是0.2mol÷0.04L=5.0mol/L,错误。
本题难度:一般
5、填空题 某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。

请回答下列问题。
(1)?图中涉及分离溶液与沉淀的方法是____________________________。
(2)? B、C、D、E四种物质的化学式为:
B__________、C__________、D__________、E__________。
(3) 写出下列反应的离子方程式:
沉淀F与NaOH溶液反应________________________________。
沉淀E与稀硫酸反应____________________________。
溶液G与过量稀氨水反应________________________________。
参考答案:(1) 过滤?(2) B:? Al2O3? C:? Fe2O3? D:? NaAlO2? E: Al(OH)3
(3) Al2O3+2OH-=AlO2-+H2O; Al(OH)3+3H+=Al3++3H2O;Al3++3NH3・H2O=3NH4++Al(OH)3↓
本题解析:Al2(SO4)3、Al2O3和Fe2O3中Al2(SO4)3溶于水,Al2O3溶于NaOH,可确定B:? Al2O3? C:? Fe2O3? D:? NaAlO2? E: Al(OH)3。
本题难度:一般