1、选择题 下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡:Cl2+H2O HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)  H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2  CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(N2+3H2 2NH3;DH<0)
2NH3;DH<0)
参考答案:B
本题解析:勒夏特列原理适应于可逆反应,当系统的条件改变时所遵循的原理;
A.当加入AgNO3溶液后,银离子消耗了氯离子,产物浓度减少,平衡右移,氯气的浓度减少,溶液颜色变浅,符合勒夏特列原理
B.反应2HI(g)  H2(g)+I2(g)属于两连气体系数相等的可逆反应,增大压强平衡并不发生移动,但由于体系体积减小,各物质的浓度均增大,体系颜色一样变深,但并不能用勒夏特列原理来解释,符合题意
H2(g)+I2(g)属于两连气体系数相等的可逆反应,增大压强平衡并不发生移动,但由于体系体积减小,各物质的浓度均增大,体系颜色一样变深,但并不能用勒夏特列原理来解释,符合题意
C.升高温度可使平衡向吸热反应方向移动,符合勒夏特列原理
D.降低温度,可逆反向放热反应方向移动,可得到更多的氨气,符合勒夏特列原理
故答案为B
本题难度:简单
2、选择题 恒温下,容积均为2L的密闭容器M、N中,分别有以下列两种起始投料建立的可逆反应3A(g)+2B(g) 2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol・(L・min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol・L-1。下列推断的结论中不正确的是
2C(g)+xD(s)的化学平衡状态,相关数据如下:M:3 mol A 、2 mol B;2 min达平衡,生成D 1.2 mol,测得从反应开始到平衡C的速率为0.3 mol・(L・min)-1。N:2 mol C 、y mol D;达平衡时c(A)="0.6" mol・L-1。下列推断的结论中不正确的是
A.x=2? B.平衡时M中c(A)>0.6 mol/L?
C.y≥2? D.M、N达到平衡时容器中各物质浓度相等
参考答案:B
本题解析:解:A从反应开始到平衡,C的速率为0.3mol/(L?min),则△n(C)=0.3mol/(L?min)×2min×2L=1.2mol,物质的量之比等于化学计量数之比,所以2:x=1.2mol:1.2mol,解得x=2,故A正确;B从反应开始到平衡,C的速率为0.3mol/(L?min),所以△c(C)=0.3mol/(L?min)×2min=0.6mol/L,浓度变化量之比等于化学计量数之比,所以△c(A)=3/2△c(C)=3/2×0.6mol/L=0.9mol/L,所以平衡时c(A)=1.5mol/L-0.9mol/L=0.6mol/L,故B不正确;C由B中计算可知M中A的平衡浓度为0.6mol/L,所以M、N是等效平衡,则按化学计量数转化到左边满足n(A)=3mol,n(B)=2mol,恰好转化时y=3mol×2/3=2mol,由于D为固体,故y≥2,故C正确;D由C中分析可知y≥2,故D正确;故选B。
本题难度:一般
3、选择题 在2L容积不变的容器中,发生N2+3H2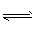 2NH3的反应。现通入4 molH2和4molN2,10 s内用H2表示的反应速率为0.12 mol/(L・s),则10 s后容器中N2的物质的量是
2NH3的反应。现通入4 molH2和4molN2,10 s内用H2表示的反应速率为0.12 mol/(L・s),则10 s后容器中N2的物质的量是
[? ]
A.1.6 mol
B.2.8 mol
C.3.2 mol
D.3.6 mol
参考答案:C
本题解析:
本题难度:简单
4、选择题 在2A + B = 3C + 4D的反应中,下列表示该反应速率最大的是
[? ]
A.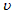 (A)=0.5 mol・L-1・min-1
(A)=0.5 mol・L-1・min-1
B.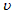 (B)=0.3 mol・L-1・min-1
(B)=0.3 mol・L-1・min-1
C.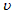 (A)=0.8 mol・L-1・min-1
(A)=0.8 mol・L-1・min-1
D.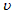 (D)=1 mol・L-1・min-1
(D)=1 mol・L-1・min-1
参考答案:C
本题解析:
本题难度:简单
5、选择题 在一定条件下,对于反应mA(g)+nB(g) cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )
cC(g)+dD(g),C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的ΔH和ΔS判断正确的是( )
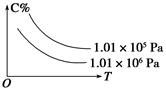
A.ΔH<0 ΔS>0
B.ΔH>0 ΔS<0
C.ΔH>0 ΔS>0
D.ΔH<0 ΔS<0
参考答案:A
本题解析:因为温度越高,生成物C的百分含量越低,所以为放热反应,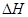 <0,压强增大,化学平衡向体积减少的方向移动,而随着压强的增大,图中生成物C的含量越小,所以c+d>m+n,所以ΔS>0,故A正确。
<0,压强增大,化学平衡向体积减少的方向移动,而随着压强的增大,图中生成物C的含量越小,所以c+d>m+n,所以ΔS>0,故A正确。 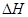 、
、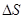 。
。
本题难度:一般