1、实验题 某同学在气体体积测定仪中用镁和硫酸反应测定1 mol氢气体积。完成下列填空:
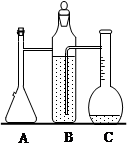
(1)A中发生反应的离子方程式为______________________。
(2)检查装置气密性的方法是塞上B瓶的玻璃塞,用橡皮塞塞紧A瓶加料口,当看到__________________现象时,可以确认装置气密性良好。
(3)已知液体量瓶的刻度范围是110~130 mL,实验时称取镁带的质量要控制在0.100~0.110 g之间,目的是_________。
(4)完成一次测定实验,需要2次用注射器抽气,其中需要记录的是第__________次抽出气体的体积。
(5)下列情况会导致实验结果偏高的是______(填编号)
a. 镁表面的氧化膜没有除尽? b. 储液瓶中的液体是水
c. 未冷却到室温就读数? d. 装置气密性不好
参考答案:(1)Mg+2H+→Mg2++ H2↑(2分)。?(2)B中导管内液面上升,并且一分钟内不下降。(3)确保产生气体体积在刻度范围之内。?(4)2。?(5)c。
本题解析:仪器名称分别为:A气体发生器;B储液瓶;C液体量瓶;
(1)A中是镁和硫酸反应生成硫酸镁和氢气,依据产物写出离子方程式;
(2)装置气密性可以利用装置内气体压强变化和液面变化分析判断装置气密性;
(3)取110和30 mL两个极端值,可以算出氢气的物质的量,氢气的物质的量和镁的物质的量相等,换算成镁的质量,就会得到范围0.100~0.110 g,这么做的目的当然是确保产生气体体积在刻度范围之内。
(4)每次做实验时,用注射器在A瓶加料口抽气,使B瓶导管内液体持平(B瓶内气体压强与外界大气压相等),注意注射器拔出时要将针头拔出,此时进入测定起始状态;再次抽气调压,用注射器在A瓶加料口处抽气,使B瓶中液面持平,与起始状态相同,读出注射器中抽出气体的体积,记录数值,所以每次试验要用2次注射器抽气,平行做3次实验共用注射器抽气6次。
(5)a. 镁条表面的氧化物没有除,部分氧化物和硫酸反应而没有气体生成,会导致气体体积偏小,故错误。
b. 储液瓶中的液体是水,会导致气体体积偏小,故错误。?
c.未冷却到室温就读数,热涨冷缩,导致气体体积偏大,故正确。
d. 装置气密性不好,当然会导致气体体积偏小,故错误。
本题难度:一般
2、实验题 测某种含有少量氧化钠的过氧化钠试样的质量分数。
方法一:利用下图装置测定混合物中Na2O2的质量分数,已知试样质量为1.560g、锥形瓶和水的质量为190.720g,每隔相同时间读得电子天平的数据如表:

(1)写出Na2O2和H2O反应的化学方程式________________
(2)该试样中过氧化钠的质量分数为____________________(保留3位有效数字)
不必作第6次读数的原因是____________________________________
方法二:测定上述样品(1.560g)中Na2O2质量分数的另一种方案,其操作流程如下:

(3)操作Ⅱ的名称是________________________
(4)需直接测定的物理量是______________________________
(5)测定过程中需要的仪器有电子天平、蒸发皿、酒精灯、还需要________、_______(固定、夹持仪器除外)
(6)在转移溶液时,如溶液转移不完全,则Na2O2质量分数的测定结果__________________
(填偏大、偏小或不变)。
方法三:请从下图中选用适当仪器测定混合物中Na2O2的质量分数,要求操作简单。
除待测试样外,限选试剂:CaCO3固体,6mol/L盐酸和蒸馏水
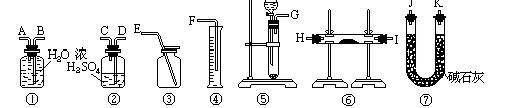
(7)所选用装置的连接顺序应是(填各接口的字母;连接胶管省略)__________________。
参考答案:(1)2Na2O2+2H2O→4NaOH+O2↑(2分)
(2)0.844
第4(或5)次读数(或用具体数值表示)锥形瓶内质量已达恒量。(2分)
(3)蒸发(1分)?(4)NaCl的质量 (1分)
(5)烧杯?玻璃棒?(2分)
(6)偏大 (2分)?(7) (G)接(A)(B)接(F)?(3分)
本题解析:略
本题难度:一般
3、实验题 某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子。以下是某化学研究性学习小组的同学设计的除去污水中的金属离子,回收绿矾、皓矾(ZnSO4・7H2O)和汞的方案。
【药品】NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
【实验方案】
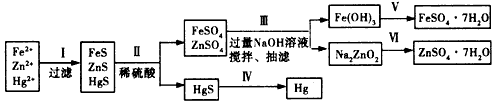
【问题探究】
(1)步骤Ⅱ所发生反应的离子方程式为____________________
(2)步骤Ⅲ中的抽滤为减压条件下的过滤,可以加快过滤速度;该步骤涉及反应的离子方程式有
Zn2++4OH-=ZnO22-+2H2O和_______________________
(3)步骤Ⅵ中得到硫酸锌溶液的离子反应方程式为_______________________
(4)欲实现步骤V,所需加入的试剂有____、____, 所涉及的主要操作依次为________________
(5)步骤Ⅳ常用的方法是___________,该步骤是否对环境有影响?_______(填“是”或“否”),如有影响,请你设计一个环境保护方案来实现步骤Ⅳ的反应____________________
参考答案:(1)FeS+2H+=Fe2++H2S↑、ZnS+2H+=Zn2++H2S↑
(2)4Fe2++O2+8OH-+2H2O=4Fe(OH)3↓
(3)ZnO22-+4H+=Zn2+ +2H2O
(4)稀硫酸;铁粉(过量);过滤、浓缩结晶、过滤
(5)加热;是;在密闭容器中加热HgS
本题解析:
本题难度:一般
4、实验题 用如图所示装置进行实验,将A逐滴加入B中。
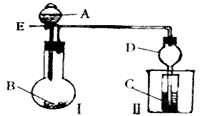
(1)若A为浓硫酸,B为第三周期金属元素的片状单质,其在常温下难与水反应;C为品红溶液,实验中观察到C中溶液褪色,则B是_______,然后往烧杯中加入沸水,又可观察到的现象是________。
(2)若B为Na2CO3,C为NaAlO2溶液,实验中观察到小试管内溶液变浑浊,则酸A的酸性比_______强,写出试管C中反应的离子方程式__________。
(3)若B是生石灰,实验中观察到C中溶液由无色变为红色,若在C中加入醋酸铵固体红色变浅,则A是__________,解释C中加入醋酸铵固体红色变浅的原因:__________(用方程式及必要的文字说明) 。
参考答案:(1)镁;C中的溶液又变为红色。
(2)碳酸;AlO2-+2H2O+CO2=Al(OH)3↓+HCO3- 或2AlO2-+3H2O+CO2=2Al(OH)3↓+CO32-
(3)浓氨水 ;NH3・H2O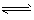 NH4+ + OH- ,加入固体醋酸铵后,使溶液中c(NH4+)增大,氨水的电离平衡向左移动,c(OH-)变小,溶液的颜色变浅。
NH4+ + OH- ,加入固体醋酸铵后,使溶液中c(NH4+)增大,氨水的电离平衡向左移动,c(OH-)变小,溶液的颜色变浅。
本题解析:
本题难度:一般
5、填空题 我国规定饮用水质量标准必须符合下列要求:
pH
| 6.5~8.5
|
Ca2+、Mg2+
| <0.004 5 mol・L-1
|
细菌总数
| <100个/mL
|
以下是源水处理成自来水的工艺流程示意图
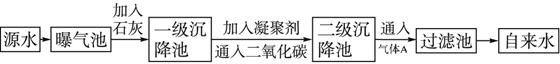
(1)源水中含Ca2+、Mg2+、HCO3-、Cl-等,加入生石灰后生成Ca(OH)2,进而发生若干复分解反应,写出其中一个离子方程式:_________________________。
(2)凝聚剂除去悬浮固体颗粒的过程____________(填序号)。FeSO4・7H2O是常用的凝聚剂,它在水中最终生成____________沉淀。
①只是物理过程 ? ②只是化学过程? ③是物理和化学过程
(3)通入二氧化碳的目的是________________和______________________。
(4)气体A的作用是_________________________。这种作用是基于气体A和水反应的产物具有__________性。
(5)下列物质中____________可以作为气体A的代用品。
①Ca(ClO)2 ②NH3(液)? ③K2FeO4 ? ④SO2
参考答案:(1)Ca2++HCO-3+OH-=CaCO3↓+H2O,Mg2++2OH-=Mg(OH)2↓?
(2)③? Fe(OH)3?(3)调节pH?除去Ca2+?
(4)杀菌消毒?强氧化?(5)①③?
本题解析:(1)源水中存在Ca2+,Mg2+,HCO-3,Cl-,溶质为Ca(HCO3)2,Mg(HCO3)2,CaCl2,MgCl2,分别与Ca(OH)2发生复分解反应,化学方程式为:?Ca(HCO3)2+Ca(OH)2=2CaCO3↓+2H2O;?Mg(HCO3)2+2Ca(OH)2=Mg(OH)2↓+2CaCO3↓+2H2O;?MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2?。根据以上三个反应可以写出离子方程式:?Ca2++HCO-3+OH-=CaCO3↓+H2O,?Mg2++2HCO-3+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O,Mg2++2OH-=Mg(OH)2↓。?
(2)常用明矾、FeCl3溶液作源水的凝聚剂,利用Al3+或Fe3+水解成Al(OH)3或Fe(OH)3胶体吸附水中悬浮的固体颗粒,这一过程既有化学变化又有物理变化,如果用FeSO4・7H2O作凝聚剂,Fe2+发生水解:Fe2++2H2O Fe(OH)2+2H+,Fe(OH)2又迅速被氧化成Fe(OH)3:4Fe(OH)2+O2+2H2O=4Fe(OH)3,最终生成Fe(OH)3沉淀。
Fe(OH)2+2H+,Fe(OH)2又迅速被氧化成Fe(OH)3:4Fe(OH)2+O2+2H2O=4Fe(OH)3,最终生成Fe(OH)3沉淀。
(3)通入CO2的目的是调节pH和进一步除去水中的Ca2+。?
(4)通入气体A用于对源水杀菌消毒,气体A必须有强氧化性。?
(5)代替A气体的物质必须有强氧化性,可选择Ca(ClO)2,K2FeO4,O3等。
点评:本题主工考查源水处理成自来水的工艺流程,难度不大,侧重考查学生实验分析能力和逻辑推断能力,解题的关键是要结合题干信息,分析每一流程的作用,从而准确作答。
本题难度:一般