1������� ��14�֣�(1)���ĺϳ�������Ҫ�Ļ�������֮һ����ҵ�Ϻϳɰ��õ�H2�ж�����ȡ�ķ���������Ȼ����ˮ������Ӧ��CH4(g)��H2O(g)  CO(g)��3H2(g)����֪�йط�Ӧ�������仯����ͼ��ʾ�������ȡH2��Ӧ�Ħ�H��____________��
CO(g)��3H2(g)����֪�йط�Ӧ�������仯����ͼ��ʾ�������ȡH2��Ӧ�Ħ�H��____________��
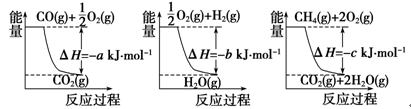
��2����֪ͨ��״���£�ÿ���ȼ��1gCO���ָ���ԭ״̬�����ͷ�10KJ����������д����ʾCOȼ���ȵ��Ȼ�ѧ��Ӧ����ʽ�� ��
��3��һ�ּ���ȼ�ϵ���Dz��ò���̼������Ϊ�缫��������ϡ������Һ��ֱ��ͨ����飬ͬʱ��һ���缫ͨ��������˵�صĸ����缫��Ӧʽ��________________________________________________��
��4��������ͼװ�ÿ���ģ�����ĵ绯ѧ������
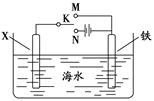
����XΪ̼����Ϊ�������ĸ�ʴ������KӦ���� �������躣ˮ��ֻ��NaCl���ʣ�д����ʱ�����ӷ�Ӧ����ʽ�� ��
����XΪп������K����M�����õ绯ѧ��������Ϊ ��
д�����缫���ĵ缫��Ӧʽ�� ��
�ο��𰸣���1����H��(a��3b��c) kJ��mol��1 ��2�֣�
��д�ɦ�H��+(a��3b��c) kJ��mol��1 ��H��-(c-a-3b) kJ��mol��1����ȷ©д��λ��1�֣�
��2��CO��g��+1/2O2(g)=CO2(g) ��H��-280KJ/mol (2��)
����״̬���÷֣�COϵ����Ϊ1���÷֣�©��λ��1�֡���
��3��CH4 -8e- + 2H2O = CO2 + 8H+ ��2�֣�
�����ʴ�©���÷֣�ϵ������1�֣�
��4����N��2�֣� 2Cl����2H2O 2OH����H2����Cl2�� ��2�֣�
2OH����H2����Cl2�� ��2�֣�
��д�ɻ�ѧ����ʽ���÷֣�ϵ���������ͼ�ͷ���ܿ�1�֣�
���������������������� (2��) O2+2H2O+4e��=4OH�� ��2�֣�
�����������1��������Ӧ���Ȼ�ѧ����ʽΪ����CO��g��+1/2O2��g��=CO2��g�� ��H��-aKJ/mol�� ��2H2��g��+O2��g��=2H2O��g�� ��H��-bKJ/mol����CH4��g��+2O2��g��=CO2��g��+2H2O��g�� ��H��-cKJ/mol�����ݸ�˹���ɷ�����������ӦӦ�â�+3����-�ۣ����Է�Ӧ�Ȧ�H��(a��3b��c) kJ��mol��1����2��1��һ����̼�����ʵ���Ϊ1/28Ħ��������ÿĦ��һ����̼��Ӧ���ɶ�����̼��Ӧ�ų�������Ϊ280KJ�����Ȼ�ѧ����ʽΪ��CO��g��+1/2O2(g)=CO2(g) ��H��-280KJ/mol����3��������ԭ��������������������·�Ӧ���ɶ�����̼��ˮ���缫��ӦΪ��CH4 -8e- + 2H2O = CO2 + 8H+����4����XΪ̼�����������ĸ�ʴ����Ҫ�������ص�������������N������Ȼ��ƣ���Ӧ�����������ƺ����������������ӷ���ʽΪ��2Cl����2H2O 2OH����H2����Cl2������XΪп��������M����������ԭ��ص����������ֵ绯ѧ������Ϊ���������������������� ��Ϊԭ��ص�����������������ʴ���缫��ӦΪ��O2+2H2O+4e��=4OH����
2OH����H2����Cl2������XΪп��������M����������ԭ��ص����������ֵ绯ѧ������Ϊ���������������������� ��Ϊԭ��ص�����������������ʴ���缫��ӦΪ��O2+2H2O+4e��=4OH����
���㣺��ѧ��Ӧ������
�����Ѷȣ�����
2������� �״���һ��ȼ�ϣ�Ҳ������Ϊȼ�ϵ�ص�ԭ�ϣ�

��1����֪�ڳ��³�ѹ�£�
��2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H1=-1275.6KJ/mol
��2CO?��g��+O2��g��=2CO2��g����H2=-566.0KJ/mol
��H2O��g��=H2O��l����H3=-44.0KJ/mol
д���״�����ȫȼ������һ����̼��Һ̬ˮ���Ȼ�ѧ����ʽ��______��
��2���״�ֱ��ȼ�ջ����һ������Ⱦ��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ1��ʾ�ĵ��װ�ã����������ĵ缫��Ӧʽ��______���õ�ع���ʱ����Һ�е�OH-��______���ƶ����õ�ع���һ��ʱ������Һ��pH��С����õ���ܷ�Ӧ�����ӷ���ʽΪ______��
��3���״���ˮ�ʻ����һ������Ⱦ������ͼ2��ʾ�ĵ绯ѧ��������������Ⱦ��ԭ���ǣ�ͨ���Co2+������Co3+��Ȼ����Co3+���������ٰ�ˮ�еļ״�������CO2�����������ø�װ�þ�����10mol�״���ˮ��ת�Ƶ�����Ϊ______��
�ο��𰸣���1����֪����2CH3OH��l��+3O2��g��=2CO2��g��+4H2O��g����H=-1275.6kJ/mol
��2CO?��g��+O2��g��=2CO2��g����H=-566.0kJ/mol
��H2O��g��=H2O��l����H=-44.0kJ/mol
���ø�˹���ɽ���-��2+�ۿɵã�CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8kJ/mol��
�ʴ�Ϊ��CH3OH��l��+O2��g��=CO��g��+2H2O��l����H=-442.8kJ/mol��
��2�����Լ״�ȼ�ϵ���У���������������Ӧ���缫��ӦʽΪCH3OH-6e-+8OH-+=CO32-+6H2O������������ԭ��Ӧ���缫��ӦʽΪO2+2H2O+4e-=4OH-���õ�ع���ʱ����Һ�е�OH-���ƶ������ܷ�ӦʽΪ2CH3OH+3O2+4OH-=2CO32-+6H2O��
�ʴ�Ϊ��O2+2H2O+4e-=4OH-������2CH3OH+3O2+4OH-=2CO32-+6H2O��
��3���״�������CO2��CԪ�صĻ��ϼ�����+6�ۣ���10mol�״�ʧȥ60mol���ӣ�ת�Ƶĵ�����Ϊ60NA���ʴ�Ϊ��60NA��
���������
�����Ѷȣ�һ��
3��ѡ���� ���������Ȼ�ѧ����ʽ�ó��Ľ�����ȷ���ǣ�������
A����֪2H2��g��+O2��g���T2H2O��g����H=-483.6?kJ?mol-1˵��2?mol?H2��g����1?mol?O2��g���������ܺ�С��2?mol?H2O��g��������
B����֪C��s��ʯī���TC��s�����ʯ����H��0������ʯ��ʯī�ȶ�
C����֪NaOH��aq��+HCl��aq���TNaCl��aq��+H2O��l����H=-57.4?kJ?mol-1����20?g?NaOH��ϡ��Һ��ϡ������ȫ�кͣ��ų�28.7?kJ������
D����֪2C��s��+2O2��g���T2CO2��g����H12C��s��+O2��g���T2CO��g����H2�����H1����H2
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4������� ��ҵ���������Ҫ��ӦΪ��4NH3��g��+5O2��g�� 4NO��g��+6 H2O��g����H��
4NO��g��+6 H2O��g����H��
��1����֪������ȼ����Ϊ285��8 kJ/mol��
N2��g��+3H2��g��=2NH3��g�� ��H=��92��4 kJ/mol;
H2O��1��=H2O��g����H=+44��0 kJ/mol;
N2��g��+O2��g��=2NO��g����H=+180��6 kJ/mol��
��������ҵ���������Ҫ��Ӧ�ġ�H= ��
��2�����ݻ��̶����ܱ������з���������Ӧ�������ڲ������ʵ����ʵ���Ũ�����±���
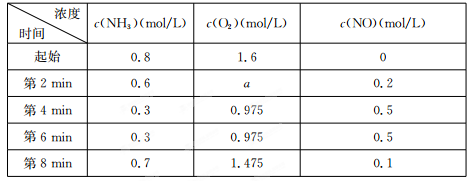
�ٷ�Ӧ�ڵ�2 min����4 minʱ��O2��ƽ����Ӧ����Ϊ ��
�ڷ�Ӧ�ڵ�6 minʱ�ı����������ı������������ ������ţ���
A��ʹ�ô��� B�������¶� C����Сѹǿ D������O2��Ũ��
������˵������˵��4NH3��g��+5O2��g�� 4NO��g��+6 H2 O��g���ﵽƽ��״̬���� ������ţ���
4NO��g��+6 H2 O��g���ﵽƽ��״̬���� ������ţ���
A����λʱ��������n mol NO����ʱ������n mol NH3
B������һ������������ƽ����Է����������ٱ仯
C���ٷֺ���w��NH3��=w��NO��
D����Ӧ����v��NH3����u��O2����v��NO����v��H2O��=4��5��4��6
E�����ں��º�ѹ���ݻ��ɱ�������з�Ӧ�����������ܶȲ��ٱ仯
��3��ij�о�����װ��CH3OH��O2ȼ�ϵ�صĹ���ԭ����ͼ��ʾ��
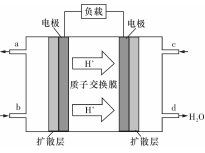
�ٸõ�ع���ʱ��b��ͨ�������Ϊ____ ��
�ڸõ�������ĵ缫��ӦʽΪ�� ��
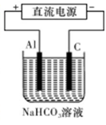
���Դ˵������Դ����ʵ������ģ������Ʒ���桰�ۻ���������װ����ͼ��ʾ���Ĺ����У�������Һ����Dz������ݲ�������ԭ������� ������ص����ӷ���ʽ��ʾ����
�ο��𰸣���1����904.8kJ��mol��1 ��2����0.1875mol/(L��min) ��B �� ABE
��3����CH3OH ��O2��4e����4H��=2H2O ��Al3����3HCO3��=Al(OH)3��3CO2(Al��3e����3HCO3-Al(OH)3��3CO2Ҳ����)
�����������1��H2��g��+1/2O2��g��
�����Ѷȣ�����
5��ѡ���� ��֪����������(B2H6)���������ܾ���ȼ�����������������ˮ��������1mol��̬ˮ�ɷų�678 kJ����������֪��H2O(l)=H2O(g) ��H=44 kJ/mol�������Ȼ�ѧ����ʽ�������
[? ]
A. B2H6(g) +3O2(g)=B2O3(s)+3H2O(l) ��H=-2 166kJ/mol
B. B2H6(g)+3O2(g)=B2O3(s)+3H2O(g) ��H=-2034kJ/mol
C. B2H6(g)+3O2(g)=B2O3(s)+3H2O(l) ��H=-2 078kJ/mol
D. 1/3B2H6(g)+O2(g)=1/3B2O3(s)+H2O(l) ��H=-722kJ/mol
�ο��𰸣�A
���������
�����Ѷȣ���