1������� (����)�ڵ�������Ԫ ���У���ϡ������Ԫ���⣺
���У���ϡ������Ԫ���⣺
��ԭ�Ӱ뾶��С��Ԫ����?������Ԫ�ط��ţ�
�ƽ�������ǿ��Ԫ����?������Ԫ�ط��ţ�
������������Ӧˮ����������ǿ����?�����û�ѧʽ�ش���ͬ����
����ȶ�����̬�⻯����?��
������������Ӧˮ���������ǿ����?��
���������о������Ե���?��
�ο��𰸣�Cl? Na? HClO4? SiH4? NaOH? Al2O3
�����������
�����Ѷȣ�һ��
2��ѡ���� ���ֶ�����Ԫ�ص�ԭ�Ӱ뾶��ijЩ���ϼۼ��±��������ж�����˵����ȷ���ǣ�?��
Ԫ�ش���
| A
| B
| D
| E
| G
| I
| J
| K
|
���ϼ�
| �C1
| �C2
| +4
�C4
| �C1
| +5
�C3
| +3
| +2
| +1
|
ԭ�Ӱ뾶��nm
| 0��071
| 0��074
| 0��077
| 0��099
| 0��110
| 0��143
| 0��160
| 0��186
|
?
A��A�ĵ����ܽ�E���ʴ�KE����Һ���û�����?
B��A��I��J�����Ӱ뾶�ɴ�С˳����A��J��I
C��GԪ�صĵ��ʲ�����ͬ��������
D��J��DB2��ȼ���������ֻ�����
�ο��𰸣�B
���������A������Ԫ����������ԭ�Ӱ뾶�����ϼ۵ı仯���ɣ�A��E�ǵ�������Ԫ�أ���A��ԭ�Ӱ뾶С��E������A��FԪ�أ�E��ClԪ�أ������ʲ����û���������Ϊ�����ʼ�����ˮ��Ӧ������B��I��J�ֱ���+3��+2�ۣ���J��ԭ�Ӱ뾶����I������J�ǵڶ�����Ԫ�أ�I�ǵ�������Ԫ�أ����ߵ�ԭ�Ӱ뾶������E������J��Mg��I��AlԪ�أ���A��I��J�����ӽṹ��ͬ�����ݰ뾶�ıȽ�ԭ�����Ӱ뾶�ɴ�С˳����A��J��I����ȷ��C��G���Ϊ+5�ۣ�Ϊ��������Ԫ�أ���ԭ�Ӱ뾶��E������G��PԪ�أ�����ͬ�������壬���ס����ף�����D������B��D�Ļ��ϼۺͰ뾶��С�ж�B��OԪ�أ�D��CԪ�أ���Mg�ڶ�����̼��ȼ�����ɵ���̼������þ������ѡB��
�����Ѷȣ�һ��
3��ѡ���� ����˵����ȷ����
A��Na+��Fe3+��Cl ��SCN
��SCN �ܴ���������ͬһ��Һ��
�ܴ���������ͬһ��Һ��
B��̼��������Һ������������������Һ��Ϻ������ӷ���ʽΪ��HCO3 + Ba2+ + OH
+ Ba2+ + OH ="=" BaCO3��+H2O
="=" BaCO3��+H2O
C����R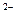 ��M+�ĵ��Ӳ�ṹ��ͬ����ԭ�������ıȽ�Ϊ��R>M
��M+�ĵ��Ӳ�ṹ��ͬ����ԭ�������ıȽ�Ϊ��R>M
D����Xԭ���е�������Ϊa��������Ϊb����X��������Ϊ��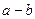
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
4��ѡ���� �����ѧ������Ǧ��Pb����봣�Kr������Ԫ�ص�ԭ�Ӻ˶�ײ�������һ��������Ϊ118��
������Ϊ293����Ԫ�أ���Ԫ��ԭ�Ӻ��ڵ��������ͺ��������֮��Ϊ
A��47
B��57
C��61
D��175
�ο��𰸣�B
�������������ԭ����˵�����ڵ����������ں���ĵ�������������Ϊ118������������Ҳ��118������������Ϊ293-118����Ԫ��ԭ�Ӻ��ڵ��������ͺ��������֮��Ϊ293��118��118=57�����ѡ��ΪB��
�����Ѷȣ���
5������� �±���Ԫ�����ڱ���һ���֡��������е���ĸ�ֱ����ijһ��ѧԪ�ء�
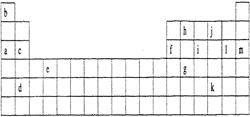
��1������?����д��ţ���Ԫ�صĵ��ʿ��ܶ��ǵ�������塣
��a��c��h?��b��g��k?��c��h��1?��d��e��f
��2���������������㹻����������Щ���ӱ�����ԭ�Ӻ˵���������ȥ����������뿪��ԭ�ӻ���������Ҫ��������Ҫ���������ص�Ӱ�죺��ԭ�Ӻ˶Ժ�����ӵ������������γ� �ȶ��ṹ�������±���һЩ��̬ԭ��ʧȥ���ⲻͬ���������������kJ��mol-1����
?
| �
| X
| Y
|
ʧȥ��һ������
| 519
| 502
| 580
|
ʧȥ�ڶ�������
| 7296
| 4570
| 1820
|
ʧȥ����������
| 11799
| 6920
| 2750
|
ʧȥ���ĸ�����
| ?
| 9550
| 11600
|
��ͨ��������Ϣ�ͱ��е����ݷ���Ϊʲô�ԭ��ʧȥ����ڶ�������ʱ���������ҪԶԶ����ʧȥ��һ�����������������?��
�ڱ��е�X����Ϊ����13��Ԫ���е�?������ĸ�����д��Ԫ�أ�����Ԫ�غ�j�γɵĻ������������ڹ��ۼ�����û�����ĵ���ʽ��?��������������?������ӡ����ۡ��������
��Y�����ڱ�����?���Ԫ�ء�
��������13��Ԫ���У�?������ĸ�����д��Ԫ��ԭ��ʧȥ�����һ��������Ҫ��������ࡣ
�ο��𰸣���1���٢ܣ�2�֣���һ����1�֣���һ����1�֣�����Ϊֹ��
��2����Liԭ��ʧȥһ�����Ӻ�Li�����γ��ȶ��ṹ����ʱ��ʧȥһ�����Ӻ����ѣ�2�֣�
��a��1�֣��� ��2�֣������ӣ�1�֣�
��2�֣������ӣ�1�֣�
�ۢ�A����������壩��1�֣�
��m��1�֣�
���������a-mԪ�طֱ�ΪNa��H��Mg��Ba��Ti��Al��Ge��C��P��O��Te��Cl��Ar����1�������������ҪΪ������ʯī�����塢����Լ��ᡢ��ε�ˮ��Һ�ȡ���2��Ԫ��Xʧȥ��һ��������������ԶԶС��ʧȥ�ڶ��������������������XԪ��λ�ڵ�һ���壬ΪNa����j�γɵĻ�������Na2O��Na2O2������Na2O2���й��ۼ���mΪϡ������Ԫ�أ��Ѵ��ȶ��ṹ���ʺ���ʧȥ���ӡ�
������Ԫ�����ڹ����Ǹ߿��ؿ�֪ʶ�㣬�����ڱ�����Ӧ���ΰ��ո����ɵĵݱ䣬��ע��������ն�����Ԫ�صĽṹ�����ʡ�
�����Ѷȣ�һ��