1、选择题 在a LAl2(SO4)3和(NH4)2SO4的混合溶液中加入b mol的BaCl2,恰好使溶液中的SO42-完全沉淀;如加入足量强碱并加热可得到cmolNH3,则原溶液中的Al3+的浓度(mol/L)为
[? ]
A.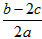
B.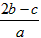
C.
D.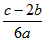
参考答案:C
本题解析:
本题难度:简单
2、选择题 用NaOH固体配制一定物质的量浓度的溶液时,必须用到的仪器是( )
A.分液漏斗
B.烧瓶
C.容量瓶
D.蒸发皿
参考答案:根据配制一定物质的量浓度的氢氧化钠溶液的步骤可知,配制过程中使用的仪器有:托盘天平、药匙、烧杯、玻璃棒、容量瓶、胶头滴管等,所以选项中必须使用的仪器为容量瓶,而分液漏斗、烧瓶和蒸发皿,在配制中不会用到,
故选C.
本题解析:
本题难度:简单
3、简答题 实验室欲配制0.5mol?L-1的NaOH溶液500mL有以下仪器:①烧杯②100mL量筒③1?000mL容量瓶④500mL容量瓶⑤玻璃棒⑥托盘天平(带砝码)
(1)配制时,必须使用的仪器有(填代号)______,
还缺少的仪器是______
(2)需称量______g烧碱固体,固体应放在______中称量.
(3)使用容量瓶前必须进行的一步操作是______.
(4)配制时,一般可分为以下几个步骤:①称量②计算③溶解④摇匀⑤转移⑥洗涤⑦定容⑧冷却.操作顺序为(填代号)______.
(5)在配制过程中,其他操作都正确,下列操作不会引起结果偏低的是(填代号)______.
①未洗涤烧杯、玻璃棒?②未等NaOH溶液冷却至室温就转移到容量瓶中③容量瓶不干燥,含有少量蒸馏水?④定容时俯视标线⑤定容时仰视标线?⑥NaOH用纸盛装进行称量⑦超过刻度线,吸出一部分水?⑧摇匀后液面下降,补充水.
参考答案:(1)操作步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,所以还需要的仪器为胶头滴管、药匙.
故答案为:①④⑤⑥;胶头滴管、药匙.
(2)需氢氧化钠的质量为m=0.5L×0.5mol?L-1×40g/mol=10.0g.
氢氧化钠有腐蚀性易潮解的药品应放在小烧杯内称量
故答案为:10.0;小烧杯.
(3)使用容量瓶前必须检查是否漏水.
故答案为:查漏.
(4)操作步骤有称量、溶解、移液、洗涤、定容、摇匀等操作,一般用托盘天平称量,用药匙取用药品,在烧杯中溶解,冷却后转移到500mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.所以操作顺序为②①③⑧⑤⑥⑤⑦④.
故答案为:②①③⑧⑤⑥⑤⑦④.
(5)①未洗涤烧杯、玻璃棒,少量氢氧化钠沾在烧杯壁与玻璃棒上,氢氧化钠的实际质量减小,溶液浓度偏低;
?②液体具有热胀冷缩的性质,氢氧化钠溶解放热,未冷却到室温,趁热将溶液到入容量瓶,并配成了溶液,会导致溶液体积偏小,溶液浓度偏高;
③最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
④定容时,俯视容量瓶刻度线,使溶液的体积偏低,所以溶液浓度偏高;
⑤定容时,仰视容量瓶刻度线,使溶液的体积偏大,所以溶液浓度偏低;
⑥用滤纸作为载体称量NaOH之后在转移NaOH的时候回损失一小部分NaOH的,所以回造成溶质质量减小,造成浓度偏低.
⑦超过刻度线,溶液体积增大,即使吸出一部分水,溶液也已经配制完,溶液浓度偏低;
⑧摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低.
偏高的是?②④;偏低的是①⑤⑥⑦⑧;没有影响的是③.
不会引起结果偏低的是②③④
故答案为:②③④
本题解析:
本题难度:一般
4、简答题 利用“化学计量在实验中的应用”的相关知识进行填空
(1)实验室需要0.5mol/L的硫酸溶液500mL,若用质量分数为98%、密度为1.84g/cm3的浓硫酸来配制,则所需该浓硫酸的体积为
______mL(列出计算过程).
(2)在标准状况下,由CO和CO2组成的混合气体8.96L,质量是16g.此混合物中CO和CO2的物质的量之比是______,混合气体的平均摩尔质量是______.
参考答案:(1)浓硫酸的物质的量浓度为1000×1.84×98%98mol/L=18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,令需要浓硫酸的体积为V,则:
500mL×0.5mol/L=V×18.4mol/L
解得:V=13.6mL
故答案为:13.6;
(2)8.96LCO和CO2混合气体的物质的量为8.96L22.4L/mol=0.4mol,
令CO和CO2的物质的量分别为xmol、ymol,则:
本题解析:
本题难度:一般
5、选择题 等体积的NaCl、MgCl2、AlCl3三种溶液分别与等体积等物质和量浓度的AgNO3溶液恰好完全反应,则NaCl、MgCl2、AlCl3三种溶液的物质的量浓度之比是
[? ]
A.1:1:1?
B.1:2:3?
C.3:2:1?
D.6:3:2
参考答案:D
本题解析:
本题难度:简单