1、填空题 化学在环境保护中起着十分重要的作用。催化反硝化法和电化学降解法可用于治理水中硝酸盐的污染。
(1)催化反硝化法中,H2能将NO3-还原为N2。25℃时,反应进行l0 min,溶液的pH由7变为l 2。
①N2的结构式为
②上述反应的离子方程式为 ,其平均反应速率v(NO3-)为 mol・L-1・min-1。
③还原过程中可生成中间产物NO2-,写出2种促进NO2-水解的方法 。
(2)电化学降解NO3-的原理如下图所示。
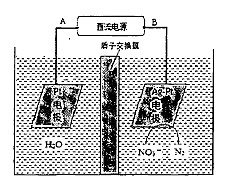
①电源正极为 (填“A”或“B”),阴极反应式为:
②若电解过程中转移了2 mol电子,则膜两侧电解液的质量变化差(△m左-△m右)为 g。
参考答案:(1)①N≡N 2NO3-+5H2 N2+2OH-+4H2O 0.001mol/(L・min)
N2+2OH-+4H2O 0.001mol/(L・min)
③加酸,升高温度,加水
(2)A, 2NO3-+6H2O+10e-=N2+12OH- ②14.4
本题解析: (1) ②废水不应显酸性(HNO3易挥发),而是中性或碱性,所以O2-在水中以H2O或OH-形式存在,有题意也可看出生成OH-(溶液pH由7变为12),依据氧化还原反应规律可配平:
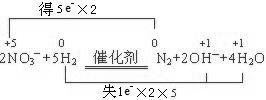
pH=12 c(H+)=1×10-12mol・L-1
c(H+)=1×10-12mol・L-1
 c(OH-)=
c(OH-)= 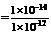 1×10-2mol・L-1
1×10-2mol・L-1
υ(NO3-)=υ(OH-)= 1×10-10mol・L-1 /10min= 0.001mol・L-1・min-1
③由方程式知NO2-+H2O HNO2+OH-△H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
HNO2+OH-△H>0 ,加热,加酸均可均可使平衡正向移动,促进NO2-转化。
(2)①2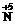 O3-+10e-→
O3-+10e-→ +6O2,所以B极为电源负极,A极为电源正极。
+6O2,所以B极为电源负极,A极为电源正极。
O2-+H2O=2OH-,可以写出阴极反应式:2NO3-+6H2O+10e-= N2↑+12OH-
② 左(+)阳极:4H2O(OH-)-4e-=4H++O2↑+2H2O
右(- )阴极:2NO3-+6H2O+10e-= N2↑+12OH-
10 e- O2(左)- 1N2(右)-10H+
O2(左)- 1N2(右)-10H+
10mol  mol 1mol 10mol
mol 1mol 10mol
2mol 0.5mol 0.2mol 2mol
由于阴阳极之间被质子交换膜隔开,左侧电解产生的H+会穿过质子交换膜进入右侧,所以:
△m左=m(O2)+m(H+)=0.5mol×32g・mol-1+2mol×1g・mol-1="18g"
△m右= m(N2)-m(H+)=0.2mol×28g・mol-1-2mol×1g・mol-1=3.6g
△m左-△m右="18g-3.6g" = 14.4g
考点:电解原理及相关计算。
本题难度:一般
2、选择题 某学生设计了一个“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。据此,下列叙述正确的是
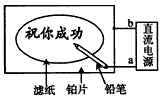
[? ]
A.铅笔端作阳极,发生还原反应
B.铂片端作阴极,发生氧化反应
C.铅笔端有少量的氯气产生
D.a点是负极,b点是正极
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列关于电解的说法中,正确的是
[? ]
A.电解池是把化学能转变为电能的装置
B.电解精炼铜时,粗铜板做阴极
C.电镀时,通常把待镀的金属制品做阴极
D.工业电解饱和食盐水用于生产金属钠和氯气
参考答案:C
本题解析:
本题难度:一般
4、简答题 工业上生产氯气,常用电解槽中电解饱和食盐水,为了避免电解产物之间发生反应,常用阳离子交换膜将电解槽隔成两部分.下图(左图)为电解槽的示意图.
(1)这种阳离子交换膜,只允许溶液中的______通过.(填下列微粒的编号)
①H2②Cl2③H+④Cl-⑤Na+⑥OH-
(2)写出在电解过程中阳极发生的电极方程式:______.
(3)已知某电解槽每小时加入10%的氢氧化钠溶液10kg,每小时能收集到标况下的氢气896L,而且两边的水不能自由流通.则理论上计算,电解后流出的氢氧化钠溶液的质量分数为______.
(4)某化学课外兴趣小组设计了用电解法制取乙醇钠的工业方法,所用的电解槽如图所示,设计要求:①所用的交换膜不能让分子自由通过;②电解过程中消耗的原料是氢氧化钠和乙醇.回答下列问题:
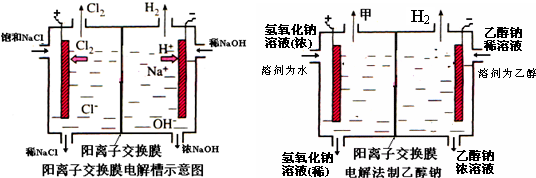
①写出在电解过程中阴极发生的电极方程式______.
②最后从乙醇钠的乙醇溶液中分离得到纯净乙醇钠固体的方法是:______.
参考答案:(1)阳离子交换膜只允许阳离子钠离子、氢离子通过,而阴离子和分子均不能通过,故答案为:③⑤;
(2)电解池中和电源的正极相连的是电解池的阳极,阳极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
(3)氢气的质量=VVmM=896L22.4L/mol×2g/mol=80g;电解水时,生成氢气与氢氧化钠的物质的量之比为1:2,所以生成氢氧化钠的质量=2896L22.4L/mol×40g/mol=3200g,溶液增加的质量为增加的钠元素的质量减去生成氢气的质量=2×896L22.4L/mol×23g/mol-80g=1760g;溶液中溶质氢氧化钠的质量为10000g×10%+3200g=4200g,溶液的质量为10000g+1760g=11760g,
电解后流出的氢氧化钠溶液的质量分数=4200g11760g×100%=35.7%,
故答案为:35.7%;
(4)①电解池中和电源的负极相连的是电解池的阴极,阴极上乙醇得电子发生还原反应,即2CH3CH2OH+2e-=2CH3CH2O-+H2↑.
故答案为:2CH3H2OH+2e-=2CH3CH2O-+H2↑;
?②从溶液中析出溶质的方法是蒸发结晶,故答案为:蒸发结晶.
本题解析:
本题难度:一般
5、判断题 若电解熔融的氢氧化钠,其有关的电极反应式及总反应式怎样?
参考答案:阳极:4OH-→2H2O +O2↑+4e-;阴极:4Na++ 4e-=? 4Na 。
⑵总反应式为:4NaOH ? ?4Na +2H2O +O2↑。
?4Na +2H2O +O2↑。
本题解析:熔融的氢氧化钠电离出Na+和OH-。OH-在电压的作用下定向向阳极移动,在阳极上发生氧化反应;而Na+定向向阴极移动,在阴极上发生还原反应。因此:
⑴电极反应式:阳极:4OH-→2H2O +O2↑+4e-;
阴极:4Na++ 4e-=? 4Na 。
⑵总反应式为:4NaOH ? ?4Na +2H2O +O2↑。
?4Na +2H2O +O2↑。
本题难度:一般