1、选择题 下列说法错误的是
[? ]
A.0.3 mol硫酸
B.1 mol水
C.0.5 mol钠
D.1.5 mol氧
参考答案:D
本题解析:
本题难度:简单
2、计算题 有14.0g Na2O和Na2O2的混合物,加足量的水使之充分反应,得到标况下气体的体积为1.12L。此时所得溶液的体积恰好为100mL,请计算:
(1)混合物中各组分的质量。
(2)所得溶液中溶质的物质的量浓度。
参考答案:(10分)
(1)m(Na2O)=6.2g(3分),m(Na2O2)=7.8g(3分)
(2)c(NaOH)=4.0mol/L(4分)
本题解析:(1)因为混合物中只有氢氧化钠与水反应产生氧气,利用氧气的体积计算过氧化钠的质量,从而计算氧化钠的质量。设混合物中过氧化钠的物质的量是x,标准状况下氧气的物质的量是1.12L/22.4L/mol=0.05mol,则
2Na2O2+2H2O=4NaOH+O2↑
1
x 0.05mol,
所以2:1=x:0.05mol,x=0.1mol,则Na2O2的质量是0.1mol×78g/mol=7.8g,所以Na2O的质量是14.0g-7.8g=6.2g;
(2)根据Na2O的质量可计算Na2O的物质的量是6.2g/62g/mol=0.1mol,与水反应后的溶液为NaOH溶液,根据Na元素守恒,NaOH的物质的量是(0.1mol+0.1mol) ×2=0.4mol,所以NaOH的物质的量浓度为0.4mol/0.1L=4.0mol/L。
考点:考查化学方程式的计算
本题难度:一般
3、选择题 设NA为阿伏加德罗常数,下列说法中正确的是(? )。
A.4mol浓盐酸与足量MnO2充分反应生成Cl2分子1NA
B.在25℃ 101kPa中,44.8 L14CO2中碳元素含有中子数16 NA
C.已知Fe3O4 + 4CO = 4CO2 + 3Fe,当生成168g Fe时转移的电子数是6NA
D.某中子数为18的34X2-微粒共1mol,其中共有电子数为 18NA
参考答案:D
本题解析:二氧化锰在和在浓盐酸的反应中,随着反应的进行,盐酸的浓度逐渐降低,而二氧化锰和稀盐酸不反应,所以选项A中实际生成的Cl2分子小于1NA,A不正确;B中CO2的体积不是在标准状况下,44.8 L14CO2的物质的量不是2mol,B不正确;四氧化三铁中铁元素的化合价是+8/3价,则选项C中当生成168g Fe时转移的电子数是8NA,C不正确;D中质子数+中子数=质量数,则该微粒的质子数是34-18=16,所以该微粒的电子数=16+2=18,因此选项D正确,答案选D。
点评:阿伏加德罗常数是历年高考的“热点”问题,这是由于它既考查了学生对物质的量、粒子数、质量、体积等与阿伏加德罗常数关系的理解,又可以涵盖多角度的化学知识内容。要准确解答好这类题目,一是要掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系;二是要准确弄清分子、原子、原子核内质子中子及核外电子的构成关系。
本题难度:一般
4、填空题 (3分)已知0.2mol的某气体的质量为16g,该气体的摩尔质量? ? ??g/mol,该气体在标况下的体积?L,该气体所含分子数? ?。(不必写出计算过程)
参考答案:80;4.48L;1.204×1023 (3分)
本题解析:M=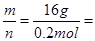 80 g/mol;
80 g/mol;
V=nVm=0.2mol×22.4L/mol=4.48L;
N=nNA=0.2mol×6.02×1023mol―mol=1.204×1023
本题难度:一般
5、选择题 .将5 mol・L-1盐酸10 mL稀释到200 mL,再取出5 mL,这5 mL溶液的物质的量浓度是
A.0.05 mol・L-1
B.0.25 mol・L-1
C.0.1 mol・L-1
D.0.5 mol・L-1
参考答案:B
本题解析:根据稀释定律有,5mol/L×10ml=c×200ml,c=0.25mol/L。
本题难度:简单