1��ѡ���� Ϊ�˽�һ���о�����ͭ�����������������ʵ�Ӱ�죬ijͬѧ��������һϵ��ʵ�顣�������������Լ���һ�������Ϻֱ�����ĸ�ʢ�й���Zn���ķ�Ӧƿ(�ס��ҡ�������)�У��ռ����������壬��¼�ռ���ͬ�������������ʱ�䡣
ʵ��
�Լ�/mL
| ��
| ��
| ��
| ��
|
4 mol/L H2SO4
| 20
| V1
| V2
| V3
|
����CuSO4��Һ
| 0
| 2.5
| V4
| 10
|
H2O
| V5
| V6
| 8
| 0
|
?
����˵����ȷ����? (����)
A��ʵ��ײ������ݵ��������?������ B��V1<V2<V3<20
C��V4��V5��10?������? D��V6��7.5
2������� �Ͼ�ӡˢ��·��Ļ������ÿ�ʵ����Դ��������������Ⱦ���Ͼ�ӡˢ��·�徭������룬�ܵõ��ǽ�����ĩ�ͽ�����ĩ��
��1�����д���ӡˢ��·��ǽ�����ĩ�ķ����У������ϻ��������������___________������ĸ����
A�����ѽ��γ�ȼ�� B��¶����� C����Ϊ�л����Ͻ������ϵ�ԭ�� D��ֱ������
��2����H2O2��H2SO4�Ļ����Һ���ܳ�ӡˢ��·�������ĩ�е�ͭ����֪��
Cu(s)��2H+(aq)=Cu2+(aq)��H2(g) ��H=64.39kJ��mol-1
2H2O2(l)=2H2O(l)��O2(g) ��H=��196.46kJ��mol-1
H2(g)��O2(g)=H2O(l) ��H=��285.84kJ��mol-1
��H2SO4��Һ��Cu��H2O2��Ӧ����Cu2+��H2O���Ȼ�ѧ����ʽΪ__________________��
��3����������������ͬ��ӡˢ��·��Ľ�����ĩ��10�GH2O2��3.0mol��L-1 H2SO4�Ļ����Һ��������ò�ͬ�¶���ͭ��ƽ���ܽ����ʣ����±�����

���¶ȸ���40��ʱ��ͭ��ƽ���ܽ��������ŷ�Ӧ�¶����߶��½�������Ҫԭ����__________________��
��4�����ᴿ���CuSO4��Һ�м���һ������Na2SO3��NaCl��Һ�����ȣ�����CuCl�������Ʊ�CuCl�����ӷ���ʽ��___________________________��
3��ʵ���� �������������ϡ����ķ�ӦΪ��Na2S2O3��H2SO4��Na2SO4��S����SO2����H2O��ijʵ����ȤС��������ͼ��ʾ��ʵ��װ��̽����������Ի�ѧ��Ӧ���ʵ�Ӱ��(���������ͼг���������ʡ��)
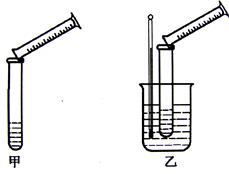
��1��ʵ��Ŀ�ģ�
װ�üף�̽��Ũ�ȶԻ�ѧ��Ӧ���ʵ�Ӱ�죻װ���ң�̽�� �Ի�ѧ��Ӧ���ʵ�Ӱ�졣
��2��װ�����еļ��ȷ�����Ϊ ���ȣ��ü��ȷ������� ��
���ŵ㡣
��3��ͨ���ס���װ�ã��ֱ����������ʵ�飬���ݼ�¼���£����������ó���ؽ��ۣ�
ʵ�����
| �¶�
| Na2S2O3
| H2SO4
| ����H2O
�����
| ���ֳ���
����ʱ��
|
���
| Ũ��
| ���
| Ũ��
|
��
| 0OC
| 5mL
| 0.1mol/L
| 10mL
| 0.1mol/L
| 5mL
| 8s
|
��
| 0OC
| 5mL
| 0.1mol/L
| 5mL
| 0.1mol/L
| 10mL
| 12s
|
��
| 30OC
| 5mL
| 0.1mol/L
| 5mL
| 0.1mol/L
| 10mL
| 4s
|
��
| 30OC
| 5mL
| 0.2mol/L
| 5mL
| 0.2mol/L
| 10mL
| 2s
|
����1�� ��
����2�� ��
4��ѡ���� ������ƽ����ϵ�У������¶�һ��ʱ���ı�ij���ʵ�Ũ�ȣ�����������ɫ��ı䣻�ı�ѹǿʱ����ɫҲ��ı䣬��ƽ�Ⲣ���ƶ��������Ӧ�ǣ�?��
A��2NO��O2  2NO2
2NO2
B��N2O4 2NO2
2NO2
C��Br2(g)��H2 2HBr
2HBr
D��6NO��4NH3 5N2��3H2O
5N2��3H2O
5��ѡ���� ���и��鷴Ӧ���������ʾ�Ϊ��Ӧ��տ�ʼʱ���ų�H2����������
���
| ��������ĩ״��
| ���ʵ���
| ���Ũ��
| ������
| ��Ӧ�¶�
|
A
| Al
| 0.1 mol
| 18.4 mol/L H2SO4
| 10 mL
| 60 ��
|
B
| Mg
| 0.1 mol
| 3 mol/L HCl
| 10 mL
| 30 ��
|
C
| Fe
| 0.1 mol
| 3 mol/L H2SO4
| 10 mL
| 60 ��
|
D
| Mg
| 0.1 mol
| 3 mol/L H2SO4
| 10 mL
| 60 ��
|