1、选择题 某温度下,将Cl2通入KOH溶液中得KCl、KClO3和 KClO的混合溶液。经测定ClO3-和ClO-物质的量之比为2:1,则反应中被还原的Cl2与被氧化Cl2的物质的量之比为?
[? ]
A.2:3
B.3:4
C.11:3
D.10:3
参考答案:C
本题解析:
本题难度:一般
2、填空题 按下图装置进行实验,并回答下列问题
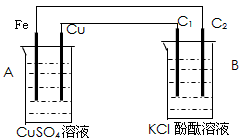
(1)判断装置的名称:A池为___________ B池为___________
(2)铁极为__________极,电极反应式为________________________石墨棒C2附近发生的实验现象为
______________________________
(3)当C2极产生2.24L气体(标准状态)时,铁的质量变化(增加或减少)____了 ____g.CuSO4溶液的质量变化(增加或减少)____ 了____g
参考答案:(1)原电池;电解池
(2)负;Fe-2e-==Fe2+;无色溶液变红色
(3)减少;5.6;减少;0.8
本题解析:
本题难度:一般
3、选择题 向含有Fe2+、I-、Br-的溶液中通入适量氯气,溶液中各种离子的物质的量变化如下图所示。有关说法不正确的是
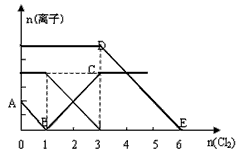
[? ]
A.线段BC代表Fe3+ 物质的量的变化情况
B.原混合溶液中 c(FeBr2)= 6mol/L
C.当通入Cl2 2mol时,溶液中已发生的离子反应可表示为:
2Fe2++2I-+2Cl2==2Fe3++I2+4Cl-
D.原溶液中n(Fe2+): n(I-): n(Br-)=2:1:3
参考答案:B
本题解析:
本题难度:一般
4、选择题 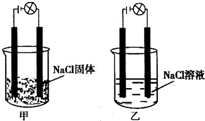 某化学兴趣小组在家中进行化学实验,按照图甲连接好线路后发现灯泡不亮,按照图乙连接好线路后发现灯泡亮,由此得出的结论正确的是
某化学兴趣小组在家中进行化学实验,按照图甲连接好线路后发现灯泡不亮,按照图乙连接好线路后发现灯泡亮,由此得出的结论正确的是
A.NaCl是非电解质
B.NaCl溶液是电解质
C.NaCl是弱电解质
D.NaCl在水溶液中电离出了可以自由移动的离子
参考答案:D
本题解析:分析:按照图甲连接好线路后发现灯泡不亮,说明无自由移动的离子存在,按照图乙连接好线路后发现灯泡亮,说明存在自由移动的离子存在;导电的实质是含有自由移动的离子在外加电源作用下定向移动;电解质是溶于水或熔融状态导电的化合物,弱电解质是电解质在水溶液中部分电离的电解质;
解答:A、氯化钠熔融状态或溶于水能导电,符合电解质概念是电解质,故A错误;
B、氯化钠溶液是混合物,不是电解质,是电解质溶液,故B错误;
C、氯化钠水溶液中完全电离,是强电解质,故C错误;
D、实验表明,NaCl在水溶液中电离出了可以自由移动的离子,溶液导电,故D正确;
故选D.
点评:本题考查溶液导电实质,电解质概念分析判断,掌握基础是关键,题目较简单.
本题难度:简单
5、选择题 根据反应方程式① 2Fe3+ +2I-? ==2Fe2+ + I2?② 2Fe2+ +Br2 == 2Fe3+ +2Br-? ,可判断离子的还原性从强到弱的顺序正确的是
A.Br->Fe2+>I-
B.I- >Fe2+ >Br-
C.Br- >I- >Fe2+
D.Fe2+ >I- >Br-
参考答案:B
本题解析:已知在氧化还原反应中,还原剂的还原性大于还原产物。由①知还原性I- >Fe2+,由②知Fe2+ >Br-,故还原性I- >Fe2+ >Br-。答案选B。
本题难度:困难