1、选择题 下列有关溶液中微粒的物质的量浓度关系正确的是 (? )
A.1L0.1mol・L-1(NH4)2Fe(SO4)2溶液: c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-)
B.25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中:
c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-)
C.25℃时,BaCO3饱和溶液(Ksp =8.1×10-9): c(Ba2+)= c(CO32-)>c(H+) = c(OH-)
D.1.0 mol・L-1 Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
参考答案:AD
本题解析:A、1L0.1mol・L-1(NH4)2Fe(SO4)2溶液中铵根离子浓度大于亚铁离子浓度水解显酸性得到溶液中离子浓度大小为:c(SO42-)>c(NH4+)>c(Fe2+)>c(H+)>c(OH-),故A正确;
B、25℃时,等体积、等浓度的NaX和弱酸HX混合后的溶液中,无法判断酸的电离程度和阴离子的水解程度,不能比较离子浓度大小,故B错误;
C、25℃时,BaCO3饱和溶液(Ksp=8.1×10-9)中碳酸根离子水解溶液中的离子浓度爱心为:c(Ba2+)>c(CO32-)>c(OH-)>c(H+),故C错误;
D、1.0 mol・L-1 Na2CO3溶液中依据水电离出的全部氢离子和氢氧根离子守恒分析得到:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故D正确;
故选AD.
本题难度:一般
2、选择题 下列各组离子中,一定能大量共存的是?(?)?
A.加入铝粉只有氢气产生的溶液中:Na+、SO42-、NO3-、Mg2+、
B.滴加石蕊试液显红色的溶液中:Fe3+、NH4+、Cl-、SCN-
C.在0.1mol/L的NaHSO4溶液中:NH4+、Na+、Al3+、Cu2+、NO3-
D.在0.1mol/L的NaHCO3溶液中K+、Al3+、Fe3+、NO3-
参考答案:C
本题解析:略
本题难度:简单
3、选择题 下列叙述正确的是(? )
A.饱和的食盐水中通入HCl气体会有白色晶体析出
B.同浓度的(NH4)2SO4、(NH4)2CO3、NH4Cl、NH4HSO4溶液中,c(NH4+)逐渐减小
C.加入盐酸出现白色沉淀,则原溶液中一定含Ag+
D.既能溶解Al(OH)3又能溶解H2SiO3的溶液可以大量共存NO3-、HCO3-、I-、K+
参考答案:A
本题解析:A、该溶液中存在沉淀溶解平衡,NaCl(s)  Na+(aq)+Cl-(aq),通入HCl,氯离子浓度增加,平衡逆向移动,析出NaCl固体,正确;B、NH4HSO4中,溶液呈酸性,抑制了其水解,故浓度大于NH4Cl中浓度,错误;C、不一定,如硅酸根与氢离子结合生成硅酸白色沉淀,错误;D、该溶液为碱性溶液,碳酸氢根不能大量共存,错误。
Na+(aq)+Cl-(aq),通入HCl,氯离子浓度增加,平衡逆向移动,析出NaCl固体,正确;B、NH4HSO4中,溶液呈酸性,抑制了其水解,故浓度大于NH4Cl中浓度,错误;C、不一定,如硅酸根与氢离子结合生成硅酸白色沉淀,错误;D、该溶液为碱性溶液,碳酸氢根不能大量共存,错误。
本题难度:一般
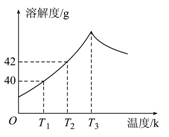
4、选择题 下图为Na2SO4的溶解度曲线,已知硫酸钠晶体(Na2SO4・10H2O)在温度为T3 K 时开始分解为无水硫酸钠。现有142 g温度为T2 ?K的饱和硫酸钠溶液,当温度降为T1 K或升为T4 K(T4>T3)时析出晶体的质量相等,则温度为T4 K时Na2SO4的溶解度为
A.小于40g
B.等于40g
C.等于42g
D.大于42g
参考答案:A
本题解析:根据图像易得:142g温度为T2 K的饱和硫酸钠溶液中,溶质有42g,水有100g
降到T1时,溶解度是40g,就是说有2gNa2SO4多余,但析出Na2SO4?10H2O质量肯定要大于2g(含结晶水);
而在T4时析出的晶体是无水硫酸钠,析出的Na2SO4质量大于2g。所以温度为T4 K时,100g水中所含Na2SO4的质量必定小于40g
本题难度:一般
5、选择题 向NaHSO3溶液中加入足量Na2O2粉末,充分反应后溶液中离子浓度减少的是(忽略溶液体积变化)
A.Na+
B.SO32-
C.OH-
D.SO42-
参考答案:B
本题解析:向溶液中加入Na2O2,与水反应生成NaOH,Na+和OH-增加;同时过氧化钠具有强氧化性,亚硫酸氢钠被氧化成SO42-,则SO32-减少了,SO42-增大,答案选B。
本题难度:一般