1、选择题 下列试剂中,可用于鉴别FeCl2溶液和FeCl3溶液的是
A.KCl
B.KNO3
C.KSCN
D.K2SO4
参考答案:C
本题解析:FeCl2溶液遇到KSCN没变化, FeCl3溶液遇到KSCN变红色,故选C。
点评:本题考查的是亚铁离子(Fe2+)和铁离子(Fe3+)的区别,利用铁离子(Fe3+)遇到KSCN变红色的特征反应及现象进行鉴别。考查的内容源自于课本。
本题难度:一般
2、填空题 现有Fe、Cu组成的合金,其中Cu、Fe的总物质的量为a mol,Cu的物质的量分数为x;研成粉末后,全部投入含b mol HNO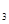 的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
的稀溶液中,微热使其充分反应,且硝酸的还原产物只有NO,试回答下列问题:
(1)若剩余的残渣只有Cu,则溶液中含有的金属离子为__________。(写出所有可能情况)
(2)当溶液中金属离子只有Fe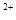 、Cu
、Cu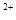 时,则b的取值范围是(用a、x表示)___________。
时,则b的取值范围是(用a、x表示)___________。
(3)当x=0.5,溶液中Fe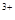 与Fe
与Fe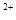 的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
的物质的量相等时,在标准状况下共产生672 mL气体。则a=____________、b=_____________。
参考答案:(1)? Fe2+或Fe2+、Cu2+ (2分)
(2) 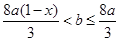 ?(2分)
?(2分)
(3)? a=0.04mol? b=0.12mol (2分)
本题解析:(1) Cu、Fe的混合物与稀硝酸反应,金属可能有剩余,可能没有剩余.金属可能有剩余时,根据共存可知,剩余金属有两种情况:
①剩余Fe、Cu,当有Fe剩余时,溶液中能与Fe反应的Fe3+、Cu2+都不存在,所以溶液中只有Fe2+;
②只剩余Cu,溶液中一定不存在与Cu反应的Fe3+,根据离子共存,溶液可能只有Fe2+;
③通过②知,溶液中还可能存在的离子是Fe2+、Cu2+;
④当固体没有剩余时,可能存在的情况是:当Fe恰好与硝酸反应生成Fe2+,Cu恰好与硝酸生成Cu2+,所以溶液中存在的离子是Fe2+、Cu2+;
⑤通过④知,固体没有剩余时,生成的Fe3+部分反应,根据离子共存,溶液中存在的离子可能的Fe2+、Fe3+、Cu2+;
⑥通过④、⑤知,固体没有剩余时,铁、铜全部被氧化成离子,根据离子共存,溶液中存在的离子可能是Cu2+、Fe3+;
有如下情况:
残留固体成分
Fe、Cu
Cu
Cu
--
--
__
溶液中的金属离子
Fe2+
Fe2+
Fe2+、Cu2+
Fe2+、Cu2+
Fe2+、Fe3+、Cu2+
Cu2+、Fe3+
?
(2)当溶液金属离子只有Fe2+、Cu2+时,说明Cu恰好完全反应或者有剩余,而HNO3和Fe则完全反应(否则的话,如果有硝酸剩余,则Fe2+则会被进一步氧化为Fe3+;如果有Fe剩余,则会和Cu2+继续反应)
3Cu+8HNO3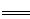 3Cu(NO3)2+2NO↑+4H2O
3Cu(NO3)2+2NO↑+4H2O
ax?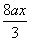
3Fe? +? 8HNO3 3Fe(NO3)2+2NO↑+ 4H2O?
3Fe(NO3)2+2NO↑+ 4H2O?
a(1-x)?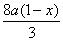
总耗用硝酸量:n(HNO3)=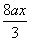 +
+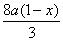 ?=
?=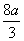
所以: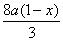 <b≤
<b≤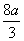
(3)当溶液中为Fe3+、Fe2+时,说明Cu、Fe完全反应(如果未完全反应,则Cu和Fe会和Fe3+反应),并且HNO3也完全反应没有剩余(如果有硝酸剩余,则Fe2+则会被进一步氧化为Fe3+)溶液中Fe3+、Fe2+的物质的量相等,说明有一半Fe变为Fe3+,一半变为Fe2+
当x=0.5,nFe3+=nFe2+? V(NO)=0.672L
则nFe3+=nFe2+="0.25a" mol? nCu = 0.5amol
此时3Fe+8HNO3 3Fe(NO3)2+2NO↑+4H2O?①
3Fe(NO3)2+2NO↑+4H2O?①
3Cu+8HNO3 3 Cu (NO3)2+2NO+4H2O?②
3 Cu (NO3)2+2NO+4H2O?②
3Fe(NO3)2+4HNO3 3Fe(NO3)3+NO+2H2O?③
3Fe(NO3)3+NO+2H2O?③
反应均发生了,且无反应物剩余。
3Fe?+? 8HNO3 3Fe(NO3)2+2NO↑+4H2O?①?
3Fe(NO3)2+2NO↑+4H2O?①?
0.5a? 0.5a×8/3? 0.5a? 0.5a×2/3
3Cu+8HNO3? ?3 Cu (NO3)2+2NO↑+4H2O?②?
?3 Cu (NO3)2+2NO↑+4H2O?②?
0.5a? 0.5a×8/3? 0.5a? 0.5a×2/3?
3Fe(NO3)2+4HNO3 ?3Fe(NO3)3+NO+2H2O?③
?3Fe(NO3)3+NO+2H2O?③
0.25a? 0.25a ×4/3? 0.25a
0.5a×2/3 +0.5a×2/3 + 0.25a×1/3 =0.672L/22.4L・mol-1=0.03mol
解得:a="0.04" mol?
b=" 0.5a×8/3" + 0.5a×8/3+0.25a ×4/3="3a=3×0.04" mol ="0.12" mol
本题难度:一般
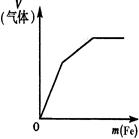
3、选择题 下列反应中,相关示意图像错误的是(?)
A
| B
| C
| D
|
将二氧化硫通入到一定量氯水中
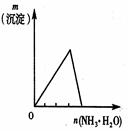
| 将氨水滴入到一定量氯化铝溶液中
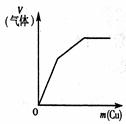
| 常温下将铜粉加入到一定量浓硝酸中
| 常温下将铁粉加入到一定量浓硝酸中
|

| 
| 
| 
|
?
参考答案:BD
本题解析:略
本题难度:简单
4、填空题 [化学――选修化学与生活](15分)
(Ⅰ)合金是生活中常用的材料,请回答下列问题:
(1)生铁和钢是含碳量不同的铁碳合金,含碳量在2%~4.3%的称为?。不锈钢在空气中比较稳定,不易生锈,有强的抗腐蚀能力,其合金元素主要是?;?(2)钢铁的腐蚀给社会造成的损失是巨大的,所以采取各种措施防止钢铁的腐蚀是十分必要的,请列举三种防止钢铁腐蚀的方法?;?
(3)青铜的主要合金元素为?,黄铜的主要合金元素为?:
(4)储氢合金是一类能够大量吸收氢气,并与氢气结合成金属氢化物的材料。如镧镍合金,它吸收氢气可结合成金属氢化物,其化学式可近似地表示为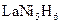 ?(
?(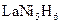 中各元素化合价均可看作是零),它跟
中各元素化合价均可看作是零),它跟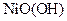 可组成镍氢可充电电池:
可组成镍氢可充电电池:
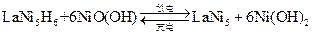
该电池放电时,负极反应是??。市面上出售的标称容量为2000 mA h的1节镍氢电池至少应含有镧镍合金??g(已知1法拉第电量为96500库仑或安培・秒)。
(Ⅱ)有机化合物与生活息息相关。请回答下列有关问题:
(1)棉花、蚕丝、小麦主要成分分别为?、?、?,它们蕃都属于天然有机高分子化合物;
(2)味精是烹饪常用的调味品,其主要成分的化学名称为?;?
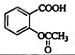
(3)解热镇痛药阿司匹林主要成分的结构简式为?。
参考答案:
(I)
(1)生铁,铬和镍
(2)在钢铁的表面喷涂油漆;在钢铁的表面镀上铬、锌等金属;对钢铁的表面进行发蓝处理;在钢铁器件上附着一种更易失电子的金属或合金。
(3)Sn? Zn
(4)LaNi5H6 + 6OH- - 6e- =LaNi5 + 6H2O;5.4
(II)
(1)纤维素、蛋白质、淀粉
(2)谷氨酸单钠盐(或2-氨基戊二酸单钠盐)
(3)
本题解析:略
本题难度:简单
5、推断题 已知有以下物质相互转化
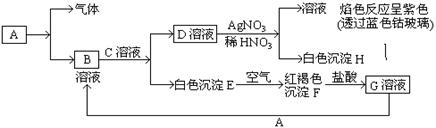
试回答:(1)写出B的化学式?,D的化学式?。
(2)写出由E转变成F的化学方程式?。
(3)写出用KSCN鉴别G溶液的实验现象是?;向G溶液加入A的有关离子反应方程式?。
参考答案:(1)FeCl2? KCl?(2)4Fe(OH)2+O2+2H2O=4Fe(OH)3
(3)出现血红色溶液? 2Fe3++Fe=3Fe2+
本题解析:红褐色沉淀F是氢氧化铁、E为氢氧化亚铁、G为氯化铁;D溶液与硝酸银溶液生成白色沉淀H为氯化银,滤液焰色反应呈紫色(透过蓝色钴玻璃)说明滤液中含有K+,所以D为KCl,逆推B和C应为氯化亚铁和氢氧化钾,FeCl3溶液与A生成B溶液,所以B为氯化亚铁,A为铁。检验氯化铁溶液中Fe3+用KSCN溶液,氯化铁溶液中加入铁生成氯化亚铁溶液。
点评:无机推断题要找准题眼,如本题中的红褐色沉淀为氢氧化铁、白色沉淀在空气中转化为氢氧化铁的反应为4Fe(OH)2+O2+2H2O=4Fe(OH)3。
本题难度:一般