1��ѡ���� ������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ����ͼ��ʾ�������л�ѧ��Ӧ��������3����

A��4Fe(OH)2��O2��2H2O=4Fe(OH)3
B��2KMnO4 K2MnO4��MnO2��O2��
K2MnO4��MnO2��O2��
C��4NH3��5O2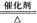 4NO��6H2O
4NO��6H2O
D��Fe��CuSO4=FeSO4��Cu
�ο��𰸣�C
���������4Fe(OH)2+O2+2H2O�T4Fe(OH)3Ϊ���Ϸ�Ӧ������������ԭ��Ӧ��Ϊ����1����A����B��2KMnO4 K2MnO4��MnO2��O2��Ϊ�ֽⷴӦ������������ԭ��Ӧ��Ϊ����2����B����C��4NH3��5O2
K2MnO4��MnO2��O2��Ϊ�ֽⷴӦ������������ԭ��Ӧ��Ϊ����2����B����C��4NH3��5O2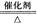 4NO��6H2O��������3��������ԭ��Ӧ����C��ȷ��D��Fe��CuSO4=FeSO4��CuΪ�û���Ӧ������������ԭ��Ӧ��Ϊ����4����D����
4NO��6H2O��������3��������ԭ��Ӧ����C��ȷ��D��Fe��CuSO4=FeSO4��CuΪ�û���Ӧ������������ԭ��Ӧ��Ϊ����4����D����
�����Ѷȣ�һ��
2��ѡ���� ���л�ѧ����˵����ȷ����
A�����ĵ���ʽ��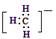
B����ϩ�ı���ģ�ͣ�
C��������Ϊ53��������Ϊ78�ĵ�ԭ�ӣ�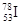
D��������Ľṹʽ��H��O��Cl
�ο��𰸣�D
���������A����������ɣ�����ʽΪ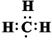 ��A����ȷ��B����ģ������ϩ�����ģ�ͣ�B����ȷ��C���ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮��������������������Ϊ53��������Ϊ78�ĵ�ԭ�ӱ�ʾΪ
��A����ȷ��B����ģ������ϩ�����ģ�ͣ�B����ȷ��C���ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮��������������������Ϊ53��������Ϊ78�ĵ�ԭ�ӱ�ʾΪ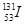 ��C����ȷ��D��������ĵ���ʽΪ
��C����ȷ��D��������ĵ���ʽΪ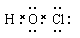 ����ṹʽΪH��O��Cl��D��ȷ����ѡD��
����ṹʽΪH��O��Cl��D��ȷ����ѡD��
�����Ѷȣ�һ��
3��ѡ���� ���б����뻯ѧ������ȷ����(����)
A��CO2�ı���ģ��
B���⻯淋ĵ���ʽ��[H��N?,?H,H ��H]��H��
C��CH3��CH��CH��CH��CH2CH3CH3C2H5CH3�����ƣ�2��3?����?4?�һ�����
D����������ķ���ʽSiO2
�ο��𰸣�C
���������̼ԭ�Ӱ뾶������ԭ�ӣ�A�����B����û���H���ĵ��ӣ�����������ΪSiԭ�Ӻ�Oԭ�Ӱ���ԭ�Ӹ�����Ϊ1��Դ:91 ��������2��ɵĿռ���״�ṹ�������ڷ��ӣ�D�����
�����Ѷȣ�һ��
4��ѡ���� ���б仯�����������������ɵ���
A��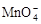
 MnO2
MnO2
B��
 CO2
CO2
C��S2�� HS��
HS��
D��Br�� Br2
Br2
�ο��𰸣�D
����������������ڷ�Ӧ�еõ����ӣ����ϼ۽��͡������������������ɣ�˵�������ǻ�ԭ����Ԫ�صĻ��ϼ����ߣ����Դ�ѡD��
������������Ҫע�������Щ���ʿ�����������������ԭ��Ӧ��������Ҫ�ټ�����������ԭ����
�����Ѷȣ�һ��
5������� ij�л���A��һ����Ҫ�м��壮
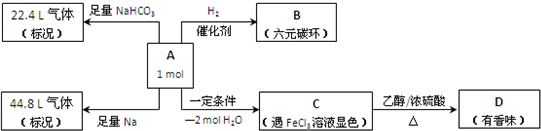
��1����֪�л���A����Է�������������180������A��ȫȼ�գ�ֻ����CO2��H2O����n��CO2����n��H2O��=7��5����Ӧ�����ĵ�O2�����ɵ�CO2�����ʵ�����ȣ��л���A�ķ���ʽΪ______��
��2�������л���A����NaHCO3��Ӧ�ų����壬��֪A�����к��еĹ����ŵ�������______��
��3���л���A���������ĸ����ڵ�ȡ��������̼̼˫���Ͻ��ǻ�ʱ������һ��̼ԭ����ͬʱ����2����2�������ǻ�ʱ�����ȶ����ڣ���֪C���ӵ�̼���ϵ�һ��ȡ����ֻ�����ֽṹ����B�Ľṹ��ʽΪ______��
��4��д�����з�Ӧ�Ļ�ѧ����ʽ��
��A+NaHCO3����������______��
��CD��______��
��5��C��ͬ���칹���У���������ȡ�������칹�干��______�֣���д������һ�ֵĽṹ��ʽ______��
�ο��𰸣���1��A��ȫȼ�գ�ֻ����CO2��H2O����n��CO2����n��H2O��=7��5������C��H�ĸ���֮���ǣ�7��10������ΪA���ӵ���Է�������������180���������ĵ�O2�����ɵ�CO2�����ʵ�����ȣ���1molA��������7mol������ȷ������ʽΪC7H10O5���ʴ�Ϊ��C7H10O5��
��2������NaHCO3��Ӧ�ų�����������������ʣ�����A�����к��еĹ��������Ȼ����ʴ�Ϊ���Ȼ���
��3���л���A���������ĸ����ڵ�ȡ������������ȥ��Ӧʧȥ2��ˮ���Ӻ��C��̼���ϵ�һ��ȡ����ֻ�����ֽṹ������AΪ
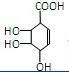
��C��
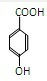
������B��

���ʴ�Ϊ��

��
��4��A

�к����Ȼ������Ժ�NaHCO3����������Ӧ��ʵ���ǣ�
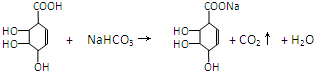
��C

�к����Ȼ������Ժʹ�����������Ӧ����
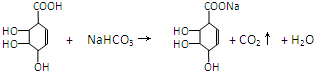
���ʴ�Ϊ��
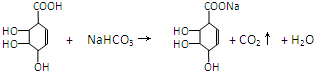
��
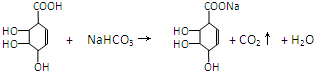
��
��5��

�е��Ȼ����ǻ�ȩ��Ϊͬ���칹�壬���Խ��Ȼ���Ϊȩ�����ǻ�����������ȡ�������칹�干��
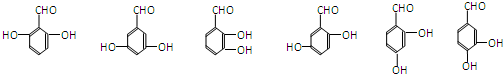
���֣��ʴ�Ϊ��6��

��
���������
�����Ѷȣ�һ��