1、选择题 短周期主族元素A、B、C、D原子序数依次增大。已知:A、C的原子序数的差为
8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最
外层电子数的一半。下列叙述正确的是
A.原子半径:A< D< B < C
B.A的氢化物稳定性大于C的氢化物稳定性
C.A在自然界中只能以化合态形式存在
D.D的单质可使干燥的红色布条褪色
参考答案:B
本题解析:A、C的原子序数的差为8,说明两元素同族,最外层电子数相等
设B的最外层电子数为x,则A与C元素的最外层电子数均为2x,则2x+2x+x=15,得x=3,说明AC分别为第VIA族的O、S元素,而B为Al元素,D只能为Cl元素
A:四元素中铝元素的层数最多且核电荷数最小,故铝的半径最大,排除
B:O的非金属性较S强,氢化物稳定性相对较强,正确
C:氧气就是氧元素的游离状态,不正确
D:干燥的氯气并没有漂白性,排除
答案为B
本题难度:一般
2、选择题 下列关于铷(Rb)的叙述正确的是
A.它位于周期表的第四周期第ⅠA族
B.氢氧化铷是强碱
C.在钠、钾、铷3种单质中,铷的熔点最低
D.碳酸铷不溶于水
参考答案:BC
本题解析:略
本题难度:简单
3、推断题 由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图的转化关系,已知C为密度最小的气体,甲为非电解质。
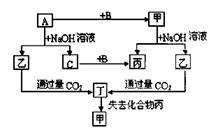
根据以上转化关系回答下列问题:
(1)写出下列物质的化学式:A ?B?丁?。
(2)元素A在周期表中的位置是?,写出甲的一种用 途?。
(3)写出下列变化的方程式:
A与NaOH溶液反应的化学方程式?。
乙与过量CO?2反应的离子方程式?。
参考答案:
(1)Si(2分)? O2(2分)? H2SiO3或H4SiO4(2分)
(2)第三周期第ⅣA族(2分)?是玻璃、光导纤维等(2分)
(3) ①Si+2NaOH+H2O=Na2SiO3+2H2↑(2分)
② SiO32―+2CO?2+2H2O=H2SiO3↓+2HCO3―(2分)
本题解析:根据题意可知A:SiB:O2、C:H2、甲:SiO2、乙:Na2SiO3、丙:H2O、丁:H2SiO3。
(1)突破口:C为密度最小的气体,知C是H2;甲为非电解质,不能是Al2O3,只能是SiO2;则A为Si、B为O2、 乙是Na2SiO3,通CO?2生成丁,丁为H2SiO3。丁失去丙生成甲,丙为H2O。
(2)A为Si,在周期表的第三周期第ⅣA族;用途是做玻璃、光导
本题难度:一般
4、选择题 A、B、C均为短周期元素,A、B同周期, A、C的最低价离子分别为A2-和C-,B2+ 和C-具有相同的电子层结构,下列说法中正确的是
A. C元素的最高正价为+7价? B.原子半径:A>B>C
C.离子半径:A2->C->B2+? ? D.还原性:A2-<C-
参考答案:C
本题解析:
正确答案:C
A、不正确,如是F,无正价;B、不正确,原子半径:B>A>C
C、正确;电子层结构相同时,原子序数大的半径小;
D、不正确,还原性:A2->C-
本题难度:一般
5、填空题 (10分)下表是元素周期表的一部分,表中所列的字母分别代表某一元素。
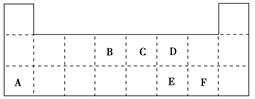
(1)1 mol A与足量D的氢化物完全反应产生的气体在标准状况下的体积为________L。
(2)写出B的最高价氧化物的电子式________。
(3)表中的另一种金属元素(未标出)的单质G,可以发生如下图所示转化:
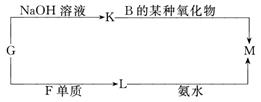
其中化合物M是一种白色胶状沉淀,则M为(填化学式)________________;
K的溶液与B的某种氧化物反应的化学方程式为____________________________;
一种新型无机非金属材料由G元素和C元素组成,其化学式为____________。
参考答案:(10分)(1)? 11.2 L(2分) ? (2) 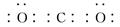 (2分)
(2分)
(3)Al(OH)3(2分) ? NaAlO2+CO2+2H2O===Al(OH)3↓+NaHCO3(2分)
(或2NaAlO2+CO2+3H2O===2Al(OH)3↓+Na2CO3) ? AlN(2分)
本题解析:依次可知为钠、碳、氮、氧、硫、氯
2Na+2H2O=2NaOH+H2↑ 氧化物为CO2,G为铝,2NaAlO2+CO2+3H2O===2Al(OH)3↓+Na2CO3
本题难度:一般