| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
���л�ѧ֪ʶ���ܽᡶ�����Ļ�ѧ��Դ������Ԥ�⣨2019��ǿ���棩(ʮ)
�ο��𰸣�B ������������ŵ�ʱ�������缫��Ӧ��ӿɵ�:Pb+PbO2+2H2SO4 �����Ѷȣ�һ�� 2��ѡ���� ȼ�ϵ����ȼ�ϣ�����CO��H2��CH4�ȣ��������������Ӧ�����˷�Ӧ�Ļ�ѧ��ת��Ϊ���ܵ�װ�ã��������Һͨ����KOH��Һ�����й��ڼ���ȼ�ϵ�ص�˵��������ǣ������� �ο��𰸣�A��ȼ���ڸ�����ʧ���ӷ���������Ӧ������ȼ�������ɶ�����̼��ˮ��������̼���������ط�Ӧ����̼��أ����Ե缫��ӦʽΪ��CH4+10OH--8e-�TCO32-+7H2O����A��ȷ�� ��������� �����Ѷȣ��� 3��ѡ���� ��ѧ��������N2��H2Ϊ��Ӧ�������A��ϡ����Ϊ�������Һ��������������ṩ���ܣ����̵ܹ�������ȼ�ϵ�أ�װ������ͼ��ʾ������˵������ȷ���� |
�ο��𰸣�C
���������A.�õ�صı����Ǻϳɰ���Ӧ�����������ǵ���������ԭ��Ӧ���缫��ӦʽΪN2 + 6e- + 8H+=2NH4+����ȷ��B.��Ӧ�����У�H���������ĵ���PHֵ�����Ҫ�������ᣬ��ȷ��C.��װ����ԭ���װ�ã�����������ͨ�����·����������ͨ�뵪���ĵ缫�����·����ͨ�������ĵ缫������D.ͨ�������ĵ缫Ϊ���������ɵ�笠��������Ȼ����������Ȼ�泥�����A��NH4Cl����ȷ��ѡC��
���㣺��������ȼ�ϵ�صĹ���ԭ����
�����Ѷȣ�һ��
4������� ������Ƴɺϳ�����CO��H2�������Ƴɼ״����������湩Ӧ���ŵ�ȼ�͡�
��֪����CH4 (g) �� H2O (g)= CO (g)��3H2 (g) ��H1=+206.2kJ��mol��1
�� CH4��g���� O2��g��=CO��g����2H2��g�� ��H2=��35.4 kJ��mol��1
O2��g��=CO��g����2H2��g�� ��H2=��35.4 kJ��mol��1
��CH4 (g) �� 2H2O (g) =CO2 (g) ��4H2 (g) ��H3="+165.0" kJ��mol��1
��1��CH4(g)��CO2 (g)��Ӧ����CO(g)��H2(g)���Ȼ�ѧ����ʽΪ ��
��2����ԭ��ѡ�����Դ���ýǶȣ��ȽϷ����ٺ͢ڣ�Ϊ�ϳɼ״����ü����ƺϳ��������˷���Ϊ ������ţ�����ԭ���� ��
��3���ϳ����е�H2����������NH3���ڽ���ϳ���ǰ����Cu(NH3)2Ac��Һ���������е�CO����ֹ�ϳ����еĴ����ж����䷴Ӧ�ǣ�
Cu(NH3)2Ac + CO + NH3 [Cu(NH3)3]Ac��CO ��H��0
[Cu(NH3)3]Ac��CO ��H��0
Cu(NH3)2Ac��Һ����CO��������������Ӧ�� ��
��4����CH4��Ƴ�ȼ�ϵ�أ��������ʸ��ߣ�װ��ʾ������ͼ��A��BΪ�����̼����������ͨ����飬�ڱ�״���£����ļ������VL��
�� 0<V��44.8 Lʱ������ܷ�Ӧ����ʽΪ ��
�� 44.8 L<V��89.6 Lʱ�������缫��ӦΪ ��
�� V="67.2" Lʱ����Һ������Ũ�ȴ�С��ϵΪ ��
�ο��𰸣���14�֣���1��CH4 (g)+CO2 (g)=2CO (g)+2H2 (g) ��H="+247.4" kJ��mol��1��2�֣�
��2���ڣ�2�֣� ѡ��CH4����ȫȼ���ƺϳ���ʱ���ų�������ͬʱ�õ���CO��H2���ʵ���֮��Ϊ1��2����ǡ����ȫ��Ӧ�ϳɼ״���2�֣�
��3�����¡���ѹ��2�֣�
��4����CH4 +2O2 +2KOH=K2CO3+3H2O��2�֣�
��CH4��8e��+ 9CO32��+3H2O=10HCO3����2�֣�
��c(K��)��c(HCO3��)��c(CO32��)��c(OH��)��c(H+) ��2�֣�
�����������1�����ݸ�˹���ɣ��١�2���ۿ�ԼȥH2O(g)����CH4(g)+CO2 (g)=2CO(g)+2H2(g)�ġ�H=�ٵġ�H��2���۵ġ�H=[��+206.2����2����+165.0��] kJ��mol��1="+247.4" kJ��mol��1����2���������ǶȱȽϣ��������ȷ�Ӧ����Ҫ���ĸ������������Ƿ��ȷ�Ӧ������Ҫ̫����������ԭ�������ʽǶȣ�����CO+2H2��CH3OH���ٵIJ�������ԭ�Ӳ�����ȫ����ΪCH3OH�����ڵIJ���������ԭ�Ӷ�����ȫ����ΪCH3OH�����ѡ�ڣ����鲻��ȫȼ���ƺϳ���ʱ�ų����������õ����ʵ���֮��Ϊ1��2��CO��H2�Ļ�����壬��ǡ����ȫ��Ӧ���ɼ״�����3����������Ӧ����̬���������С�ķ��ȷ�Ӧ����˲��ý����¶ȡ�����ѹǿ��ʹƽ�����ƣ����CO��ת���ʣ���ֹ�����ж�����4��n(KOH)=2mol/L��2L=4mol�������Ⱥ�����Ӧ��CH4+2O2��CO2+2H2O����CO2+2KOH=K2CO3+H2O����K2CO3+CO2+H2O =2KHCO3����0<V��44.8 Lʱ��0<n(CH4)��2mol����0<n(CO2)��2mol��ֻ������Ӧ�٢ڣ���KOH�����������ܷ�ӦʽΪCH4+2O2+2KOH=K2CO3+3H2O��������ӦʽΪCH4��8e��+10OH��=CO32��+7H2O����44.8 L<V��89.6 L��2mol <n(CH4)��4mol����2mol <n(CO2)��4mol��������Ӧ�٢ڢۣ��õ�K2CO3��KHCO3��Һ������ӦʽΪCH4��8e��+ 9CO32��+3H2O =10HCO3������V="67.2" Lʱ��n(CH4)=3mol��n(CO2)=3mol�������ܷ�ӦʽΪ3CH4+6O2+4KOH=K2CO3+2KHCO3+7H2O����õ�1mol K2CO3��2mol KHCO3����Һ����c(K��)��c(HCO3��)��c(CO32��)��c(OH��)��c(H+)��
���㣺���黯ѧ��Ӧ�������漰���ø�˹���ɼ����ʱ䡢�Ȼ�ѧ����ʽ����д���������ʺϳɷ�����Ӱ�컯ѧƽ������ء�ȼ�ϵ�ء���Һ������Ũ�ȴ�С��ϵ����Ҫ���㡣
�����Ѷȣ�һ��
5������� ��8�֣���ͼ�ǰ���ȼ�ϵ��ʾ��ͼ�����մ�ͼ����ʾ���ش��������⣺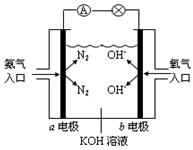
��1��a�缫��______�������������������������������������缫��ӦʽΪ_________________��
��2����Ӧһ��ʱ��������Һ��PH��?�����������С�����䡱����
��3����֪N2(g)+3H2(g)=2NH3(g) ��H=" ��92.4" kJ��mol-1��2H2(g)+O2(g)=2H2O(g) ��H=" ��483.6" kJ��mol-1����д��������ȫ ȼ��������̬ˮ���Ȼ�ѧ����ʽ��__________________________��
ȼ��������̬ˮ���Ȼ�ѧ����ʽ��__________________________��
��4�����ø�ȼ�ϵ�ز����ĵ�������Ƥ�϶�п���ư���Ƥ����ij��Ƥ������Ҫ����97.5gп��������������Ҫ���İ���_________L����״������
�ο��𰸣���8�֣�
��1������1�֣�? 2NH3-6e-+6OH-=N2+6H2O��2�֣������֣�
��2����С��1�֣�
(3) 4NH3(g)+3O2(g) = 2N2(g) +6H2O(g) ��H=" ��1266" kJ��mol-1��2�֣������֣�
(4)22.4��2�֣�
�����������
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ�����л�ѧ֪ʶ�㽲�⡶�л������.. | |
| �����Ŀ |