| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《原电池原理》高频试题特训(2019年最新版)(三)
2、选择题 有如表所示三个实验
A.金属的活动性顺序:Y>Z>X>W B.实验1中,Y作正极 C.Z放入CuSO4溶液中一定有Cu析出 D.用X、Z和稀硫酸可构成原电池,X作正极 3、选择题 下列实验装置符合实验目的是( )
A.A B.B C.C D.D 4、推断题 X、Y、Z三种短周期元素,它们的原子序数之和等于16,X2、Y2、Z2在常温下都是无色气体,它们均为工业合成某化工产品的重要原料,其流程如下 5、填空题 (14分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如下图:
(2)在500℃,以下表的物质的量(按照CO、H2O、H2、CO2的顺序)投入恒容密闭容器中进行上述第II步反应,达到平衡后下列关系正确的是
(3)在一个绝热等容容器中,不能判断此流程的第II步反应达到平衡的是?。 ①体系的压强不再发生变化?②混合气体的密度不变 ③混合气体的平均相对分子质量不变?④各组分的物质的量浓度不再改变 ⑤体系的温度不再发生变化?⑥v(CO2)正=v(H2O)逆 (4)下图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是?、? (写出两种)。若t4时刻通过改变容积的方法将压强增大为原先的两倍,在图中t4和t5区间内画出CO、CO2浓度变化曲线,并标明物质(假设各物质状态均保持不变)。 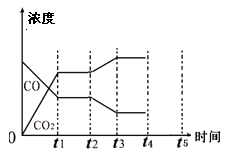 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《常见的化学.. | |