1、选择题 下列各种液体与溴水混合并充分振荡,静止后混合液为两层,且下层几乎为无色的是( ?)
A.酒精
B.汽油
C.四氯化碳
D.食盐水
参考答案:B
本题解析:酒精、食盐水都可以和溴水互溶,不分层;汽油不溶于水,密度比水轻,可以萃取溴,上层为橙红色,下层为无色;四氯化碳不溶于水,密度比水大,可以萃取溴,下层为橙红色,上层无色;故选B
本题难度:简单
2、填空题 在新制的氯水参加的反应中,有如下几种情况:
(1)向KBr溶液中加入氯水,氯水中起作用的主要微粒是______,反应的离子方程式是______.
(2)向AgNO3溶液中加入氯水,氯水中起作用的主要微粒是______,反应的离子方程式是______.
(3)向氯水中滴加石蕊试液,溶液变红,起作用的微粒是______,然后又褪色,起作用的微粒是______.
参考答案:氯水含有H2O、Cl2、HClO、Cl-、H+、OH-,
(1)向KBr溶液中加入氯水,发生Cl2+2Br-=Br2+2Cl-,故答案为:Cl2;Cl2+2Br-=Br2+2Cl-;
(2)向AgNO3溶液中加入氯水,生成白色沉淀,发生Cl-+Ag+=AgCl↓,故答案为:Cl-;Cl-+Ag+=AgCl↓;
(3)氯气与水发生Cl2+H2O?HCl+HClO,具有酸性,向氯水中滴加石蕊试液,溶液变红,由于次氯酸具有漂白性,则加入试纸最终变为无色,故答案为:H+;HClO.
本题解析:
本题难度:一般
3、简答题 (14分)
研究小组用下图装置制取Cl2,证明产生的气体中含有HCl。
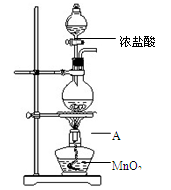
(1)仪器A的名称为?;A中反应的离子方程式为?。
(2)甲同学将A中产生的气体通入下列溶液:
实验序号
| 试剂
| 现象
|
a
| 紫色石蕊溶液
| ??
|
b
| AgNO3溶液
| 出现白色沉淀
|
①实验a中的现象为?。
②不能证明产生的气体中含有HCl的实验是?(填字母序号)。
(3)已知将HCl气体通入饱和食盐水中有白色固体析出。乙同学将A中产生的气体通入饱和食盐水中,有白色固体析出,但该实验不能证明气体中含有HCl,结合化学用语解释其原因:?。
(4)已知:2S2O32- + I2 ="==" S4O62- + 2I-。丙同学将A中产生的气体通入蒸馏水中,得到溶液X,进行以下实验证明气体中含有HCl。
I.测定X中溶解的Cl2。取25.00 mL溶液X,加入过量KI溶液,然后用0.04 mol?L-1 Na2S2O3溶液滴定生成的I2,达滴定终点时消耗Na2S2O3溶液V mL。
II.测定X中Cl元素总量。另取25.00 mL溶液X,选用适当的还原剂将溶解的Cl2全部还原为Cl-,再用0.10 mol?L-1 AgNO3溶液滴定所得溶液中的Cl-。
X中的HClO不会影响I的测定结果,原因是?。
由I、II 中实验数据可证明A中产生的气体中含有HCl,则II中消耗0.10 mol?L-1 AgNO3溶液的体积应大于?mL(用含V的代数式表示)。
参考答案:(14分)
(1)圆底烧瓶(1分)? 4H++2Cl-+MnO2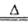 2H2O + Cl2↑+Mn2+
2H2O + Cl2↑+Mn2+
(2)①溶液先变红再褪色 ②a、b
(3)Cl2+ H2O HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
(4)(3分)
①答案一:生成1 mol HClO需消耗1 mol Cl2(1分), HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2(2分)。
答案二: Cl2+ H2O HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
HCl+HClO,Cl2发生反应时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
②0.4V
本题解析:(1)仪器A的名称为圆底烧瓶;A是二氧化锰与浓盐酸制取氯气的反应,离子方程式为4H++2Cl-+MnO2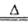 2H2O + Cl2↑+Mn2+
2H2O + Cl2↑+Mn2+
(2)①氯气溶于水生成氯化氢和次氯酸,溶液呈酸性,所以石蕊试液变红;次氯酸具有漂白性,随后溶液红色褪去;
②ab都不能证明产生的气体中含有HCl。因为氯气溶于水生成氯化氢,所以即使产生的气体中不含氯化氢,石蕊试液也会变红;同时生成的氯化氢与硝酸银溶液反应生成氯化银沉淀,不能说明产生的气体中有氯化氢;
(3)氯气与水反应生成氯化氢和次氯酸,Cl2+ H2O HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
HCl+HClO,Cl2溶于水后使得溶液中的c(Cl-)增大,也能析出晶体。
(4)①生成1 mol HClO需消耗1 mol Cl2, HClO也有氧化性,1 mol HClO和1 mol Cl2均能将2 mol KI氧化成I2,所以HClO的存在不影响实验结果;或者Cl2+ H2O HCl+HClO,Cl2氧化KI时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
HCl+HClO,Cl2氧化KI时,上述平衡逆向移动,相当于Cl2全部参与氧化I-的反应。
②I中测定Cl2的物质的量是0.04 mol?L-1×V×10-3L×1/2,则转化为Cl-的物质的量是0.04V×10-3mol;不考虑气体中的氯化氢,氯气转化的Cl-需要硝酸银的体积是0.04V×10-3mol/0.1mol/L=0.4VmL,所以II中消耗0.10 mol?L-1 AgNO3溶液的体积应大于0.4VmL,说明气体中含有HCl。
本题难度:一般
4、选择题 下列物质不能使品红溶液褪色的是( )
A.氯气
B.二氧化硫
C.漂白粉
D.氨气
参考答案:A.氯气通到品红溶液中,生成HClO使溶液褪色,故A不选;
B.二氧化硫与品红化合生成无色物质,能使品红溶液褪色,故B不选;
C.漂白粉中含ClO-,具有强氧化性,能使品红溶液褪色,故C不选;
D.氨气不具有强氧化剂,也不与品红反应,则不能使品红溶液褪色,故D选;
故选D.
本题解析:
本题难度:简单
5、选择题 取三张蓝色石蕊试纸放在表面皿上,然后按顺序分别滴加65%的浓硝酸、98%的浓硫酸和新制的氯水,三张试纸最后呈现的颜色是(? )
A.白、红、白
B.白、黑、白
C.红、红、红
D.红、黑、红
参考答案:B
本题解析:浓硝酸和氯水具有漂白性,所以当滴加到蓝色石蕊试纸上时,试纸会变为白色,浓硫酸具有脱水性,所以当滴加在蓝色石蕊试纸上时,试纸会变为黑色,所以答案选B。
本题难度:简单