1、选择题 一定量混合气体在密闭容器中发生如下反应:xA(g)+yB(g)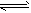 zC(g)(正反应放热),达到平衡后测得A气体的浓度为0.5mol・L-1,当恒温下将密闭容器的容积扩大到原来的两倍并再次达到平衡时,测得A的浓度为0.3mol・L-1。则下列叙述正确的是
zC(g)(正反应放热),达到平衡后测得A气体的浓度为0.5mol・L-1,当恒温下将密闭容器的容积扩大到原来的两倍并再次达到平衡时,测得A的浓度为0.3mol・L-1。则下列叙述正确的是
[? ]
A.平衡向右移动
B.x+y>z
C.B的转化率提高
D.C的体积分数增加
参考答案:B
本题解析:
本题难度:一般
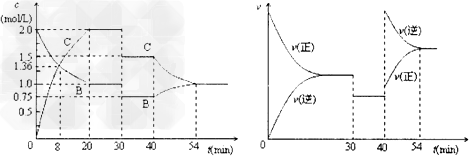
2、选择题 某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A?(g)+xB(g)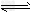 2C(g), 达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示。下列说法中正确是
2C(g), 达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化如图所示。下列说法中正确是
[? ]
A.8min时表示正反应速率等于逆反应速率
B.前20min?A的反应速率为1.00mol/(L・min?)
C.反应方程式中的x=1,30min时表示增大压强
D.40min时改变的条件是升高温度,且正反应为放热反应
参考答案:D
本题解析:
本题难度:一般
3、选择题 在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 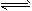 2SO3(g) ;△H<0。600℃时,在某密闭容器中,将二氧化硫和氧气混合,反应过程中 SO2、O2、SO3物质的量有如图所示的变化。其中
2SO3(g) ;△H<0。600℃时,在某密闭容器中,将二氧化硫和氧气混合,反应过程中 SO2、O2、SO3物质的量有如图所示的变化。其中
10min到15min时,与图像不相符的变化是

[? ]
A.加了催化剂
B.增加SO3的物质的量
C.升高温度
D.缩小容器体积
参考答案:B
本题解析:
本题难度:一般
4、选择题 SO2的催化氧化反应(2SO2+O2?2SO3)是一个放热的反应.如果反应在密闭容器中进行,下列有关说法中正确的是( )
A.因为反应放热,所以升高温度会使反应速率减慢
B.通过调控反应条件,SO2可以100%地转化为SO3
C.当SO2与SO3的浓度相等时,反应达到平衡
D.使用催化剂的目的是加快反应速率,提高生产效率
参考答案:该反应是前后气体体积减小的放热反应.
A、温度对化学反应速率影响是温度升高,速率增大,只是平衡逆向进行,故A错误;
B、该反应是可逆反应,所以该反应存在反应限度,反应物不可能100%的转化,故B错误;
C、达到平衡时,SO2的浓度与SO3的浓度可能相等,也可能不相等,要依据反应物的初始浓度及转化率,故C错误;
D、使用催化剂加快了反应速率,缩短反应时间,提高反应效率,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 反应:2SO2(g)+O2(g)?

2SO3(g),△H<0,根据勒夏特列原理和生产的实际要求,在硫酸生产中,下列哪一个条件是不适宜的( )
A.选用V2O5作催化剂
B.空气过量些
C.适当的压力和温度
D.低压,低温
参考答案:A.选用V2O5作催化剂,可加快反应速率,符合生产实际,故A不选;
B.空气过量些,可提高二氧化硫的转化率,符合生产要求,故B不选;
C.适当的压力和温度可加快反应的速率,符合生产要求,故C不选;
D.低压不利于产率的提高,低温时反应速率较低,不利于生产的要求,故D选.
故选D.
本题解析:
本题难度:简单