1、选择题 下图表示反应X(g)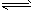 4Y(g)+Z(g),△H <0,在某温度时X的浓度随时间变化的曲线如下图,下列有关该反应的描述正确的是
4Y(g)+Z(g),△H <0,在某温度时X的浓度随时间变化的曲线如下图,下列有关该反应的描述正确的是

|
[? ]
A.第6 min后,反应就终止了
B.X的平衡转化率为85%
C.若升高温度,X的平衡转化率将大于85%
D.若降低温度,v正和v逆将以同样倍数减小
2、选择题 将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2+Br2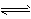 2HBr(g) △H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是?
2HBr(g) △H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是?
[? ]
A.a >b
B.a=b
C.a<b
D.无法确定
3、填空题 一定温度下,在2L的密闭容器中,发生反应:2SO2(g)+O2(g)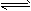 2SO3(g) △H<0
2SO3(g) △H<0

(1)用SO2表示0~4 min内该反应的平均速率为__________。
(2)若升高温度,则SO2的反应速率_________(填“变大”“变小”或“不变”),平衡常数K值
______(填“变大”“变小”或“不变”)。
(3)下列有关该反应的说法正确的是_________(填序号)。
A.反应在第4分钟时已达平衡状态
B.保持容器体积不变,当混合气体的密度不变时,说明反应已达平衡状态
C.达平衡后,缩小容器的体积,正反应速率变大,逆反应速率变小
D.通入过量O2,SO2的转化率将增大
4、填空题 某研究小组为探讨反应 A(g) + 2B(g)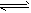 2C(g) + D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图
2C(g) + D(s)在催化剂存在的条件下对最适宜反应条件进行了一系列的实验,并根据所得实验数据绘制出下图
图中C%为反应气体混合物中C的体积百分含量(所有实验的反应时间相同)。

⑴该反应的反应热为△H______0(填>、<或=)
⑵点M和点N处平衡常数K的大小是:KM________KN(填“>”、“<”或“=”)
⑶工业上进行该反应获得产品C的适宜条件是:温度为_________℃,选择该温度的理由是____________________,压强为_________,选择该压强的理由是________________________
⑷试解释图中350℃前C%变化平缓而后急剧增大、500℃以后又缓慢增加的可能原因:
________________________
5、选择题 可逆反应mA(g)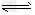 nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是
nB(g)+pC(s) ΔH=Q,温度和压强的变化对正、逆反应速率的影响分别符合下图中的两个图象,以下叙述正确的是

[? ]
A.m>n,Q>0?
B.m>n+p,Q>0?
C.m>n,Q<0?
D.m<n+p,Q<0