1、选择题 下列有关物质除杂的方法中可行的是
A.除去石英中混有的少量铝粉,可加入氢氧化钠溶液溶解后过滤
B.除去乙酸乙酯中混有的少量乙酸,加入饱和氢氧化钠溶液振荡后分液
C.已知:Ksp(CuS)<Ksp(FeS),可加入过量的难溶电解质FeS,使水中少量的Cu2+转化成硫化物沉淀而除去
D.向含有少量的FeBr2的FeCl2溶液中,加入适量氯水,再加CCl4萃取分液,以除去FeCl2溶液中的FeBr2
参考答案:D
本题解析: A、石英成分是二氧化硅,与氢氧化钠溶液反应后溶解,错误; B、乙酸乙酯在氢氧化钠溶液中发生水解反应,错误;C、根据沉淀溶解平衡知识,可以实现从难溶的到更难溶的转化,正确; D、Fe2+还原性强于Br-,Cl2首先氧化的Fe2+,错误。
本题难度:一般
2、选择题 为提纯粗盐,除去Ca2+、Mg2+、SO42-等离子,常常加入一些化学试剂,使这些可溶性的杂质沉淀下来,过滤而除去,同时采用必要的操作,下列操作顺序正确的是
[? ]
①加BaCl2?②加NaOH ③加Na2CO3?④加稀盐酸⑤过滤
A.①②③④⑤
B.⑤④③②①?
C.①②③⑤④
D.③①②⑤④?
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列各组仪器常用于物质分离的是
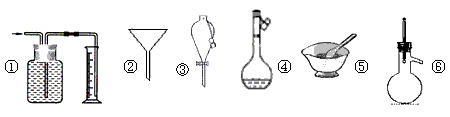
[? ]
A.①③⑥
B.②③⑥
C.②④⑥
D.②③⑤
参考答案:B
本题解析:
本题难度:简单
4、简答题 高锰酸钾是常用的氧化剂.以下是工业上用软锰矿制备高锰酸钾的一种工艺流程.
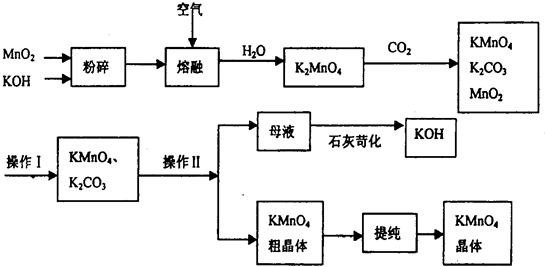
(1)高锰酸钾保存在棕色试剂瓶,下列试剂保存不需要棕色试剂瓶的是______?(填序号)
a.浓硝酸?b.硝酸银?c.氯水?d.烧碱
(2)K2MnO4和C02反应生成KMnO4、MnO2和K2C03的化学方程式为:______
(3)上述流程中可循环使用的物质有______?(用化学式表示,至少写2种).
(4)操作I的名称是______;用结晶法分离KMnO4、K2C03两种物质,进行该操作前需查阅的资料是______.
(5)以下是KMnO4的溶解度数据.
| 温度(℃) | O | 10 | 20 | 50 | 60
S(g/lOOg水)
2.8
4.3
6.3
17.0
22.1
|
实验室用重结晶的方法将KMnO4粗品制成精品.需进行的操作有:配制热饱和溶液、______、过滤、洗涤、______.洗涤所需要的玻璃仪器有烧杯、玻璃棒和______;检查是否洗净的操作是______.
参考答案:(1)浓硝酸、硝酸银、氯水光见易分解需要保存在棕色试剂瓶中,KOH不需要保存在棕色试剂瓶中.
故选:d.
(2)反应中K2MnO4→KMnO4,Mn元素化合价由+6价升高为+7价,共升高变化1价,K2MnO4→MnO2,Mn元素化合价由+6价降低为+4价,共降低2价,化合价升降最小公倍数为2,故KMnO4系数为2,MnO2系数为1.根据Mn元素守恒可知KMnO4系数为3,
根据K元素守恒可知K2C03系数为2,由碳元素守恒可知系数C02为2,方程式为3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2.
故答案为:3K2MnO4+2CO2=2KMnO4+2K2CO3+MnO2.
(3)由转化关系图知KOH及MnO2可以被循环利用.
故答案为:KOH、MnO2.
(4)过滤除去不溶于水的MnO2,利用溶解度的不同,采取浓缩结晶的方法使KMnO4从溶液中析出而分离出来.
故答案为:过滤;KMnO4、K2C03的溶解度随温度变化情况.
(5)实验室用重结晶的方法将KMnO4粗品制成精品.应配制热饱和溶液、冷却晶体、过滤、洗涤、干燥.过滤结束进行洗涤,洗涤所需要的玻璃仪器有烧杯、玻璃棒和漏斗.晶体中主要含有杂质K2CO3,可以取第二次洗涤液,加入CaCl2溶液,若没有白色沉淀生成,说明洗涤干净.
故答案为:冷却晶体; 干燥;漏斗;取第二次洗涤液,加入CaCl2溶液,若没有白色沉淀生成,说明洗涤干净.
本题解析:
本题难度:一般
5、选择题 下列除去杂质的实验方法不正确的是
[? ]
A.除去CO2中少量HCl气体:通过饱和NaHCO3溶液后再干燥气体
B.除去Na2CO3固体中少量NaHCO3:置于坩埚中加热
C.除去Cl2中的HCl气体:通过NaOH溶液
D.除去FeCl3酸性溶液中少量的FeCl2:通入稍过量的Cl2
参考答案:C
本题解析:
本题难度:一般