1������� ��ͼ��A��E��Ϊ��ѧ��ѧ�г��������ʣ�����֮��������ת����ϵ������A��DΪ�������ʣ�C�����������BΪ����ɫ��ĩ����Ӧ���������ɵ�ˮ��������������ȥ��
��ش��������⣺
��1��B��______��C��______�����ѧʽ��
��2��д��E��NaOH��Һ��Ӧ��ʵ������______��
��3��A�ڳ�����Ҳ����NaOH��Һ��Ӧ��д���˷�Ӧ�Ļ�ѧ����ʽ______��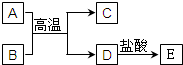
�ο��𰸣�C�����������ӦΪAl2O3��BΪ����ɫ��ĩ��ӦΪFe2O3����A��B�ķ�ӦΪ���ȷ�Ӧ��AΪAl��DΪFe����EΪFeCl2��
��1�������Ϸ�����֪��BΪFe2O3��CΪAl2O3���ʴ�Ϊ��Fe2O3��Al2O3��
��2��ΪFeCl2������NaOH��Һ������Fe��OH��2��Ϊ��ɫ������Fe��OH��2���ȶ����ױ�����Ϊ���ɫFe��OH��3������Ϊ������ɫ������Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��
�ʴ�Ϊ��������ɫ������Ѹ�ٱ�ɻ���ɫ�����ձ�ɺ��ɫ��
��3��AΪAl������NaOH��Ӧ������������Ӧ�Ļ�ѧ����ʽΪ2Al+2NaOH+2H2O�T2NaAlO2+3H2����
�ʴ�Ϊ��2Al+2NaOH+2H2O�T2NaAlO2+3H2����
���������
�����Ѷȣ�һ��
2������� A��B��C��D��E���ֻ����������ij�ֳ���������Ԫ�أ����ǵ�ת����ϵ��ͼ��ʾ������AΪ������Һ��CΪ���ܵİ�ɫ���壬E��������ˮ����ȡA��Һ���գ���ɫ��ӦΪdz��ɫ������ɫ�ܲ�����
��1��д����ѧʽ��A______��B______��C______��D______��E______��
��2��д�����з�Ӧ�����ӷ���ʽ��A��B��______��A��D______��
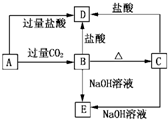
�ο��𰸣�B��C�����������ᷴӦ������NaOH��Һ��Ӧ��ӦΪ���Ի������B���ȷֽ������C�����֪BΪAl��OH��3��CΪA12O3����DΪAlCl3��EΪNaAlO2����ȡA��Һ���գ���ɫ��ӦΪ��ɫ������ɫ�ܲ���Ƭ����˵��A�к���KԪ�أ�A���������̼��Ӧ����Al��OH��3����AӦΪKAlO2��
��1��ͨ�����Ϸ���֪��A��B��C��D��E�ֱ���KAlO2��Al��OH��3��A12O3��AlCl3��NaAlO2��
�ʴ�Ϊ��KAlO2��Al��OH��3��A12O3��AlCl3��NaAlO2��
��2��A��B�ķ�ӦΪAlO2-��Al��OH��3��ת������Ӧ�����ӷ���ʽΪAlO2-+CO2+2H2O=Al��OH��3��+HCO3-��
A��D�ķ�ӦΪAlO2-��Al3+��ת������Ӧ�����ӷ���ʽΪAlO2-+4H+=Al3++2H2O��
�ʴ�Ϊ��AlO2-+CO2+2H2O=Al��OH��3��+HCO3-��AlO2-+4H+=Al3++2H2O��
���������
�����Ѷȣ���
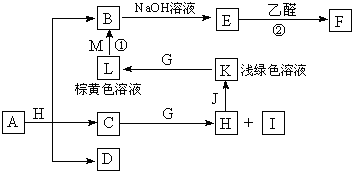
3������� ������֮���ת����ϵ��ͼ������������ʡ�ԣ�C��D����X��Y��Z������Ԫ����ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�ǿ�ȼ�����壬GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ�ٳ���������ӡˢ��·�壮
�ݴ˻ش����и��⣺
��1��д��������A�Ļ�ѧʽ______��C�ĵ���ʽ______����������L�������ӵ��Լ���______�����Լ���ɫΪ��ɫ����
��2������E�����ڹ���______�����Լ����ƣ��õ�����ɫ������Һ�����ָ���ɫ����Ϊ��Һ�д���������______���ѧʽ����
��3��д����Ӧ�ٵ����ӷ���ʽ______��д����Ӧ�ڵĻ�ѧ����ʽ���л����ýṹ��ʽ��ʾ��______��
��4����֪F����ϡ���ᣬ��Һ�����ɫ���ų���ɫ���壬��д���÷�Ӧ�Ļ�ѧ����ʽ______��
�ο��𰸣�X�����ڱ��е�ԭ�Ӱ뾶��С��ΪHԪ�أ�Y��Zԭ������������֮��Ϊ10����X��Y��Z��ԭ�������������������Ƴ�D����H��C��O�е�����Ԫ����ɣ���ɫ�ǿ�ȼ�����壩ΪCO2������֪��X��Y��Z��H��C��O����CΪH2O��HΪHCl��I��Ư�����ã�ӦΪHClO��dz��ɫ���ػ�ɫ��ҺΪFe2+��Fe3+����֪JΪFe��KΪFeCl2��LΪFeCl3����Ӧ����������ӡˢ��·��ΪFeCl3��Cu����MΪCu��BΪCuCl2��E������ȩ��Ӧ��ӦΪCu��OH��2��FΪCu2O����A+H��HCl��=B��CuCl2��+C��H2O��+D��CO2����֪��A�Ǻ���Cu2+��̼���Σ���A+H��HCl��=B��CuCl2��+C��H2O��+D��CO2����֪��A�Ǻ���Cu2+��̼���Σ�ӦΪCuCO3��Cu2��OH��2CO3��Cu��OH��2?CuCO3��
��1�������Ϸ�����֪A��CuCO3��Cu2��OH��2CO3��Cu��OH��2?CuCO3��CΪH2O������ʽΪ
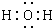
��LΪFeCl3����������L�������ӵ��Լ������軯�أ�
�ʴ�Ϊ��CuCO3��Cu2��OH��2CO3��Cu��OH��2?CuCO3��
�����軯�أ�
��2��EΪCu��OH��2�����백ˮ������Ϸ�Ӧ����[Cu��NH3��4]2+���õ�����ɫ������Һ��
�ʴ�Ϊ����ˮ��[Cu��NH3��4]2+��
��3����Ӧ��Ϊ�Ȼ�����ͭ�ķ�Ӧ����Ӧ�����ӷ���ʽΪCu+2Fe3+�TCu2++2Fe2+����ȩ��������ͭ��Һ�ڼ��ȵ������·�Ӧ�ķ���ʽΪCH3CHO+2Cu��OH��2+NaOH��
���������
�����Ѷȣ�һ��
4������� (9��)�Ժ�ˮ�г�������AΪԭ�Ͽ��Է�չ�ܶҵ��������ͼ�а�������ѧ�α��н��ܵļ��ֻ�����ҵ�������������ͼ������֮���ת����ϵ�ش��������⡣
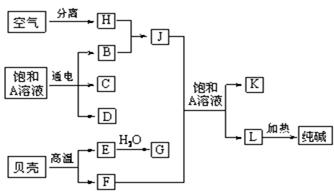
(1) C��D��C��G��Ӧ��������ȡ��������д��C��G��Ӧ��ȡ�������Ļ�ѧ��Ӧ����ʽ��?��
(2) ���A��Һ��Ӧ�����ӷ���ʽΪ___________________________��
���÷�Ӧ��ת�Ƶ�����Ϊ8NA��������������ڱ�״�������Ϊ?L
(3) J���ӵĿռ乹��Ϊ______________________
(4)ʵ���ҿ���K��G���������ȡJ��д���÷�Ӧ��ѧ����ʽ��_______________________________________��
�ο��𰸣�(9��)��1��2Cl2 + 2Ca(OH)2 === CaCl2 + Ca(ClO)2?+ 2H2O? (2��)
(2)2H2O��2Cl��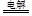 Cl2����H2����2OH��?89.6L?��4�֣�
Cl2����H2����2OH��?89.6L?��4�֣�
(3) ������? (1��)
(4) Ca(OH)2��2NH4Cl 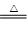 ?CaCl2��2NH3����2H2O? (2��)
?CaCl2��2NH3����2H2O? (2��)
�������������������ͼ�⣬�ؼ�����ͻ�Ƶ㡣���ǵ���Ҫ�ɷ���̼��ƣ������·ֽ����������ƺ�CO2�����ں�ˮ�к����Ȼ��ƣ��� C��D��C��G��Ӧ��������ȡ����������˵��C��������D���������ƣ�B����������A���Ȼ��ơ�J��CO2ͨ�뱥���Ȼ�����Һ���ܵõ�L����L���ȼ�����̼���ƣ�˵��L��̼�����ƣ���˸÷�Ӧʽ�����Ƽ��ԭ������J�ǰ�������H�ǵ�����K���Ȼ�李�
��1���������������Ʒ�Ӧ����Ư�۵ķ���ʽ��2Cl2 + 2Ca(OH)2 === CaCl2 + Ca(ClO)2?+ 2H2O��
��2����ҵ��ⱥ��ʳ��ˮ�ķ���ʽ��2H2O��2Cl�� Cl2����H2����2OH�����ؼ�����ʽ��֪����Ӧ��ת��2�����ӣ��������ת��8NA�����ӣ���������������������4mol���ڱ�״���µ������4mol��22.4L/mol��89.6L��
Cl2����H2����2OH�����ؼ�����ʽ��֪����Ӧ��ת��2�����ӣ��������ת��8NA�����ӣ���������������������4mol���ڱ�״���µ������4mol��22.4L/mol��89.6L��
��3�������������νṹ��
��4��ʵ������ȡ�����ķ���ʽ��Ca(OH)2��2NH4Cl 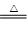 ?CaCl2��2NH3����2H2O��
?CaCl2��2NH3����2H2O��
�����Ѷȣ�һ��
5������� A��B��C��D��EΪ��ѧ��ѧ�������ʣ�����A��CΪ�������ʣ�EΪ�ǽ������ʣ���ͼ������֮����ת����ϵ����ش�
��1����Ӧ�ٵĻ�����Ӧ������______��
��2��C�Ļ�ѧʽΪ______��
��3��д������E��B�ڼ��������·�Ӧ�Ļ�ѧ��?��ʽ______��
��4����dz��ɫ��ҺDת��Ϊ��ɫ��Һ�ķ����ǣ������ӷ���ʽ��ʾ��______��
��5���Ҵ���A�������������¿��Ա������е���������������д���÷�Ӧ�Ļ�ѧ����ʽ��______��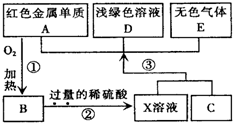
�ο��𰸣���AΪ��ɫ�������ʣ���AΪCu���ɷ�Ӧ�ٿ�֪BΪCuO���ɷ�Ӧ��XΪ����ͭ����������Һ���ɷ�Ӧ��X��Һ+C��A+D+E����DΪdz��ɫ��Һ������Fe2+����EΪ��ɫ���壬��CΪFe��DΪFeSO4��EΪH2��
��1����Ӧ����2Cu+O2?��ȼ?.?2CuO�����ڻ��Ϸ�Ӧ���ʴ�Ϊ�����Ϸ�Ӧ��
��2��������������֪��CΪFe���ʴ�Ϊ��Fe��
��3��H2��CuO�ڼ��������·�Ӧ��Cu��H2O����Ӧ����ʽΪ��H2+CuO?��?.?Cu+H2O���ʴ�Ϊ��H2+CuO?��?.?Cu+H2O��
��4������ǿ��������dz��ɫFeSO4��Һת��Ϊ��ɫFe2��SO4��3��Һ���������ˮ�ȣ���Ӧ���ӷ���ʽΪ��2Fe2++Cl2=2Fe3++2Cl-��
�ʴ�Ϊ��2Fe2++Cl2=2Fe3++2Cl-��
��5���Ҵ���Cu�������������¿��Ա������е�����������������ȩ��ˮ���÷�Ӧ�Ļ�ѧ����ʽΪ��2CH3CH2OH+O2Cu
���������
�����Ѷȣ�һ��