1、选择题 下列解释实际应用的原理表达式中,不正确的是
A.用排饱和食盐水法收集Cl2:Cl2 + H2O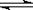 H+ + Cl-+ HClO
H+ + Cl-+ HClO
B.碳酸氢钠溶液中加入过量石灰水:HCO3- + Ca2+ + OH-= CaCO3↓+ H2O
C.KI溶液与H2SO4酸化的H2O2溶液混合:2I- + H2O2 + 2H+ = 2H2O + I2
D.用饱和FeCl3溶液制备Fe(OH)3胶体:FeCl3 +3H2O= Fe(OH)3+ 3HCl
参考答案:D
本题解析:D错,正确反应方程式为: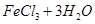


本题难度:一般
2、简答题 某无色溶液,由Na+、Ba2+、Al3+、Cl-、MnO4-、CO32-、NO3-中的若干种组成.,现取两份100mL溶液进行如下实验:
①第一份小心蒸发得溶质3.08g;
②第二份加足量AgNO3溶液后,得干燥沉淀5.63g,向沉淀中加入足量盐酸,生成标准状况下气体0.224L.
根据上述实验回答下列问题:
(1)第二份溶液所得沉淀的成分是?,其物质的量分别是?.
(2)写出步骤②中所发生的所有反应的离子方程式?.
(3)一定存在的离子是?,其浓度分别是?.
参考答案:溶液无色,则一定不存在MnO4-,
第二份加足量AgNO3溶液后,得干燥沉淀5.63g,向沉淀中加入足量盐酸,生成标准状况下气体0.224L,
则说明原溶液中含有CO32-,且n(CO32-)=0.224L22.4L/mol=0.01mol,
则m(Ag2CO3)=0.01mol×276g/mol=2.76g<5.63g,
所以:溶液中还有Cl-,n(Cl-)=n(AgCl)=5.63g-2.76g143.5g/mol=0.02mol,
步骤②中所发生的所有反应的离子方程式有:2Ag++CO32-=Ag2CO3↓,
Ag++Cl-=AgCl↓,
Ag2CO3+2H++2Cl-=2AgCl+H2O+CO2↑.
所以原溶液中含有n(NaCl)=0.02mol,n(Na2CO3)=0.01mol,
m(NaCl)=0.02mol×58.5g/mol=1.17g,
n(Na2CO3)=0.01mol×106g/mol=1.06g.
则有:1.17g+1.06g=2.23g<3.08g,
所以溶液中还应含有NO3-,
则:n(NO3-)=n(NaNO3)=3.08g-2.23g85g/mol=0.01mol,
n(Na+)=0.01mol×2+0.02mol+0.01mol=0.05mol,
故答案为:(1)AgCl、Ag2CO3;0.02mol、0.01mol;
(2)2Ag++CO32-=Ag2CO3↓,Ag++Cl-=AgCl↓,Ag2CO3+2H++2Cl-=2AgCl+H2O+CO2↑;
(3)Na+、Cl-、CO32-、NO3-;Na+(0.5mol/L)、Cl-(0.2mol/L)、CO32-(0.1mol/L)、NO3-(0.1mol/L).
本题解析:
本题难度:一般
3、选择题 下列离子方程式中,书写正确的是
A.铝与盐酸反应:Al + H+= Al3+ + H2↑
B.氢氧化铝与氢氧化钠溶液反应:Al(OH)3 + OH-=AlO2- + 2H2O
C.铁与氯化铁溶液反应:
D.铝与氢氧化钠溶液反应:Al + 2OH- = AlO2- + H2↑
参考答案:B
本题解析:A中电子的得失不守恒,应该是2Al + 6H+=2 Al3+ +3H2↑,A不正确;C也是没有配平,应该是Fe +2Fe3+=3Fe2+,C不正确;D中反应物还有水参加,不正确,答案选B。
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生能力的培养和训练。该题需要明确判断离子方程式正确与否的方法一般,即(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式,然后灵活运用即可。该题有助于培养学生分析问题、解决问题的能力。
本题难度:一般
4、选择题 能正确表示下列化学反应的离子方程式是
[? ]
A.氧化铜与稀硫酸反应:O2-+2H+= H2O
B.稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑
C.铜片插入硝酸银溶液中Cu+Ag+=Cu2++Ag
D.硫酸氢钾与氢氧化钠:OH-+H+=H2O
参考答案:D
本题解析:
本题难度:一般
5、选择题 下列离子方程式书写正确的是( )
A.AgNO3溶液滴入少量的Na2S溶液?2Ag++S2-=Ag2S↓
B.过量的CO2通入Ca(ClO)2溶液中?2ClO-+2CO2+H2O=2HCO3-+2HClO
C.向Na2CO3溶液中加入过量CH3COOH溶液?CO32-+2H+=CO2↑+H2O
D.向Ba(OH)2溶液中加入少量NaHSO3溶液2HSO3-+Ba2++2OH-=BaSO3↓+2H2O
参考答案:A、AgNO3溶液滴入少量的Na2S溶液反应生成硫化银沉淀,离子方程式为2Ag++S2-=Ag2S↓,故A正确;
B、过量的CO2通入Ca(ClO)2溶液中反应的离子方程式为:ClO-+CO2+H2O=HCO3-+HClO,故B错误;
C、向Na2CO3溶液中加入过量CH3COOH溶液反应的离子方程式?CO32-+2CH3COOH=CO2↑+H2O+2CH3COO-;故C错误;
D、向Ba(OH)2溶液中加入少量NaHSO3溶液,亚硫酸氢钠全部反应,离子方程式为:HSO3-+Ba2++OH-=BaSO3↓+H2O,故D错误;
故选A.
本题解析:
本题难度:简单