1、选择题 镍铬(Ni-Cd)可充电电池的电解质溶液为KOH溶液,它的充、放电反应按下式进行:
Cd + 2NiOOH + 2H2O Cd(OH)2 + 2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和
Cd(OH)2 + 2Ni(OH)2;已知Ni(OH)2、Cd(OH)2和
NiOOH都不溶于KOH溶液。则下列有关电极反应式正确的是
A.放电时负极:Cd-2e-=Cd2+
B.放电时正极:2NiOOH + 2e- + 2H2O=2Ni(OH)2 + 2OH-
C.充电时阳极:2Ni(OH)2-2e-+ 4H+=2Ni3+ + 4H2O
D.充电时阴极:Cd(OH)2 + 2e-=Cd + 2OH-
参考答案:BD
本题解析:书写可逆电池电极反应式时要注意电池反应的方向,即确定原电池和电解池的反应,注意介质等内容。A、Cd(OH)2不溶解,故写化学式,错误;B、正确;C、电池的介质为碱性,电池反应式中不能出现H+,错误;D、正确。
本题难度:简单
2、选择题 下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是(?)
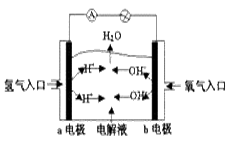
A.a电极是负极
B.b电极的电极反应为:4OH--4e-==2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储存电池内的新型发电装置
参考答案:B
本题解析:氢氧燃料电池中,通入氢气的一极为电源的负极,发生氧化反应,通入氧气的一极为原电池的正极,电子由负极经外电路流向正极。A、通入氢气的a极为电源的负极,正确;B、通入氧气的b极为原电池的正极,该极上发生得电子的还原反应,错误;C、氢氧燃料电池的产物是水,环保无污染,是一种具有应用前景的绿色电源,正确;D、氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏电池内的新型发电装置,正确。
本题难度:一般
3、简答题 “阿波罗号飞船”所用的氢氧燃料电池的电极应为:负极:2H2+4OH--4e-=4H2O则正极反应为______,该电池工作时,通氢气的一极发生______反应?(填氧化、还原),每转移4摩电子,电池内增加______摩水,负极附近溶液的pH值______,(填升高、降低、不变),正极附近[H+]______(填升高、降低、不变)
参考答案:通入氢气的一极为负极,发生氧化反应,负极反应为2H2-4e-+4OH-=2H2O,可判断溶液呈碱性,负极消耗OH-离子,浓度降低,则pH降低;
碱性溶液中正极发生还原反应,电极反应为O2-4e-+2H2O=4OH-,正极生成OH-离子,OH-离子浓度增大,则H+离子浓度降低;
氢氧燃料电池的实质是在一定条件下形成了原电池,其实质仍然是O2把H2氧化,电池总反应为2H2+O2=2H2O,
每转移4mol电子,消耗1molO2,生成2molH2O.
故答案为:O2-4e-+2H2O=4OH-;氧化;2mol;降低;降低.
本题解析:
本题难度:一般
4、选择题 铅蓄电池在现代生活中有广泛的应用。其电极材料是Pb和PbO2,电解质是稀硫酸。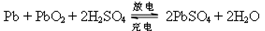 ,下列说法正确的是?
,下列说法正确的是?
A.铅蓄电池使用一段时间后要添加硫酸
B.电池充电时,阴极反应为:Pb-2e-+SO42-
C.电池充电时,电池正极应和电源的正极相连接
D.电池放电时,电池正极周围溶液pH不断增大
参考答案:CD
本题解析:铅蓄电池的工作原理:
放电时:(负极)Pb?电极式为Pb-2e-+ SO42-="=" PbSO4
?(正极):PbO2?电极式为PbO2+ 2e-+4 H++SO42-="=" PbSO4+ 2H2O;
故放电时总反应式为:? Pb+PbO2+2H2SO4="=" 2PbSO4+ 2H2O;
充电时:(阴极)?电极式为PbSO4+ 2 e-="=Pb" +SO42-
?(阳极)电极式为PbSO4+ 2e-+2H2O=PbO2+4H+;
故充电时总反应式为2PbSO4+2H2O==PbO2+Pb+2H2SO4
铅蓄电池充电时,负极要与电源的负极相连,正极与电源正极相连。
本题难度:一般
5、填空题 (14分,每空2分)四种短周期元素A、B、C、D的性质或结构信息如下。
①原子半径大小:A>B>C>D
②四种元素之间形成的某三种分子的比例模型及部分性质如下:

请根据上述信息回答下列问题。
(1)C元素在周期表中的位置 , 请写出D2C2分子的结构式________,A元素的单质与物质甲发生反应的离子方程式_______。
(2)丁物质与乙互为同系物,在相同条件下其蒸气的密度是氢气密度的36倍,且核磁共振氢谱只有
1组峰,写出丁物质的结构简式 。
(3)A与同周期的E元素组成的化合物EA5在热水中完全水解生成一种中强酸和一种强酸,该反应的化学方程式是 。
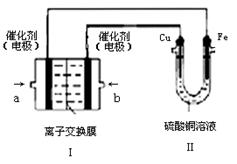
(4)以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,该同学想在装置Ⅱ中实现铁上镀铜,则a处电极上发生的电极反应式 ,一段时间后,测得铁增重128g,此时b极通入气体的体积是 L(标准状况下)。
参考答案:(14分,每空2分)
(1)第2周期、ⅥA族 ;H-O-O-H Cl2+H2O H+ + Cl―+HCO (2)C(CH3)4
H+ + Cl―+HCO (2)C(CH3)4
(3)PCl5+4H2O = H3PO4+5HCl (4)CH4-8e-+10OH-=CO32- +7H2O 22.4
本题解析:(1)根据三种模型可知分别是水、甲烷和次氯酸。则根据原子半径大小顺序A>B>C>D可知D是H、B是碳元素,C是氧元素,A是氯元素。氧元素位于周期表的第二周期第ⅥA族。双氧水的结构式为H―O―O―H。氯气与水反应的方程式为Cl2+H2O H+ + Cl―+HClO。
H+ + Cl―+HClO。
(2)丁物质与甲烷互为同系物,在相同条件下其蒸气的密度是氢气密度的36倍,则相对分子质量水72,所以是戊烷。核磁共振氢谱只有1组峰,说明是新戊烷,则丁物质的结构简式为C(CH3)4。
(3)A与同周期的E元素组成的化合物EA5在热水中完全水解生成一种中强酸和一种强酸,该化合物是五氯化磷,因此该反应的化学方程式是PCl5+4H2O = H3PO4+5HCl。
(4)铁上镀铜,则铁是阴极,所以a是负极,通入的是甲烷,电极反应式为CH4-8e-+10OH-=CO32- +7H2O。一段时间后,测得铁增重128g,即析出铜是2mol,转移4mol电子,所以根据电子守恒可知需要乙炔是1mol,因此时b极通入标准状况下气体的体积是22.4L。
考点:考查元素、物质推断的有关应用
本题难度:困难