1、选择题 下列反应中不能引入羟基(―OH)的是
A.加成反应
B.取代反应
C.消去反应
D.还原反应
参考答案:C
本题解析:乙烯和水加成引入羟基,溴苯和氢氧化钠的水溶液反应取代生成苯酚,乙醛加氢生成乙醇,消去反应减去羟基。
本题难度:简单
2、选择题 下列物质在相同状况下含C量最高的是
A.丙烷
B.乙烯
C.苯
D.氯仿
参考答案:C
本题解析:根据烃的最简式CHn可知,n越大,含碳量越低。所以根据有机物的分子式可判断选项C是正确的。答案选C。
本题难度:一般
3、选择题 取一定质量含Cu、Cu2O、CuO的固体混合物,将其分成两等份,进行如下实验:A份通入足量H2,固体质量减少6.4g;B份加入500mL稀硝酸,固体恰好完全溶解,生成NO气体4.48L(标况下),则转化过程中加入的HNO3的浓度是
A.3.2mol/L
B.3.6mol/L
C.4.0mol/L
D.4.4mol/L
参考答案:A
本题解析:分析:将Cu2O拆分为Cu与CuO,则混合物视为Cu与CuO,固体质量减少6.4g为失氧的质量,故n(CuO)=n(O);生成NO为0.2mol,由电子守恒知:2n(Cu)=3n(NO),根据铜元素守恒可知与硝酸反应后的溶液在n[Cu(NO3)2]=n(Cu)+n(CuO),由氮元素守恒可知原硝酸溶液中n(HNO3)=2n[Cu(NO3)2]+n(NO),再根据c=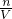 计算加入的HNO3的浓度.
计算加入的HNO3的浓度.
解答:将Cu2O拆分为 Cu与CuO,则混合物视为Cu与CuO,固体质量减少6.4g为失氧的质量,故n(CuO)=n(O)=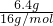 =0.4mol;
=0.4mol;
生成NO为 =0.2mol,由电子守恒知:2n(Cu)=3n(NO),即2n(Cu)=0.2mol×3,n(Cu)=0.3mol,
=0.2mol,由电子守恒知:2n(Cu)=3n(NO),即2n(Cu)=0.2mol×3,n(Cu)=0.3mol,
根据铜元素守恒可知与硝酸反应后的溶液在n[Cu(NO3)2]=n(Cu)+n(CuO)=0.3mol+0.4mol=0.7mol,
由氮元素守恒可知原硝酸溶液中n(HNO3)=2n[Cu(NO3)2]+n(NO)=0.7mol×2+0.2mol=1.6mol,
所以加入的HNO3的浓度c(HNO3)= =3.2mol/L.
=3.2mol/L.
故选A.
点评:本题考查有关混合物的计算、氧化还原反应计算等,难度中等,关键是清楚反应过程,可以根据守恒列方程组解答,本题采取拆分法简化计算,注意掌握常用的计算方法.
本题难度:困难
4、选择题 超市销售的“84”消毒液,其商标标识上注明:①可对餐具、衣物进行消毒,可漂白浅色衣物?②本品为无色液体,呈碱性?③使用时应加水稀释.其有效成份可能是
A.NaHCO3
B.Cl2
C.NaClO
D.NaCl
参考答案:C
本题解析:分析:①可对餐具、衣物进行消毒,可漂白浅色衣物,说明物质具有强氧化性; ②本品为无色液体,呈碱性,说明为强碱弱酸盐,应含有NaClO.
解答:“84”消毒液的有效成份为NaClO,为强碱弱酸盐,溶液呈碱性,可与酸反应生成具有强氧化性和漂白性的HClO,则可对餐具、衣物进行消毒,可漂白浅色衣物.
故选C.
点评:本题考查84消毒液的成份和性质,题目难度不大,注意HClO的性质和用途,学习中注意相关基础知识的积累.
本题难度:简单
5、选择题 下列离子方程式书写正确的是
A.Ca(HCO3)2溶液中滴入过量NaOH溶液:HCO+Ca2++OH-=CaCO3↓+H2O
B.向NaAlO2溶液中通入过量的CO2:CO2+2H2O+AlO2=Al(OH)3↓+HCO
C.0.01mol/L?NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO+2H2O
D.向Ca(ClO)2溶液中通入过量的SO2:ClO-+SO2+H2O=HClO+HSO
参考答案:B
本题解析:分析:A.Ca(HCO3)2完全反应,生成碳酸钙、碳酸钠和水;
B.反应生成氢氧化铝和碳酸氢钠;
C.二者以1:2反应,生成硫酸钡、氢氧化铝、一水合氨;
D.发生氧化还原反应生成硫酸钙和盐酸.
解答:A.Ca(HCO3)2溶液中滴入过量NaOH溶液的离子反应为Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32-,故A错误;
B.向NaAlO2溶液中通入过量的CO2的离子反应为CO2+2H2O+A1O2-=Al(OH)3↓+HCO3-,故B正确;
C.0.01mol/L?NH4Al(SO4)2溶液与0.02mol/L Ba(OH)2溶液等体积混合的离子反应为NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3.H2O,故C错误;
D.向Ca(ClO)2溶液中通入过量的SO2的离子反应为Ca2++ClO-+SO2+H2O=CaSO4↓+2H++Cl-,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,注意与量有关的离子反应及与氧化还原有关的离子反应均为解答的难点,题目难度较大,选项C为易错点.
本题难度:困难