1、选择题 .有一无色透明溶液,取出少量并滴入BaCl2溶液,只有白色沉淀生成;另取一定体积并加入Na2O2, 有无色无味气体产生,同时有白色沉淀生成,其沉淀量与加入Na2O2的量的关系如图所示。则该溶液中一定存在的离子是
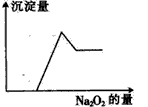
[? ]
①H+ ②NH4+ ③Al3+ ④Mg2+ ⑤Fe2+ ⑥NO3- ⑦SO42- ⑧CO32-
A.③④⑧
B.③④⑦
C.①③④⑦
D.②③④⑧
参考答案:C
本题解析:
本题难度:一般
2、选择题 某溶液中只可能含有Fe2+、A13+、NH4+、CO32-、AlO2-、SO32-、SO42-、C1-、NO2-中的若干种(忽略水的电离),离子浓度均为0.2mol?L-1,现取该溶液加入稀硫酸后得强酸性X溶液,过程中无明显现象,取X溶液进行以下实验:
①X溶液中滴加Ba(NO3)2溶液至过量会产生白色沉淀A、无色气体A,A遇空气变成棕色;过滤,获得溶液A
②在溶液A中加入过量的NaOH溶液产生气体、沉淀B,过滤获得溶液B
③在溶液B中通入适量CO2气体有沉淀C产生
则下列说法中正确的是( )
A.无法确定沉淀C的成分
B.无法确定原溶液中是否含有Cl-、A13+
C.溶液A中存在的阳离子有Ba2+、Fe2+、NH4+、H+
D.原溶液中存在Fe2+、NH4+、Cl-、SO42-
参考答案:加入的是稀硫酸,无明显现象,直接排除CO32-,AlO2-、SO32-、NO2-,此过程中引入了SO42-,且溶液呈酸性溶液X,
①X溶液中滴加Ba(NO3)2溶液至过量会产生白色沉淀A,白色沉淀A为BaSO4,加入硫酸引入了SO42-,不能说明原溶液中含有SO42-.得到无色气体A,A遇空气变成棕色,A为NO,说明原溶液中含有还原性离子,故一定含有Fe2+,过滤,获得溶液A,溶液A中含有Fe3+、Ba2+等;
②在溶液A中加入过量的NaOH溶液产生气体、沉淀B,沉淀B为Fe(OH)3,产生气体,该气体一定为NH3,原溶液中含有NH4+,过滤,获得溶液B,溶液B含有Ba2+等;
③在溶液B中通入适量CO2气体有沉淀C产生,则沉淀为BaCO3或Al(OH)3或二者都有,
由上述分析可以得出原溶液一定有Fe2+、NH4+,一定不含CO32-,AlO2-、SO32-、NO2-,可能含有A13+、SO42-、C1-,由于离子浓度均为0.2mol?L-1,根据电荷守恒,阳离子总电荷一定大于等于0.6mol?L-1,但是阴离子总电荷最大只能为0.6mol?L-1,故一定存在SO42-、C1-,一定不存在A13+,
综合上述分析,可知原溶液一定有Fe2+、NH4+、SO42-、C1-,一定不含A13+、CO32-,AlO2-、SO32-、NO2-,
A.由上述分析可知,原溶液中不含A13+,故沉淀C为BaCO3,故A错误;
B.由上述分析可知,溶液中一定含有C1-,一定不含A13+,故B错误;
C.由上述分析可知,溶液A中Ba2+、Fe3+、NH4+、H+,故C错误;
D.由上述分析可知,原溶液一定有Fe2+、NH4+、SO42-、C1-,故D正确;
故选D.
本题解析:
本题难度:简单
3、选择题 下列有机物鉴别方法不正确的是( )
A.苯和己烷分别放入水中,观察液体是否分层
B.将溴水分别加入到四氯化碳和苯中,观察溶液颜色及是否分层
C.将乙烯和甲烷分别通入酸性高锰酸钾溶液,观察溶液颜色是否变化
D.将碳酸氢钠分别加入到乙醇和乙酸中,观察是否有气泡产生
参考答案:A、苯和己烷都不溶于水,放入水中都分层,不能鉴别,故A错误;
B、四氯化碳和苯都不溶于水,但四氯化碳的密度比水大,苯的密度比水小,色层位置不同,可鉴别,故B正确;
C、乙烯能与酸性高锰酸钾反应,而甲烷不反应,能够褪色的是乙烯,可鉴别,故C正确;
D、乙酸具有酸性,与碳酸氢钠反应产生气体,而乙醇不反应,可鉴别,故D正确.
故选A.
本题解析:
本题难度:简单
4、选择题 把氢氧化钠溶液和硫酸铜溶液加入某病人的尿液中,微热时如果观察到红色沉淀,说明该尿液中含有( )
A.醋酸
B.乙醇
C.乙酸乙酯
D.葡萄糖
参考答案:D
本题解析:
本题难度:简单
5、填空题 有A、B、C、D、E五种可溶性物质,它们所含的阴、阳离子互不相同,分别是以下两组离子中的各一种。?

(1)某同学通过分析,认为无需检验就可确定其中两种物质的组成,试写出这两种物质的化学式:____________、___________。
(2)把第(1)小题检验出的物质分别标记为A、B。当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时,产生棕灰色沉淀,向该沉淀中滴入过量稀HNO3,发现最后仍有白色沉淀残留。则X可能为____________离子。
(3)在D的水溶液中加入Cu片,Cu不溶解,再加适量稀H2SO4,Cu会逐渐溶解。则D中一定含有_______________离子,有关反应的离子方程式为______________。
(4)你认为能否通过上述已检验出的物质来确定E的组成?若能,简述实验方案;若不能,简述理由。____________。
参考答案:(1)Na2CO3 ;Ba(OH)2
(2)SO42-
(3)NO3-? ;3Cu+8H++2NO3-=3Cu2+ +2NO↑+4H2O
(4)能。向E的水溶液中加入过量A[Ba(OH)2],若最后有沉淀,则E为MgCl2,否则为AlCl3[或向E的水溶液中加入适量B(Na2CO3),若只产生沉淀,则E为MgCl2,否则为AlCl3]
本题解析:
本题难度:一般