| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《电解池原理》高频试题预测(2019年最新版)(八)
参考答案:B 本题解析:A、一个苯乙烯中有1个碳碳双键,所以0.1摩尔苯乙烯中含有0.1摩尔的碳碳双键,错误,不选A;B、根据氯原子守恒判断,正确,选B;C、二氧化硫和氧气反应是可逆反应,不能完全反应,故转移电子数不能确定,错误,不选C;D、电解精炼时,阳极先溶解锌铁等杂质,所以阳极质量减少部分不能确定,不选D。 本题难度:困难 2、选择题 某同学为了使反应2HCl + 2Ag==2AgCl + H2↑能进行,设计了下列四个实验,如下图所示,你认为可行的方案是 参考答案:C 本题解析: 本题难度:简单 3、选择题 用惰性电极电解CuSO4溶液一段时间后,停止电解向所得溶液中加入0.2molCu(OH)2,恰好反应时溶液浓度恢复至电解前,关于电解过程说法不正确的是 |
参考答案:C
本题解析:A.根据铜原子守恒,加入0.2molCu(OH)2,恰好反应时溶液浓度恢复至电解前,说明生成铜0.2mol,A项正确;B.电解硫酸铜生成铜、氧气和硫酸,所以随着电解的进行,溶液的PH值减小,B项正确;C.根据加入的物质,氧原子都是由阳极放电得到,阳极电解反应为4OH--4e-=2H2O+O2↑,一共生成0.2mol氧气,转移的电子物质的量为0.8mol,C项错误;D.项正确;选C。
考点:考查电解的计算。
本题难度:一般
4、选择题 按下图的装置进行试验,若图中X轴表示阴极的电子的量,则Y轴可能表示为(?)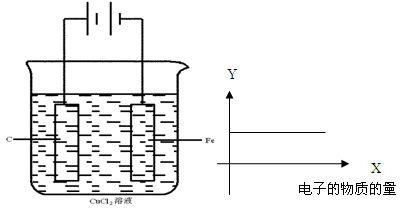
A.Cu2+物质的量浓度
B.C棒的质量
C.Fe棒的质量
D.Cl-物质的量浓度
参考答案:B
本题解析:该装置为电解池。由图乙可知在阴极电子的物质的量不断增加,但是Y的量不发生变化。A.若电解含Cu2+的溶液,在由于放电能力Cu2+>H+,则在阴极发生反应Cu2++2e-="Cu," Cu2+的物质的量减小,其浓度也减小。不符合题意。错误。B.由于C是不活泼的非金属单质,在电解的过程中,无论是作阳极还以阴极,其质量都不会发生变化。正确。C.由于Fe是比较活泼的金属,所以若Fe棒作阳极,则在阳极就会发生反应:Fe-2e-=Fe2+.Fe棒的质量就会减小,若Fe棒作阴极,其质量就不会发生变化。因此质量可能会发生变化。错误。D.若电解的电解质溶液中含有Cl-,由于阴离子的放电能力Cl-> OH-,所以在阳极发生反应:2Cl―2e-=Cl2↑.Cl-物质的量会减小,其浓度也要减小。错误。
本题难度:一般
5、填空题 (14分)
如下图所示,A、F为石墨电极,B、E为铁片电极.按要求回答下列问题.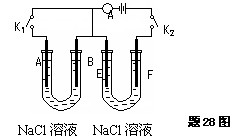
(1)打开K2,合并K1.B为?极,A的电极反应为?,最终可观察到的现象是?.
(2)打开K1,合并K2.E为?极,F极的电极反应为?,
检验F极产生气体的方法是?.
(3)若往U型管中滴加酚酞,进行(1)(2)操作时,A、B、E、F电极周围能变红的是?,原因是?.
参考答案:
(1)B为?负极(1’),A的电极反应为? O2+4e-+2H2O==4OH-?,(2’)
现象是?溶液中产生白色沉淀,最终变为红褐色?(2’)
(2)E为?阴极,(1’)F极的电极反应为? 2Cl--2e-==Cl2↑?,(2’)
方法是?用湿润的淀粉-KI试纸检验,试纸变蓝则说明是氯气?.(2’)
(3)能变红的是 AE?,(2’)原因是? A极O2上放电产生OH-,E极上水放电产生H2和OH-,均导致电极区域呈碱性?.(2’)
本题解析:略
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《手性分子》.. | |