1、填空题 (12分)(1)环境专家认为可以用金属铝将水体中的NO3-转化为N2,从而消除污染。该反应中涉及的微粒有:H2O、Al、OH-、Al(OH)3、NO3-、N2,请将这些微粒中除NO3-以外的微粒填入以下空格内(不用配平)。

该反应过程中,被氧化与被还原的元素的物质的量之比为 。
(2)我国首创的海洋电池以海水为电解质溶液,电池总反应是4Al +3O2+6H2O ="4" Al(OH)3。电池正极的电极反应式是 ;消耗13.5 g Al时转移_________mole-。
(3)铝与某些金属氧化物在高温下的反应称为铝热反应,可用于冶炼高熔点的金属。
已知:4Al(s) +3O2(g) = 2Al2O3(s)△H = -2830 kJ/mol
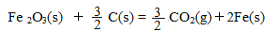 △H = +230 kJ/mol
△H = +230 kJ/mol
C(s)+O2(g) = CO2(g) △H = -390 kJ/mol
铝与氧化铁发生铝热反应的热化学方程式是 ,铝热反应属于______(填字母)反应。
a.氧化还原 b.复分解 c.置换
参考答案:(1)NO3- + Al +H2O→ Al(OH)3 + N2 + OH-(2分) 5∶3
(2)O2+4e-+2H2O=4OH- 1.5
(3)2 Al(s) + Fe2O3 (s)= 2 Fe(s) +Al2O3 (s) △H = - 600 kJ/mol a c
本题解析:(1)根据金属铝将水体中的NO3-转化为N2,可知Al为还原剂,则Al(OH)3为氧化产物,再根据电荷守恒和原子守恒可得:NO3- + Al +H2O→ Al(OH)3 + N2 + OH-;Al元素被氧化,N元素被还原,则被氧化与被还原的元素的物质的量分别为x、y,由电子守恒可知,x×(3-0)=y×(5-0),解得x:y=5:3,所以被氧化与被还原的元素的物质的量之比为5∶3。
(2)由电池总反应4Al+3O2+6H2O=4Al(OH)3可知,Al作负极,氧气在正极上得电子发生还原反应,正极反应为2H2O+O2+4e-=4OH-;Al元素由0价升高为+3价,则 Al~3e?,所以消耗13.5 g Al时转移电子:13.5g÷27g/mol×3=1.5mol。
(3)首先写出化学方程式并注明各物质的状态,然后根据盖斯定律求出?H,?H="1/2" ?H1+?H2
本题难度:困难
2、填空题 (8分)请根据反应:Fe + Cu2+ = Fe 2++ Cu 设计原电池:
(1) (2分)画出实验的简易装置图:(用铅笔画图)
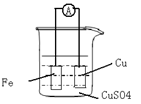
(2)(6分)写出电极反应式,正极: ,负极: 。当反应进行到一段时间后取出电极材料,测得某一电极增重了6.4g,则反应共转移了的电子数是 。
参考答案:(2) Cu2+ + 2e- = Cu 、 Fe
本题解析:
本题难度:一般
3、选择题 一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是 (?)?
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O
C.通入空气的一极是负极,电极反应为:O2 + 4e- = 2O2-
D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O
参考答案:B
本题解析:在原电池中,阳离子移向正极,阴离子移向负极,故A错误;氧气发生得电子的还原反应,故通氧气的一极为原电池的正极,通丁烷的为原电池的负极,故C、D均错误;故选B。
本题难度:一般
4、选择题 控制合适的条件,将反应2Fe3++2I- 2Fe2+I2设计成如下图所示的原电池。下列说法不正确的是
2Fe2+I2设计成如下图所示的原电池。下列说法不正确的是
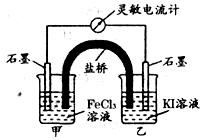
A.盐桥中的K+移向FeCl3溶液
B.反应开始时,乙中石墨电极上发生氧化反应
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
参考答案:D
本题解析:反应2Fe3++2I-?2Fe2++I2可知,铁元素的化合价降低,而碘元素的化合价升高,则图中甲烧杯中的石墨作正极,乙烧杯中的石墨作负极。A、根据电流方向,K+移向正极,即移向FeCl3溶液,正确;B、因乙中I-失去电子放电,元素的化合价升高,则发生氧化反应,正确;C、当电流计为零时,说明没有电子发生转移,则反应达到平衡,正确;D、当加入Fe2+,导致平衡逆向移动,则Fe2+失去电子生成Fe3+,作为负极,而乙中石墨成为正极,正确。
本题难度:一般
5、填空题 银器皿日久表面逐渐变黑色,这是由于生成了硫化银(Ag2S)。有人设计用原电池的原理进行“抛光”,其处理方法为:将一定浓度的食盐溶液放入一铝制容器中,再将变黑的银器浸入溶液中,放置一段时间后,黑色会褪去而银恢复光泽,且不会损失。试回答:
(1)食盐的作用是______________________。
(2)在此原电池反应中,负极发生的电极反应为_____________________________,正极发生的电极反应为____________________________。
(3)反应过程中产生臭鸡蛋气味的气体,溶液中发生的反应为2Al3++3S2-+6H2O==2Al(OH)3↓+3H2S↑,则原电池总反应方程式为____________________________。
参考答案:(1)食盐溶于水形成电解质溶液
(2)Al-3e-==Al3+;Ag2S+2e-==2Ag+S2-
(3)3Ag2S+2Al+6H2O==6Ag+2Al(OH)3↓+3H2S↑
本题解析:
本题难度:一般