1、填空题 常温下,在20.0 mL 0.20 mol/L CH3COONa溶液中滴加0.20 mol/L的稀盐酸。溶液的pH的变化关系如下图所示。
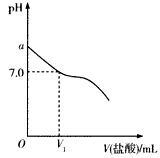
(1)a>7.0的理由是__________________(用离子方程式表示)。
(2)如图,当加入稀盐酸的体积为V1mL时,溶液的pH刚好为7.0。此时溶液中c(Cl-)___c(CH3COOH)(填 “<”、“>”或“=”)。简要写出判断依据:_____________________。
(3)当加入盐酸的体积为20.0 mL时,测得溶液中的c(H+)为1.3×10-3 mol/L,则CH3COOH的电离平衡常数Ka=_______(计算结果保留两位有效数字)。
2、选择题 下列叙述正确的是
A.某溶液中所有离子的浓度大小排序是:c(CH3COO-)> c(Na+)>c(H+)>c(OH-),则该溶液的溶质一定是CH3COONa和CH3COOH
B.CH3COOH与NaOH的混合溶液显碱性,则溶液中各离子浓度大小排序一定为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
C.常温下,a moL/L的CH3COOH溶液与b moL/L的NaOH溶液等体积混合后溶液的pH =7,则一定有a=b
D.常温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合后溶液的pH一定等于7
3、选择题 下列观点你认为正确的是(?)
A.某单质固体能导电,该单质一定是金属
B.某化合物的水溶液能导电,该化合物一定是电解质
C.纯水的导电性很差,所以水不是电解质
D.Na2O液态时能导电,所以Na2O是电解质
4、选择题 下列叙述正确的是
[? ]
A.强电解质的饱和溶液导电能力一定强
B.凡是能导电的物质都是电解质
C.强电解质在水溶液中的电离过程是不可逆的
D.强酸溶液的酸性一定强于弱酸溶液的酸性
5、选择题 下列说法正确的是
[? ]
A.向0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红
B.Al3+、NO3-、Cl-、CO32-、Na+可大量共存于pH=2的溶液中
C.在氯化铵溶液中离子浓度大小顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-)
D.H2SO3的电离方程式为H2SO3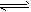 2H++SO32-
2H++SO32-