1、实验题 (12分)化学实验兴趣小组在实验室进行氢气在氯气中的燃烧实验。
(一)设计如下图所示装置I制备和收焦干燥纯净的氯气以备后续实验;
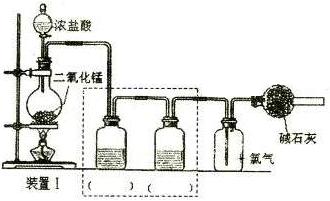
烧瓶中发生反应的离子方程式为?;
请根据实验目的将装置I中虚线框内装置补充完整并在括号内注明所需试剂;
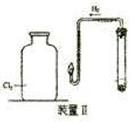
(二)在上图所示装置Ⅱ中,在试管中先加入过量铁粉,再滴入少量CaSO4溶液,最后加入一定量稀盐酸,塞上胶塞,观察到有大量气泡产生。
①检查制取氢气装置气密性的操作方法是?
②当点燃氢后,将导管伸入盛有氯气的集气瓶中,观察到的现象是?
(三)当氢气停止燃烧后,取出导管,同学们进行了分组探究实验。A组同学发现制氢气后的试管中还有较多固体剩余,同学们将足量氯气通入试管中,发现固体全部消失,但未观察到有气泡产生,请解释可能原因(用离子方程式表示);?;B组同学向集气瓶中注入适量水,用力振荡后,向中满入少量Na2SO3溶液,发现溶液中没有出现黄色沉淀,但再向溶液中滴入稀盐酸酸化的氯化钡溶液后,生成了白色沉淀。[已知Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O],同学们分析是由于集气瓶中还有少量氯气残留的缘故。可以解释该实验现象的两个离子方程式是:
①?
参考答案:Ⅰ:MnO2+4H++2Cl-?Mn2++Cl2↑+2H2O(2分)
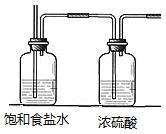 (2分);
(2分);
Ⅱ:将导气管末端插入水槽中,用手握住试管,在导气管末端会有气泡产生。松开手后,导气管末端有一段水柱上升,则证明该装置的气密性良好(1分);氢气安静地燃烧,发出苍白色火焰,瓶口出现白雾(1分)
Ⅲ:Cl2+2Fe2+= Cl-+2Fe3+? 2Fe3++Fe= 3Fe2+? 2Fe3++Cu = Cu2++ 2Fe2+
3Cl2+2Fe=" 2Fe" Cl3(4分)
4Cl2+S2O32-+5H2O=2SO42-+8Cl-+10H+? Ba2++SO42-=BaSO4↓(2分)
本题解析:略
本题难度:简单
2、选择题 下列有关实验的叙述或方法正确的是
A.用渗析的方法精制氢氧化铁胶体
B.滴定管、容量瓶在使用前均需用待装液润洗
C.加入适量NaOH溶液后过滤,以除去KCl溶液中少量的MgCl2
D.测定硫酸铜晶体中结晶水含量,加热坩埚中的晶体,失水后应在空气中冷却再称量
参考答案:A
本题解析:B中容量瓶不能用待装液润洗;C中会引入NaCl杂质;D中CuSO4・5H2O失水后应在干燥器中冷却。
本题难度:简单
3、选择题 如图装置可用于( )
A.用NH4Cl与浓NaOH溶液反应制NH3
B.用Cu与稀HNO3反应制NO
C.加热NaHCO3制CO2
D.用MnO2与浓HCl反应制Cl2
