1、实验题 用0.14mol・L-1 的NaOH溶液测定未知浓度的H2SO4溶液,其实验步骤如下:
(1)配制稀H2SO4溶液取10.00 mL 待测H2SO4溶液,配成1.00 L稀H2SO4溶液。在配制过程中,应选用下列仪器中的?(用序号填空)。
1烧瓶2锥形瓶3容量瓶4烧杯5酸式滴定管6漏斗7玻璃棒8胶头滴管9量筒
(2)滴定用酸式滴定管取稀释后硫酸溶液20.00 mL,注入?中,再滴入几滴酚酞试液,摇匀后,用0.14mol・L-1 的NaOH溶液进行滴定,直至加入最后一滴NaOH溶液时,恰好使溶液?即可停止滴定。
(3)计算
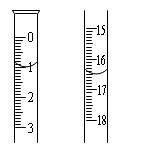
根据上图所示0.14mol・L-1 的NaOH溶液的用量,计算稀释前后H2SO4溶液的物质的量浓度?。
(4)碱式滴定管在注入0.14mol・L-1 的NaOH溶液之前,用水冼净之后,立即装入0.14mol・L-1 的NaOH溶液,其结果将会使测得的H2SO4溶液的物质的量浓度?(填“偏高”、“偏低”或“无影响”)。
(5)滴定前,盛稀释后H2SO4溶液的容器用水冼净后,用H2SO4溶液润冼,再准确量取20.00 mL 稀释后的H2SO4溶液,并滴入数滴酚酞试液,然后用NaOH溶液滴定。其结果将会使测得的H2SO4溶液的物质的量浓度?(填“偏高”、“偏低”或“无影响”)。
(6)滴定前,碱式滴定管内无气泡,在滴定结束时,管内进入气泡。记录消耗NaOH溶液体积时,未赶走气泡,结果将会使测得的H2SO4溶液的物质的量浓度?(填“偏高”、“偏低”或“无影响”)。
2、实验题 下图为常见气体制备、分离、干燥和性质验证的部分仪器装置(加热设备及夹持固定装置均略去,已知乙醇的沸点为78.5℃),请根据要求完成下列问题 (仪器装置可任意选用,必要时可重复选择,a、b为旋钮)。
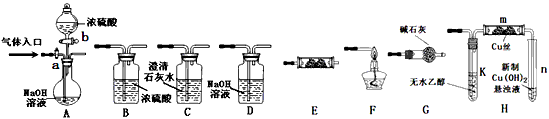
(1)①若A中气体入口通入CO和CO2的混合气体,E内放置CuO,欲得到纯净干燥的CO,并验证其还原性及氧化产物,所选装置的连接顺序为A→____→____→E→____→F (填写装置代号)。
②能验证CO氧化产物的实验现象是_____________________。
(2)完成实验⑴后,将A中旋钮a关闭,并在E内放置Na2O2,按A→E→D→B→H装置顺序,制取纯净干燥的O2,并用O2催化氧化乙醇。
①为获得氧气,关闭旋钮a后,首先需进行的操作是_____________________。
②为得到平稳的乙醇蒸气流,提高反应效率,可采取的措施是(用文字简述)____________________;
m中发生反应的化学方程式是____________________。
3、选择题 用体积为2 V L的试管收集SO2,采用的集气方法应是
[? ]
A.向上排空气法
B.向下排空气法
C.排水法
D.排食盐水法
4、填空题 (Ⅰ)某化学兴趣小组的同学得上用下 图所示实验装置进行实验(图中a、b、c表示止水夹)。
图所示实验装置进行实验(图中a、b、c表示止水夹)。
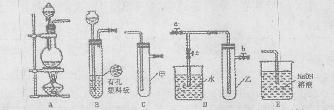
(1)请利用上述装置设计一个简单的实验验证Cl-和Br-的还原性强弱。
①选择合理的装置连接:?→?→?(填字母编号)。
②选择所需的试剂:?(填字母编号)。
a.固体氯化钠? b.固体二氧化锰? c.浓硫酸
d.浓盐酸? e.稀盐酸? f.溴化钠溶液
③实验现象及结论:?。
(Ⅱ)电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成。由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收并制备NiSO4・7H2O晶体,设计实验流程如下:

已知:①NiSO4易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的KSP及析出理论pH如下表所示:
M(OH)n
| Ksp[来
| pH
|
开始沉淀
| 沉淀完全
|
Al(OH)3
| 1.9×10-23
| 3.43
| 4.19
|
Fe(OH)3
| 3.8×10-38
| 2.53
| 2.94
|
Ni(OH)2
| 1.6×10-14
| 7.60
| 9.75
|
?回答下列问题:
(1)根据上表数据判断操作2依次析出的沉淀I是?沉淀II是?(填化学式),pH1?pH2(填“>”、“<”或“=”);
(2)操作1和操作2所用到的仪器除铁架台(带铁圈)、酒精灯、烧杯、玻璃棒外还需要的主要仪器为?。
(3)“调节pH为2-3”的目的是?;
(4)NiSO4在强碱溶溶中用NaClO氧化,可制得碱性镍镉电池电极材料――NiOOH。该反应的离子方程式是?。
5、选择题 以下气体能用NaOH固体干燥的是
A.NH3
B.SO2
C.CO2
D.HCl