1、选择题 在盛有碘水的三支试管中分别加入苯、四氯化碳和酒精,振荡后静置,出现如图所示现象,则加入的试剂分别是

A.①是酒精,②是CCl4,③是苯
B.①是苯,②是CCl4,③是酒精
C.①是CCl4,②是苯,③是酒精
D.①是苯,②是酒精,③是CCl4
参考答案:A
本题解析:苯能萃取溴水中的溴,但密度小于水的密度,所以看到的现象是溶液分层,上层呈紫红色,下层呈无色;四氯化碳能萃取溴水中的溴,但密度大于水的密度,所以看到的现象是溶液分层,下层呈紫红色,上层呈无色;酒精和溴水能互溶,所以看到的现象是溶液不分层,溶液为橙黄色。
本题难度:一般
2、选择题 为提纯下列物质(括号中为杂质),所选除杂试剂和分离的主要操作方法都合理的是
选项
| 被提纯的物质(杂质)
| 除杂试剂
| 主要操作方法
|
A
| NaHCO3溶液(Na2CO3)
| 澄清石灰水
| 过滤
|
B
| NaCl溶液(Br2)
| 乙醇
| 分液
|
C
| CO2(SO2)
| 饱和NaHCO3溶液
| 洗气
|
D
| KNO3溶液(KOH)
| FeCl3溶液
| 过滤
|
?
参考答案:C
本题解析:A、澄清石灰水与NaHCO3溶液和Na2CO3溶液都反应,错误;B、乙醇与NaCl溶液和Br2都能溶解,错误;C、饱和NaHCO3溶液能与二氧化硫反应生成二氧化碳,并且二氧化碳在碳酸氢钠中的溶解度很小,正确;D、引进了新的杂质氯离子,错误。
本题难度:一般
3、选择题 下列各组物质仅用水就能鉴别的是
①NO2和Br2蒸气?②硝基苯和苯?③固体NaOH和KNO3.
A.①②
B.②③
C.①③
D.①②③
参考答案:D
本题解析:分析:①根据二氧化氮和水反应以及溴蒸气溶于水分析;
②根据硝基苯不溶于水密度比水大以及苯不溶于水且密度比水小分析;
③根据氢氧化钠溶于水放热和硝酸钾溶于水吸热分析.
解答:①二氧化氮和溴蒸气都是红棕色气体,二氧化氮与水反应生成硝酸和无色的一氧化氮气体,而溴蒸气溶于水,溶液颜色为橙红色,二者现象不同,故可鉴别;
②硝基苯不溶于水密度比水大,油状液体在下层,苯不溶于水密度比水小,油状液体在上层,二者现象不同,可鉴别;
③氢氧化钠溶于水放热,硝酸钾溶于水吸热,二者溶于水后烧杯的温度不同,故可鉴别.
故①②③都可鉴别.
故选D.
点评:本题考查物质的鉴别,分别涉及物质的化学性质和物理性质,题目难度不大,注意物质的性质的区别.
本题难度:一般
4、选择题 要除去CO2气体中所含的少量HCl气体,最好的方法是将混合气通过( )
A.饱和NaHCO 3溶液
B.Na2CO3溶液
C.饱和石灰水
D.氨水
参考答案:A
本题解析:A、NaHCO3溶液能与盐酸反应生成氯化钠、水和二氧化碳,在除去氯化氢的同时增加了二氧化碳的量,故A正确;
B、Na2CO3溶液能够与二氧化碳反应,把二氧化碳也除去了,故B错误;
C、饱和的石灰水会吸收二氧化碳和氯化氢,把二氧化碳也除去了,故C错误;
D、氨水会吸收二氧化碳和氯化氢,把二氧化碳也除去了,故D错误.
故选A。
点评:进行物质除杂时,可以根据物质的性质,采用物理或化学的方法除去,要求所选的除杂试剂只与杂质反应,不能与原有物质反应,且反应后不能生成新的杂质。
本题难度:简单
5、填空题 以铝灰(主要成分为Al、Al2O3,另有少量CuO、SiO2、FeO和Fe2O3杂质)为原料,可制得液体聚合氯化铝Alm(OH)nCl3m-n,生产的部分过程如下图所示(部分产物和操作已略去)。
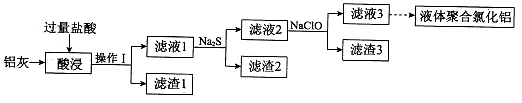
已知某些硫化物的性质如下表:

(1)操作I是?。Al2O3与盐酸反应的离子方程式是?。
(2)滤渣2为黑色,该黑色物质的化学式是?。
(3)向滤液2中加入NaClO溶液至不再产生红褐色沉淀,此时溶液的pH约为3.7。NaClO的作用是?。
(4)将滤液3的pH调至4.2~4.5,利用水解反应得到液体聚合氯化铝。反应的化学方程式是?。
(5)将滤液3电解也可以得到液体聚合氯化铝。装置如图所示(阴离子交换膜只允许阴离子通过,电极为惰性电极)。
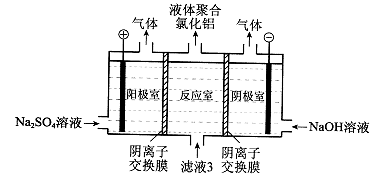
①写出阴极室的电极反应:?。
②简述在反应室中生成聚合氯他铝的原理:?。
参考答案:(1)过滤?(2分)Al2O3+6H+=2Al3++3H2O? (2分)
(2)CuS? (2分)
(3)将Fe2+氧化为Fe3+,使转化为Fe(OH)3沉淀?(2分)
(4)mAlCl3+nH2O=Alm(OH)nCl3m-n+nHCl? (写“ ”得分)(1分)
”得分)(1分)
(5)①2H++2e-=H2↑ (2分)
②电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中的OH-通过阴离子交换膜进入反应室,生成聚合氯化铝。(2分)
本题解析:(1)加入稀盐酸后,CuO、SiO2不溶于稀盐酸的杂质可过滤出,所以操作I是过滤;氧化铝与稀盐酸反应的离子方程式为Al2O3+6H+=2Al3++3H2O;
(2)根据硫化物的性质可知该黑色物质为CuS,因为硫化亚铁溶液稀盐酸中;
(3)加入次氯酸钠目的是把亚铁离子氧化成铁离子,转化为Fe(OH)3沉淀除去;
(4)根据聚合氯化铝的化学式和质量守恒定律,氯化铝水解的化学方程式为
mAlCl3+nH2O=Alm(OH)nCl3m-n+nHCl;
(5)①滤液3的主要成分是氯化铝,根据离子放电顺序,在阴极是阳离子放电,所以应为H+放电,电极反应为2H++2e-=H2↑;
②反应室两侧均为阴离子交换膜,电解过程中反应室中的Cl-通过阴离子交换膜进入阳极室,阴极室中OH-浓度增大,通过阴离子交换膜进入反应室,生成聚合氯化铝。
本题难度:一般