1������� ��14�֣��������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ� ����Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����1mol CO2��3mol H2����500oC�·�����Ӧ��
����Ϊ̽����Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1 L���ܱ������У�����1mol CO2��3mol H2����500oC�·�����Ӧ��
CO2(g)��3H2(g) CH3OH(g)��H2O(g)����H����49.0kJ/mol
CH3OH(g)��H2O(g)����H����49.0kJ/mol
���CO2��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
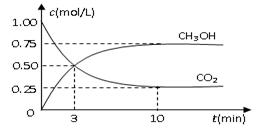
�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����
v(H2)��_________________________ _____��
_____��
�ڸ÷�Ӧ��ƽ�ⳣ��KΪ__________ ����ȷ��С�������λ����������¶ȵ�800oC���д�ƽ��ʱ��Kֵ__________��n(CH3OH)/n(CO2)��ֵ__________�������������������С�����䡱����
����ȷ��С�������λ����������¶ȵ�800oC���д�ƽ��ʱ��Kֵ__________��n(CH3OH)/n(CO2)��ֵ__________�������������������С�����䡱����
��ƽ��ʱCH3OH���������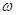 Ϊ__________��
Ϊ__________��
��������ͬ�����£���ʼʱ�������ʵ���Ϊ��a mol CO2��b mol H2��c mol CH3OH��c mol H2O����ƽ���CH3OH�����������Ϊ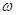 ����a��b��c�Ĺ�ϵΪ__________��
����a��b��c�Ĺ�ϵΪ__________��
��2�������˺���������̬ϵͳ�У�����Ҫ�����ȥ��CO2����Ҫ���ṩ�����O2��ij�ֵ绯ѧװ�ÿ�ʵ������ת����2CO2��2CO��O2��CO������ȼ�ϡ���֪�÷�Ӧ��������ӦΪ��4OH�D-4e�D��O2����2H2O����������ӦʽΪ_________ _____________________��
_____________________��
�ο��𰸣���1����0.225mol/(L��min)��5.33?��С?��С
��30%?��a+c="1" b+3c=3
��2��CO2+2e-+H2O=CO+2OH-
�����������
�����Ѷȣ�һ��
2��ѡ���� ��һ�ܱ������У���Ӧm A(g)��n B(g)  ?3C(g)�ﵽƽ��ʱ�����c(A)��0.5 mol/L�����¶Ȳ��������£����ݻ�����һ�������ﵽ�µ�ƽ��ʱ�����c(A)��0.25 mol/L�������ж�����ȷ����(? )
?3C(g)�ﵽƽ��ʱ�����c(A)��0.5 mol/L�����¶Ȳ��������£����ݻ�����һ�������ﵽ�µ�ƽ��ʱ�����c(A)��0.25 mol/L�������ж�����ȷ����(? )
A��A��������������?B��ƽ�ⷢ���ƶ�
C����ѧ��������m��n��3?D������C�����������С
�ο��𰸣�C
�����������һ�ܱ������У���Ӧm A(g)��n B(g)  ?3C(g)�ﵽƽ��ʱ�����c(A)��0.5 mol/L�����¶Ȳ��������£����ݻ�����һ��������ƽ�ⲻ�ƶ�ʱ��A��Ũ��Ӧ����c(A)��0.25 mol/L�����ﵽ�µ�ƽ��ʱ�����c(A)��0.25 mol/L������ƽ�ⲻ�ƶ�������Ӧǰ������Ļ�ѧ��������ͬ������m��n��3����ѡC��
?3C(g)�ﵽƽ��ʱ�����c(A)��0.5 mol/L�����¶Ȳ��������£����ݻ�����һ��������ƽ�ⲻ�ƶ�ʱ��A��Ũ��Ӧ����c(A)��0.25 mol/L�����ﵽ�µ�ƽ��ʱ�����c(A)��0.25 mol/L������ƽ�ⲻ�ƶ�������Ӧǰ������Ļ�ѧ��������ͬ������m��n��3����ѡC��
��������������֪������֪ʶ��ѹǿ�Ի�ѧƽ���Ӱ��Ĺ���Ϊ����Ӧǰ������Ļ�ѧ��������ͬ�Ļ�ѧ��Ӧ���ı�ѹǿ��ƽ�ⲻ�ƶ�������ƽ���ƶ���
�����Ѷȣ�һ��
3������� ��80��ʱ����0��4mol��A�������2L�ѳ�յĹ̶��ݻ����ܱ������з�����Ӧ��A(g) mB(g)��һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
mB(g)��һ��ʱ��Ը������ڵ����ʽ��з������õ��������ݣ�
ʱ�䣨s��
c��mol/L��
| 0
| 20
| 40
| 60
| 80
| 100
|
c��A��
| 0��20
| 0��14
| 0��10
| c
| d
| e
|
c��B��
| 0��00
| 0��12
| b
| 0��22
| 0��22
| 0��22
|
��m=?������b?c���<������=����>������
��100������������������С��ԭ��һ�룬ƽ��ʱB��Ũ��____________0.44 mol/L���<������=����>������
����80��ʱ�÷�Ӧ��ƽ�ⳣ��KֵΪ?������1λС������
��������������ͬʱ���÷�Ӧ��KֵԽ��������ƽ��ʱ?��
��A��ת����Խ��?��B�IJ���Խ��
��A��B��Ũ��֮��Խ��?������Ӧ���еij̶�Խ��
�ο��𰸣���2��> ��<?��0.5�� �Ȣ٢ۢ�
�����������1����Ӧ���е�20sʱ��A��B��Ũ�ȱ仯���ֱ���0.06mol/L��0.12mol/L������m��2������ݷ���ʽ��֪2����0.10��c����0.22��b�����b��2c��0.02������b����c��
100������������������С��ԭ��һ�룬˲��B��Ũ����0.44mol/L����ƽ�����淴Ӧ�����ƶ�������ƽ��ʱB��Ũ��С��0.44mol/L��
��3�����ݱ������ݿ�֪����Ӧ���е�60sʱ���ʵ�Ũ�Ȳ��ٷ����仯����Ӧ�ﵽƽ��״̬������B��Ũ����0.22mol/L����A��Ũ��Ӧ����0.20mol/L��0.11mol/L��0.09mol/L������ƽ�ⳣ��K��
��4����ѧƽ�ⳣ������һ�������£������淴Ӧ�ﵽƽ��״̬ʱ��������Ũ�ȵ���֮���ͷ�Ӧ��Ũ�ȵ���֮���ı�ֵ���ݴ˿�֪������÷�Ӧ��KֵԽ��������ƽ��ʱA��ת����Խ�ߡ�B�IJ���Խ������Ӧ���еij̶�Խ��A��B��Ũ��֮��Խ��ԽС����ѡ�٢ۢܡ�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������������ѧ���������������ͳ���˼ά���������ѧ��������û���֪ʶ���ʵ�������������
�����Ѷȣ�һ��
4��ѡ���� һ�������£����ݻ�������ܱ������м���P��Q���з�ӦP(g)+2Q(g)  3R(g)+S(l)��˵���÷�Ӧ�Ѵﵽƽ�����
3R(g)+S(l)��˵���÷�Ӧ�Ѵﵽƽ�����
A����Ӧ�����������ƽ��Ħ���������ٸı�
B����Ӧ������P��Q��R��S���߹���
C��2v��(Q)="3" v��(R)
D����Ӧ������ѹǿ����ʱ��仯���仯
�ο��𰸣�A
���������A����ȷ��B����ʹδ�ﵽƽ�⣬��Ӧ������P��Q��R��S����Ҳ�Ṳ�棬����C��2v��(Q)="3" v��(R) �Ǹ����ʽ�������Ƿ�ﵽƽ�⣬����D ����Ϊ��Ӧ�������������һ��������ѹǿһֱ���䣬����
�����Ѷȣ�һ��
5������� ��1����4�֣���ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2 2SO3 ��H<0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������?��bc�����иı������������?��
2SO3 ��H<0�ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����ab�����иı������������?��bc�����иı������������?��

��2����3�֣���֪���������Ȼ�ѧ����ʽ��
H2(g)�� O2(g) �� H2O( l )?��H����285.8 kJ��mol��1
O2(g) �� H2O( l )?��H����285.8 kJ��mol��1
C3H8(g)��5O2(g) �� 3CO2(g) +4H2O(l)?��H����2220.2 kJ��mol��1
ʵ����H2��C3H8�Ļ�����干5mol����ȫȼ������Һ̬ˮʱ����3847kJ������������H2��C3H8���������?
��3������3�֣�ʵ���ҽ��е���Ȼ�����Һʱ���������ռ���4.48L���壨����������跴Ӧ����Һ�������Ϊ200ml���������Һ���������Ƶ����ʵ���Ũ��?
�ο��𰸣���1�������¶ȡ���������SO3��Ũ�ȣ���2�֣�
��2��3��1?��3�֣�?��3��1mol/l��3�֣�
�����������
�����Ѷȣ�һ��