1、填空题 (10分)三氟化氮是一种无色、无味、无毒且不可燃的气体,可在铜的催化作用下由F2和过量NH3反应得到,在半导体加工,太阳能电池和液晶显示器的制造中得到广泛应用。它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO 和 HNO3,请根据要 求回答下列问题:
求回答下列问题:
⑴写出制备NF3的化学反应方程式:?。反应过程中,氧化剂与还原剂的物质的量之比为?。
⑵写出三氟化氮与水蒸气反应的化学方程式:?。⑶NF3是一种无色、无臭的气体,但一旦NF3在空气中泄漏,还是易于发现。你判断该气体
泄漏时的现象是?。
⑷一旦NF3泄漏,可以用NaOH溶液喷淋的方法减少污染。其产物除H2O外,还有另三种
钠盐:?(填化学式)。
2、填空题 (8分) 化合物A俗称石灰氮,以前是一种常用的肥料,其含氮量为35.0%,含钙量为50%。它可以用CaCO3通过下列步骤制得:

请回答下列问题:
(1)写出化学式:A________________、B________________;
(2)CaC2是__________________(填“离子”或“共价”)化合物;
(3)A与水完全反应的现象是产生白色沉淀并放出有刺激性气味的气体,写出A与水完全反应的化学方程式_______________________________________________________。
3、选择题 含n g硝酸的稀溶液恰好和m g铁粉完全反应若有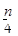 g HNO3被还原成NO,n:m可能
g HNO3被还原成NO,n:m可能
A.1:1
B.2:1
C.3:1
D.9:2
4、选择题 五氧化二磷不仅是一种强干燥剂,而且有很强的脱水性。向浓HNO3中加入过量的P2O5,能生成一种含氮的化合物M,则M最可能是(? )
A.N2
B.NO2
C.NO
D.N2O5
5、选择题 某溶液中含有大量Fe2+、Fe3+、Mg2+和NH4+,其C(H+)= 10-2mol/L,在该溶液中可以大量存在的阴离子是(?)
A.SO42-
B.NO3-
C.SCN-
D.CO32-